Chuyên đề Hóa 12 Bài 8 (Kết nối tri thức): Liên kết và cấu tạo của phức chất
Với giải bài tập Chuyên đề Hóa 12 Bài 8: Liên kết và cấu tạo của phức chất sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Chuyên đề học tập Hóa 12 Bài 8.
Giải Chuyên đề Hóa 12 Bài 8: Liên kết và cấu tạo của phức chất
Mở đầu trang 40 Chuyên đề Hóa học 12: Trong phức chất [MLn], các phối tử L sắp xếp xung quanh nguyên tử trung tâm M tạo ra các dạng hình học khác nhau. Vậy, sự hình thành liên kết trong phức chất tứ diện và phức chất bát diện được giải thích như thế nào theo thuyết liên kết hoá trị?
Lời giải:
Thuyết liên kết hoá trị giải thích sự hình thành liên kết hoá học giữa nguyên tử trung tâm M và phối tử L trong phức chất dựa trên các luận điểm cơ bản sau:
- Liên kết hoá học giữa M và L trong phức chất là liên kết cho – nhận. Phối tử cho cặp - electron chưa liên kết vào orbital lai hoá trống của nguyên tử trung tâm.
- Kiểu lai hoá của các orbital của nguyên tử trung tâm quyết định dạng hình học của phức chất.
|
Phức chất [MLn] |
Kiểu lai hóa của M |
Hình ảnh các orbital lai hóa |
Dạng hình học của phức chất |
|
[ML4] |
sp3 |
|
Tứ diện |
|
[ML6] |
d2sp3 hoặc sp3d2 |
|
Bát diện |
I. Liên kết trong phức chất
Câu hỏi và bài tập 1 trang 41 Chuyên đề Hóa học 12: Xác định nguyên tử trung tâm và kiểu lai hóa của nó trong phức chất [Zn(NH3)4]2+ (có dạng hình học tứ diện) và phức chất [CoF6]3−.
Lời giải:
|
Phức chất [Zn(NH3)4]2+ |
Phức chất [CoF6]3− |
|
|
Nguyên tử trung tâm |
Zn2+ |
Co3+ |
|
Kiểu lai hóa |
sp3 |
sp3d2 |
Câu hỏi và bài tập 2 trang 41 Chuyên đề Hóa học 12: Phức chất [CoCl2(en)2]+ có cấu tạo như sau:
a) Chỉ ra các phối tử trong phức chất trên và dung lượng phối trí của chúng.
b) Chỉ ra nguyên tử trung tâm trong phức chất trên và số phối trí của nó.
c) Nguyên tử trung tâm trong phức chất trên đã nhận cặp electron từ nguyên tử nào của các phối tử?
d) Nêu dạng hình học của phức chất trên.
Lời giải:
a) Phối tử H2NCH2CH2NH2 có dung lượng phối trí là 2. Phối tử Cl− có dung lượng phối trí là 1.
b) Nguyên tử trung tâm là Co3+ có số phối trí là 6.
c) Nguyên tử trung tâm trong phức chất trên đã nhận cặp electron từ nguyên tử N của phối tử H2NCH2CH2NH2 và cặp electron của ion Cl−.
d) Hình dạng của phức chất là bát diện.
Câu hỏi và bài tập 3 trang 42 Chuyên đề Hóa học 12: Biết phức chất [NiCl4]2- có dạng hình học tứ diện.
a) Xác định nguyên tử trung tâm và số phối trí của nguyên tử trung tâm.
b) Trình bày sự hình thành liên kết trong phức chất [NiCl4]2− theo thuyết liên kết hóa trị biết Ni có Z = 28.
Lời giải:
a) Nguyên tử trung tâm là Ni2+ số phối trí của nguyên tử trung tâm là 4.
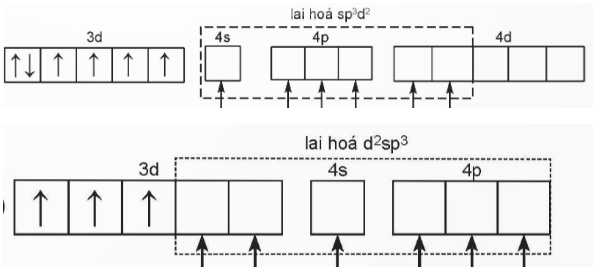
b) Nguyên tử trung tâm Ni2+ có cấu hình electron: 1s22s22p63s23p63d8
Để tạo ra dạng hình học tứ diện, nguyên tử trung tâm Ni2+ lai hóa sp3, bốn phối tử Cl− cho cặp electron chưa liên kết vào bốn orbital lai hóa sp3 trống của Ni2+, tạo thành bốn liên kết σ.
Sự hình thành bốn liên kết σ này có thể được biểu diễn như sau:
Câu hỏi và bài tập 4 trang 43 Chuyên đề Hóa học 12: Dự đoán dạng hình học của phức chất [Ti(H2)6]3+ và kiểu lai hóa của nguyên tử trung tâm trong phức chất, biết Ti có Z = 22.
Lời giải:
Nguyên tử trung tâm Ti3+ có cấu hình electron là 1s22s22p63s23p63d1
Dựa đoán hình dạng của phức chất là bát diện. Nguyên tử trung tâm Ti3+ lai hóa d2sp3.
Câu hỏi và bài tập 5 trang 43 Chuyên đề Hóa học 12: Mô tả sự hình thành phức chất [FeF6]3- theo thuyết liên kết hóa trị. Biết Fe có Z = 26.
Lời giải:
Nguyên tử trung tâm Fe3+ có cấu hình electron là 1s22s22p63s23p63d5
Nguyên tử trung tâm Fe3+ lai hóa sp3d2, sau phối tử F− cho cặp electron chưa liên kết vào sáu orbital lai hóa sp3d2 trống của Fe3+ tạo thành sáu liên kết σ.
Sự hình thành sáu liên kết σ này có thể được biểu diễn như sau:
II. Biểu diễn dạng hình học của phức chất
Hoạt động nghiên cứu trang 43 Chuyên đề Hóa học 12: Biểu diễn dạng hình học của phức chất tứ diện [NiCl4]2− và phức chất bát diện [Fe(H2O)6]3+.
Lời giải:
Phức tứ diện [NiCl4]2−:
Phức bát diện [Fe(H2O)6]3+:
III. Một số đồng phân cơ bản của phức chất
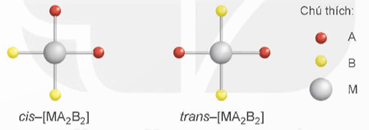
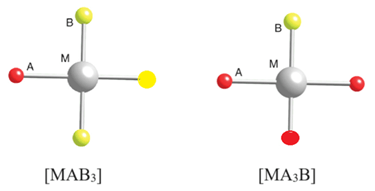
Hoạt động nghiên cứu trang 44 Chuyên đề Hóa học 12: Xét phức chất vuông phẳng có nguyên tử trung tâm M và hai loại phối tử A, B. Cả A và B đều có dung lượng phối trí là 1.
1. Viết các công thức hóa học có thể có của phức chất (bỏ qua điện tích của phức chất).
2. Biểu diễn dạng hình học có thể có của các phức chất.
Lời giải:
1. Công thức hóa học có thể có là: cis−[MA2B2], trans−[MA2B2], [MAB3] và [MA3B].
2.
Câu hỏi và bài tập 6 trang 45 Chuyên đề Hóa học 12: Cho các phức chất sau: [Ag(NH3)2]+, [ZnCl4]2-, [Ni(CN)4]2-, [PtCl2(NH3)2] (vuông phẳng).
a) Phức chất nào có đồng phân cis-, trans-?
b) Vẽ đồng phân cis-, trans- (nếu có) của mỗi phức chất.
Lời giải:
a) Phức chất có đồng phân Cis- là: [ZnCl4]2-, [Ni(CN)4]2-, [PtCl2(NH3)2]
Phức chất có đồng phân Trans- là : [PtCl2(NH3)2]
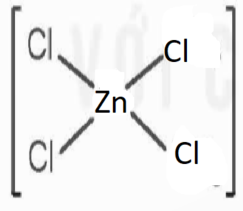
Đồng phân cis của [ZnCl4]2-:
Đồng phân cis của [Ni(CN)4]2-:
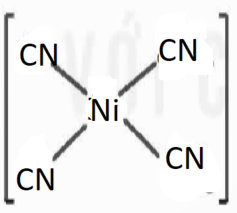
Đồng phân cis của [PtCl2(NH3)2]:
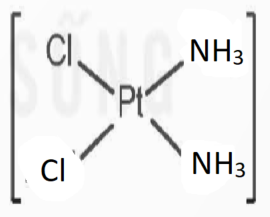
Đồng phân trans của [PtCl2(NH3)2]:
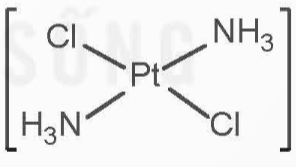
Hoạt động nghiên cứu trang 45 Chuyên đề Hóa học 12: Xét phức chất [MA4B2], trong đó phối tử A, B đều có dung lượng phối trí là 1.
1. Xác định số phối trí của nguyên tử trung tâm M và dạng hình học của phức chất.
2. Biểu diễn dạng hình học có thể có của phức chất.
Lời giải:
Nội dung đang được cập nhật...
Câu hỏi và bài tập 7 trang 45 Chuyên đề Hóa học 12: Cho phức chất: [Ni(NH3)6]2+ và [PdCl2(NH3)4].
a) Phức chất nào có đồng phân cis-, trans-?
b) Vẽ đồng phân cis-, trans- (nếu có) của mỗi phức chất
Lời giải:
Nội dung đang được cập nhật...
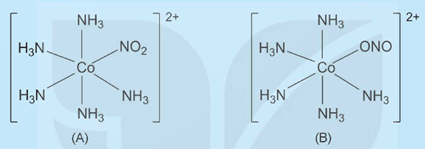
Câu hỏi và bài tập 8 trang 46 Chuyên đề Hóa học 12: Phức chất (A) và phức chất (B) có cấu tạo như sau:
Lời giải:
Hãy chỉ ra sự khác nhau về cấu tạo của hai phức chất này.
Lời giải:
Sự khác nhau giữa hai phức chất:
Phức chất A, có phối tử NO−2 liên kết với nguyên tử trung tâm Co3+ qua nguyên tử N.
Phức chất B, có phối tử NO−2 liên kết với nguyên tử trung tâm Co3+ qua nguyên tử O.
Em có thể trang 47 Chuyên đề Hóa học 12: Mô tả được sự hình thành liên kết của một số phức chất tứ diện và bát diện theo thuyết liên kết hóa trị.
- Biểu diễn được dạng hình học của một số phức chất dạng tứ diện và bát diện
- Xác định được đồng phân cis-, trans-, đồng phân liên kết, đồng phân ion hóa của một số phức chất.
Lời giải:
Theo thuyết liên kết hoá trị, liên kết trong phức chất có dạng hình học tứ diện được hình thành từ sự cho cặp electron chưa liên kết của phối tử vào các orbital lai hoá sp3 trống của nguyên tử trung tâm.
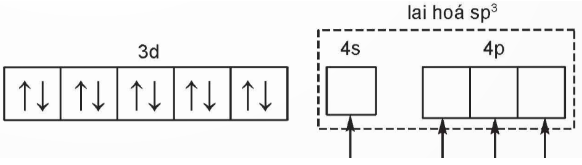
Theo thuyết liên kết hoá trị, liên kết trong phức chất có dạng hình học bát diện (còn được gọi là phức chất bát diện) được hình thành từ sự cho cặp electron chưa liên kết của phối tử đến các orbital lai hoá d2sp3 hoặc sp3d2 trống của nguyên tử trung tâm.
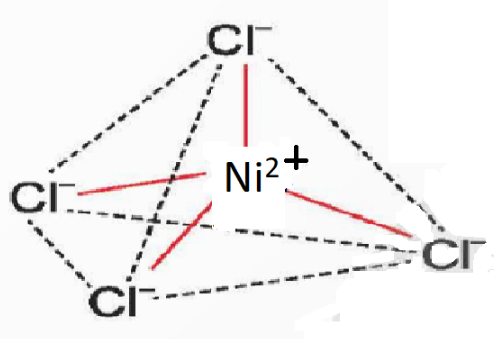
Ví dụ như hình học của phức chất tứ diện [NiCl4]2-;
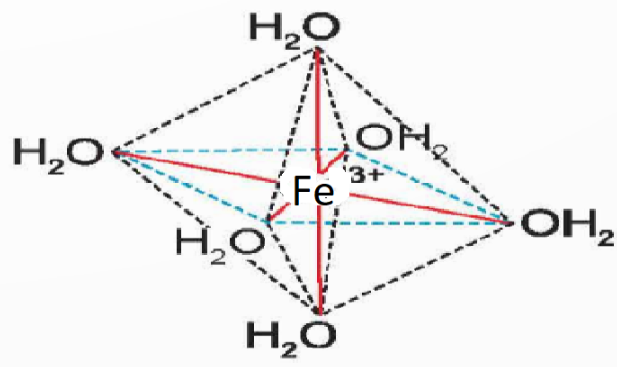
Hình học của phức chất bát diện [Fe(H2O)6]3+:
Đồng phân cis là phức chất với hai phối tử giống nhau nằm cùng một phía với nguyên tử trung tâm. Vd: [Ni(NH3)6]2+
Đồng phân trans là phức chất với hai phối tử nằm khác phía với nguyên tử trung tâm. Vd: [PdCl2(NH3)4]. Có cả cis và trans.
Đồng phân liên kết có thể xuất hiện khi phối tử có hai hay nhiều nguyên tử có khả năng tạo liên kết cho nhận với nguyên tử trung tâm.
Đồng phân ion hoá của phức chất có thành phần trong cầu nội và cầu ngoại khác nhau.
Xem thêm các chương trình khác:
- Soạn văn 12 Kết nối tri thức (hay nhất)
- Văn mẫu 12 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 12 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn 12 - Kết nối tri thức
- Bố cục tác phẩm Ngữ văn 12 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn 12 – Kết nối tri thức
- Giải sgk Toán 12 – Kết nối tri thức
- Giải Chuyên đề học tập Toán 12 – Kết nối tri thức
- Lý thuyết Toán 12 – Kết nối tri thức
- Giải sbt Toán 12 – Kết nối tri thức
- Bài tập Tiếng Anh 12 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 12 - Global success
- Trọn bộ Từ vựng Tiếng Anh 12 Global success đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 12 Global success đầy đủ nhất
- Giải sbt Tiếng Anh 12 – Global Success
- Giải sgk Vật lí 12 – Kết nối tri thức
- Giải Chuyên đề học tập Vật lí 12 – Kết nối tri thức
- Lý thuyết Vật lí 12 – Kết nối tri thức
- Giải sbt Vật lí 12 – Kết nối tri thức
- Giải sgk Sinh học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Sinh học 12 – Kết nối tri thức
- Lý thuyết Sinh học 12 – Kết nối tri thức
- Giải sbt Sinh học 12 – Kết nối tri thức
- Giải sgk Lịch sử 12 – Kết nối tri thức
- Giải Chuyên đề học tập Lịch sử 12 – Kết nối tri thức
- Giải sbt Lịch sử 12 – Kết nối tri thức
- Giải sgk Địa lí 12 – Kết nối tri thức
- Giải Chuyên đề học tập Địa lí 12 – Kết nối tri thức
- Giải sbt Địa lí 12 – Kết nối tri thức
- Giải sgk Tin học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Tin học 12 – Kết nối tri thức
- Giải sbt Tin học 12 – Kết nối tri thức
- Lý thuyết Tin học 12 - Kết nối tri thức
- Giải sgk Công nghệ 12 – Kết nối tri thức
- Giải sgk Kinh tế pháp luật 12 – Kết nối tri thức
- Giải Chuyên đề học tập Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sbt Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng 12 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 12 – Kết nối tri thức

![Trong phức chất [MLn] các phối tử L sắp xếp xung quanh nguyên tử trung tâm M](https://vietjack.com/chuyen-de-hoa-12/images/mo-dau-trang-40-chuyen-de-hoa-hoc-12-kntt.PNG)
![Trong phức chất [MLn] các phối tử L sắp xếp xung quanh nguyên tử trung tâm M](https://vietjack.com/chuyen-de-hoa-12/images/mo-dau-trang-40-chuyen-de-hoa-hoc-12-kntt-1.PNG)
![Phức chất [CoCl2(en)2]+ có cấu tạo như sau trang 41 Chuyên đề Hóa 12](https://vietjack.com/chuyen-de-hoa-12/images/cau-hoi-va-bai-tap-2-trang-41-chuyen-de-hoa-hoc-12-kntt.PNG)
![Biết phức chất [NiCl4]2- có dạng hình học tứ diện trang 42 Chuyên đề Hóa 12](https://vietjack.com/chuyen-de-hoa-12/images/cau-hoi-va-bai-tap-3-trang-42-chuyen-de-hoa-hoc-12-kntt.PNG)
![Mô tả sự hình thành phức chất [FeF6]3- theo thuyết liên kết hóa trị Biết Fe có Z](https://vietjack.com/chuyen-de-hoa-12/images/cau-hoi-va-bai-tap-5-trang-43-chuyen-de-hoa-hoc-12-kntt.PNG)
![Biểu diễn dạng hình học của phức chất tứ diện [NiCl4]2- và phức chất bát diện [Fe(H2O)6]3+](https://vietjack.com/chuyen-de-hoa-12/images/hoat-dong-nghien-cuu-trang-43-chuyen-de-hoa-hoc-12-kntt.PNG)
![Biểu diễn dạng hình học của phức chất tứ diện [NiCl4]2- và phức chất bát diện [Fe(H2O)6]3+](https://vietjack.com/chuyen-de-hoa-12/images/hoat-dong-nghien-cuu-trang-43-chuyen-de-hoa-hoc-12-kntt-1.PNG)