Trắc nghiệm Nhận biết một số ion trong dung dịch (có đáp án)
Trắc nghiệm Bài 40: Nhận biết một số ion trong dung dịch
-
382 lượt thi
-
30 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Các muối cần nhận biết đều là muối của Na+, chúng chỉ khác nhau gốc axit, do đó thuốc thử cần dùng là thuốc thử có thể giúp nhận ra được các gốc axit này.
Khi đó thuốc thử thường dùng là các dung dịch axit mạnh như HCl, H2SO4,...Ta có cách nhận biết và hiện tượng quan sát được như sau: Khi cho dung dịch HCl vào các mẫu thử thì:
+ Mẫu thử phản ứng với dung dịch HCl và giải phóng khí không màu không mùi là Na2CO3
Na2CO3 + 2HCl 2NaCl + 2CO2+ H2O
+ Mẫu thử phản ứng với dung dịch HCl giải phóng khí mùi trứng thối là Na2S
Na2S + 2HCl 2NaCl + H2S
+ Mẫu thử phản ứng với dung dịch HCl giải phóng khí mùi hắc là Na2SO3
Na2SO3 + 2HCl 2NaCl + 2SO2 + H2O
+ Mẫu thử không phản ứng mà chỉ tan trong dung dịch HCl là Na2SO4.
Câu 2:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Trích mẫu thử của 3 dung dịch ra 3 ống nghiệm có đánh số.
Sử dụng dung dịch NaOH nhỏ vào từng mẫu thử.
+ Nếu không xuất hiện hiện tượng gì → Na2CO3
+ Nếu xuất hiện kết tủa trắng không tan khi NaOH dư → MgCl2
MgCl2 + 2NaOH → Mg(OH)2↓ + 2NaCl
+ Nếu xuất hiện kết tủa keo trắng, kết tủa tan khi NaOH dư → Al(NO3)3
Al(NO3)3 + 3NaOH → Al(OH)3↓ + 3NaNO3
Al(OH)3 ↓+ NaOH → NaAlO2 + 2H2O
Câu 3:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Trích mẫu thử của 4 dung dịch ra 4 ống nghiệm có đánh số.
Sử dụng dung dịch Ba(OH)2 nhỏ vào từng mẫu thử.
+ Nếu xuất hiện kết tủa trắng, kèm theo khí mùi khai thoát ra → (NH4)2SO4
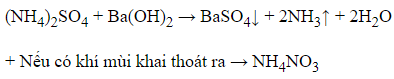
NH4+ + OH- → NH3↑ + H2O
+ Nếu có kết tủa trắng → Na2CO3
Ba2+ + CO32- → BaCO3↓
+ Không hiện tượng → NaNO3
Câu 4:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Trích mẫu thử của 4 dung dịch ra 4 ống nghiệm có đánh số.
Sử dụng dung dịch BaCl2 nhỏ vào từng mẫu thử.
+ Nếu xuất hiện kết tủa trắng
→ H2SO4; Na2CO3 (nhóm I)
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
BaCl2 + Na2CO3 → BaCO3↓ + 2NaCl
+ Nếu không có hiện tượng xuất hiện
→ NaOH; HCl (nhóm II)
Lấy lần lượt hóa chất ở nhóm II, cho vào từng kết tủa ở nhóm I
+ Nếu không xuất hiện hiện tượng gì ở mỗi kết tủa
→ Mẫu thử ở nhóm II là NaOH
+ Mẫu thử nhóm II là HCl: Nếu 1 kết tủa tan, có khí thoát ra (→ kết tủa là BaCO3 → mẫu thử ban đầu là Na2CO3); 1 kết tủa không tan (→ kết tủa là BaSO4 → mẫu thử ban đầu là H2SO4)
BaCO3 + 2HCl → BaCl2 + CO2↑ + H2O
Câu 5:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Thuốc thử cần dùng là dung dịch HCl, đun nóng
+) CuO + HCl → dung dịch màu xanh dương
CuO + 2HCl → CuCl2 + H2O
+) FeO + HCl → dung dịch màu xanh nhạt (gần như không màu)
FeO + 2HCl → FeCl2 + H2O
+) Fe3O4 + HCl → dung dịch màu vàng
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
+) MnO2 + HCl → tạo khí màu vàng lục
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
+) Ag2O + HCl → chất rắn chuyển nâu đen sang trắng
Ag2O↓ (đen) + 2HCl → 2AgCl↓ (trắng) + H2O
+) (Fe + FeO ) + HCl → khí, dung dịch màu xanh nhạt
Fe + 2HCl → FeCl2 + H2↑
FeO + 2HCl → FeCl2 + H2O
Câu 6:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Bước 1. Dùng dung dịch BaCl2
Ba2+ + → BaSO4
Lọc kết tủa được dung dịch gồm:
Na+, Mg2+, Ca2+, Ba2+, Cl-
Bước 2. Thêm dung dịch Na2CO3 dư
R2+ + → RCO3
(R2+ là Mg2+, Ba2+, Ca2+)
Lọc kết tủa thu được dung dịch gồm:
Na+, , Cl-
Bước 3. Dùng dung dịch HCl
+ 2H+ → CO2 + H2O
Cô cạn dung dịch thu được NaCl
Câu 7:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Trích mẫu thử của 2 dung dịch ra 2 ống nghiệm có đánh số
Nhỏ dung dịch Ba(NO3)2 vào hai mẫu thử:
+ Xuất hiện kết tủa trắng: Na2SO4
Ba(NO3)2 + Na2SO4 → BaSO4 + NaNO3
+ Không có hiện tượng gì: NaNO3
Câu 8:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Trích các mẫu thử của 6 dung dịch ra 6 ống nghiệm có đánh số.
Thả vào mỗi ống nghiệm một mẩu Ba. Khi đó Ba phản ứng với nước trong dung dịch sinh ra Ba(OH)2 và giải phóng khí H2 trước.
Ba + 2H2O → Ba(OH)2 + H2
+ Ống nghiệm xuất hiện kết tủa trắng, lẫn kết tủa xanh → CuSO4.
CuSO4 + Ba(OH)2 → Cu(OH)2↓ + BaSO4↓.
+ Ống nghiệm xuất hiện kết tủa nâu đỏ → FeCl3
2FeCl3 + 3Ba(OH)2 → 3BaCl2 + 2Fe(OH)3↓
+ Ống nghiệm xuất hiện kết tủa, sau đó kết tủa tan một phần → Al2(SO4)3
Al2(SO4)3 + 3Ba(OH)2 → 3BaSO4↓ + 2Al(OH)3↓
2Al(OH)3 + Ba(OH)2 → Ba(AlO2)2 + 4H2O
+ Ống nghiệm chỉ xuất hiện kết tủa trắng
→ K2CO3
K2CO3 + Ba(OH)2 → 2KOH + BaCO3↓
+ Ống nghiệm xuất hiện kết tủa trắng đồng thời có khí mù khai bay ra
→ (NH4)2SO4.
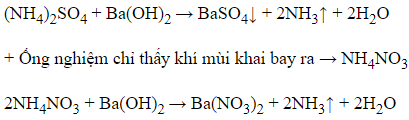
Câu 9:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Sử dụng dung dịch AgNO3 để nhận biết:
+ Dung dịch phản ứng với AgNO3 làm xuất hiện kết tủa trắng là HCl:
AgNO3 + HCl AgCl + HNO3
+ Dung dịch phản ứng với AgNO3 làm xuất hiện kết tủa vàng đậm là KI:
AgNO3 + KI AgI + KNO3
+ Dung dịch phản ứng với AgNO3 làm xuất hiện kết tủa vàng nhạt là ZnBr2:
2AgNO3 + ZnBr2 Zn(NO3)2 + 2AgBr
+ Dung dịch khi cho AgNO3 không có hiện tượng gì là Mg(NO3)2
Câu 10:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
- Dùng quỳ tím phân 4 mẫu thử thành 2 nhóm:
+ Nhóm 1: Nhóm các mẫu thử làm quỳ tím hóa đỏ: H2SO4 và HCl.
+ Nhóm 2: Nhóm mẫu thử không làm đổi màu quỳ tím: BaCl2 và NaCl.
- Lấy lần lượt các mẫu thử thuộc nhóm 1 cho vào các mẫu thử thuộc nhóm 2, mẫu thử nào phản ứng với nhau tạo kết tủa trắng là H2SO4 (nhóm 1) và BaCl2 (nhóm 2).
H2SO4 + BaCl2 → BaSO4 + HCl
Câu 11:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Hiện tượng khi cho dung dịch Na2CO3 vào các mẫu thử:
+ Mẫu thử không có hiện tượng: NaCl.
+ Mẫu thử xuất hiện kết tủa trắng là CaCl2:
+ Mẫu thử xuất hiện khí không màu và kết tủa keo trắng là A1Cl3:
![]()
Câu 12:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Câu 13:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Trích mẫu thử của ba dung dịch ra ba ống nghiệm có đánh số
Các hiện tượng và nhận biết:
+) Dung dịch không hòa tan được BaCO3 là KOH.
+) Dung dịch hòa tan được BaCO3 và giải phóng khí không màu là HCl:
BaCO3 + 2HCl BaCl2 + CO2 + H2O
+) Dung dịch hòa tan được BaCO3, giải phóng khí không màu đồng thời xuất hiện kết tủa trắng không tan trong mẫu thử dư là dung dịch H2SO4 :
BaCO3 + H2SO4 BaSO4+ CO2 + H2O
Câu 14:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Sử dụng dung dịch Ba(OH)2 làm thuốc thử thì ta nhận biết được các chất như sau:
+ Dung dịch phản ứng với thuốc thử làm xuất hiện kết tủa trắng là Na2CO3:
Na2CO3 + Ba(OH)2 BaCO3 + 2NaOH
+ Dung dịch phản ứng với thuốc thử giải phóng khí mùi khai là NH4NO3 :
![]()
+ Dung dịch mà khi cho thuốc thử vào chuyển sang màu đỏ là phenolphatlein.
+ Dung dịch mà khi cho thuốc thử vào không có hiện tượng là NaNO3.
Câu 15:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Trích mẫu thử của 3 dung dịch ra 3 ống nghiệm có đánh số.
+ Mẫu thử phản ứng với BaCl2 xuất hiện kết tủa trắng là H2SO4.
BaCl2 + H2SO4 BaSO4 + 2HCl
+ Mẫu thử hòa tan Cu giải phóng khí không màu hóa nâu trong không khí là HNO3.
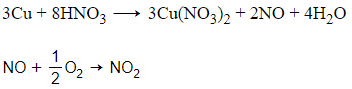
+ Mẫu thử còn lại là HCl.
Câu 16:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Trích mẫu thử của ba dung dịch ra 3 ống nghiệm có đánh số
Ta sử dụng ion OH- để nhận biết các dung dịch trên
Hiện tượng quan sát và nhận biết khi cho dung dịch chứa OH- vào các mẫu thử :
+ Xuất hiện kết tủa nâu đỏ → FeCl3
Fe3+ + 3OH- → Fe(OH)3
+ Xuất hiện kết tủa trắng xanh → FeCl2
Fe2+ + 2OH- → Fe(OH)2
+ Xuất hiện kết tủa keo trắng tan trong OH- dư → Al3+
Al3+ + 3OH- → Al(OH)3
Al(OH)3 + OH- → + 2H2O
→ Cả ba thuốc thử NaOH, KOH, Ba(OH)2 đều có thể sử dụng được.
Câu 17:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án D
- Đánh số thứ tự từng lọ mất nhãn, trích mỗi lọ một ít sang ống nghiệm đánh số tương ứng.
- Sử dụng dung dịch Ba(OH)2
+ Có khí mùi khai bay ra: NH4NO3
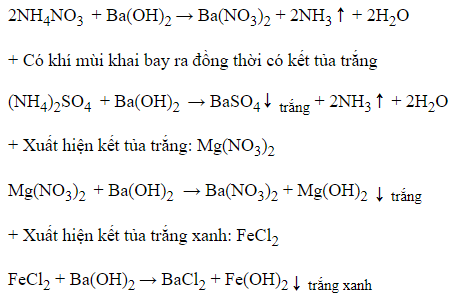
+ Không có hiện tượng gì: NaCl
Câu 18:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Sử dụng dung dịch Ba(OH)2
+ Không hiện tượng: KOH.
+ Xuất hiện kết tủa trắng đồng thời có khí mùi khai: (NH4)2SO4
Phương trình hóa học:
![]()
+ Chỉ có khí mùi khai: NH4Cl
Phương trình hóa học:
2NH4Cl + Ba(OH)2 → BaCl2 + 2NH3+ 2H2O
+ Chỉ có kết tủa trắng: Na2SO4
Phương trình hóa học:
Na2SO4 + Ba(OH)2 → BaSO4 (↓ trắng) + 2NaOH
Câu 19:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Cho Ba(OH)2 phản ứng lần lượt với từng chất:
- Có kết tủa trắng xuất hiện, không tan trong Ba(OH)2 dư: dung dịch là K2CO3.
Ba(OH)2 + K2CO3 → BaCO3 + 2KOH
- Có kết tủa trắng xanh xuất hiện, để lâu kết tủa chuyển màu nâu đỏ: dung dịch là FeCl2.
FeCl2 + Ba(OH)2 → BaCl2 + Fe(OH)2
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
- Có kết tủa trắng xuất hiện, tan khi thêm dư Ba(OH)2: dung dịch là CrCl3.
3Ba(OH)2 + 2CrCl3 → 2Cr(OH)3 + 3BaCl2
2Cr(OH)3 + Ba(OH)2 → Ba(CrO2)2 + 4H2O
- Không có hiện tượng gì: dung dịch là NaCl.
Câu 20:
22/07/2024Cho 4 lọ dung dịch riêng biệt X, Y, Z, T chứa các chất khác nhau trong số 4 chất: (NH4)2CO3, NaHCO3, NaNO3, NH4NO3. Thực hiện nhận biết bốn dung dịch trên bằng dung dịch Ba(OH)2 thu được kết quả sau:
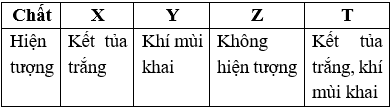
Nhận xét nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án D
+) X + Ba(OH)2 → Kết tủa trắng
→ X là NaHCO3.
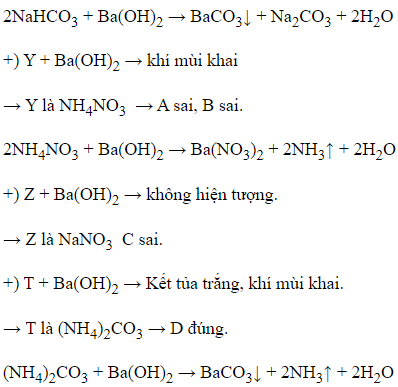
Câu 21:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Dùng BaCO3 vì:
![]()
BaCO3 + 2HCl → BaCl2 + CO2↑ + H2O
BaCO3 không tác dụng với NaCl.
Câu 22:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Trích mẫu thử của mỗi dung dịch ra từng ống nghiệm có đánh số tương ứng.
Nhỏ dung dịch AgNO3 vào từng mẫu thử để phân biệt
+ Xuất hiện kết tủa trắng: KCl
KCl + AgNO3 → AgCl (↓ trắng) + KNO3
+ Xuất hiện kết tủa vàng nhạt: KBr
KBr + AgNO3 → AgBr (↓ vàng nhạt) + KNO3
+ Xuất hiện kết tủa vàng đậm: KI
KI + AgNO3 → AgI (↓ vàng đậm) + KNO3
+ Không có hiện tượng gì: KF
Câu 23:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Trích mẫu thử của các dung dịch ra từng ống nghiệm có đánh số.
Ta nhỏ dung dịch AgNO3 vào từng mẫu thử
- Xuất hiện kết đen thì đó là Na2S
Na2S + AgNO3 → NaNO3 + AgS(↓ đen)
- Xuất hiện kết tủa trắng thì đó là NaCl
NaCl + AgNO3 → NaNO3 + AgCl (↓ trắng)
- Xuất hiện kết tủa vàng nhạt thì đó là NaBr
NaBr + AgNO3 → NaNO3 + AgBr(↓ vàng nhạt)
Câu 24:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
- Trích mẫu thử của mỗi chất cho ra các ống nghiệm khác nhau và đánh số thứ tự tương ứng.
- Cho dung dịch Ba(OH)2 vào các dung dịch trên
+ Dung dịch xuất hiện kết tủa trắng và mùi khai là: NH4HCO3 và (NH4)2CO3 (nhóm I)
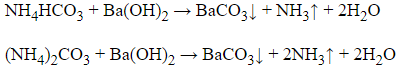
+ Dung dịch chỉ xuất hiện kết tủa trắng là: NaHCO3, Na2CO3 và H2SO4 (nhóm II)
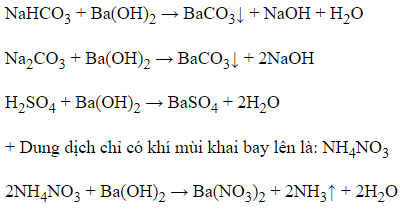
+ Dung dịch không có hiện tượng gì là HCl
2HCl + Ba(OH)2 → BaCl2 + 2H2O
- Lấy dung dịch HCl đã nhận biết được nhỏ lần lượt vào kết tủa vừa thu được ở nhóm II
+ Kết tủa tan là BaCO3 → dung dịch ban đầu là: NaHCO3 và Na2CO3 (nhóm III)
BaCO3 + 2HCl → BaCl2 + H2O + CO2
+ Kết tủa không tan là BaSO4 → dung dịch ban đầu là H2SO4
- Cho dd BaCl2 lần lượt vào các chất ở nhóm (I), nhóm (III)
+ Nhóm I: xuất hiện kết tủa trắng là (NH4)2CO3 còn lại không có hiện tượng gì là NH4HCO3
(NH4)2CO3 + BaCl2 → BaCO3↓ + NH4Cl
+ Nhóm II: xuất hiện kết tủa trắng là Na2CO3 còn lại không có hiện tượng gì là NaHCO3
Na2CO3 + BaCl2 → BaCO3↓ + 2NaCl
Câu 25:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Cho NaHCO3 lần lượt vào các chất
Có khí thát ra là HCl, Có kết tủa xuất hiện là Ca(OH)2, còn lại không có hiện tượng gì là CaCl2
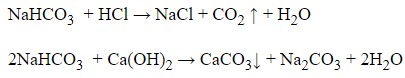
Câu 26:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Cho dung dịch Ca(OH)2 dư vào các mẫu phân bón trên
- Nếu xuất hiện kết tủa trắng thì đó là Ca(H2PO4)2
Ca(H2PO4)2 + 2Ca(OH)2 → Ca3(PO4)2 (↓ trắng) + 4H2O
- Nếu vừa xuất hiện kết tủa trắng vừa có khí mùi khai thì đó là NH4H2PO4
2NH4H2PO4 + 3Ca(OH)2 → Ca3(PO4)2 (↓ trắng) + 2NH3 + 6H2O
- Nếu chỉ xuất hiện khí có mùi khai thì đó là NH4NO3
2NH4NO3 + Ca(OH)2 → Ca(NO3)2 + 2NH3 + 2H2O
- Không thấy hiện tượng gì là KCl.
Câu 27:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án D
- Dùng quì tím: chỉ nhận biết được dung dịch KOH.
- Dùng Zn, Al: không nhận biết được.
- Dùng BaCO3:
+ Cho vào dung dịch KOH không có hiện tượng
+ Cho vào dung dịch HCl có khí bay lên
BaCO3 + 2HCl → BaCl2 + CO2 + H2O
+ Cho vào dung dịch H2SO4: có khí bay lên và kết tủa trắng
BaCO3 + H2SO4 → BaSO4 + CO2 + H2O
Câu 28:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Trích mẫu thử của 4 dung dịch ra 4 ống nghiệm có đánh số.
Nhỏ dung dịch NaOH lần lượt vào 4 mẫu thử.
- Mẫu thử xuất hiện khí có mùi khai → NH4Cl
NH4Cl + NaOH → NaCl + NH3 + H2O
- Xuất hiện kết tủa màu trắng, không tan trong NaOH dư → MgCl2
MgCl2 + NaOH → Mg(OH)2 + NaCl
- Xuất hiện kết tủa keo trắng, tan trong NaOH dư → AlCl3
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
Al(OH)3 + NaOH → NaAlO2 + 2H2O
- Không có hiện tượng gì → NaNO3
Câu 29:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Khi dùng NaOH:
+) NH4+ + OH- → NH3↑ + H2O (sủi bọt khí)
+) Mg2+ + 2OH- → Mg(OH)2 (kết tủa trắng)
+) Fe3+ + 3OH- → Fe(OH)3 (kết tủa vàng nâu)
+) Al3+ + 3OH- → Al(OH)3 (kết tủa keo trắng)
Al(OH)3 + OH- → AlO2- + 2H2O (kết tủa tan)
+) Na+: Không có hiện tượng.
Câu 30:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Muối của K cháy với ngọn lửa màu tím
Muối của Na cháy với ngọn lửa màu vàng
Muối của Ba cháy với ngọn lửa màu vàng lục
Muối của Ca cháy với ngọn lửa màu vàng cam
Có thể bạn quan tâm
- Trắc nghiệm Nhận biết một số ion trong dung dịch (có đáp án) (381 lượt thi)
- Trắc nghiệm Hóa 12 Bài 40 (có đáp án): Nhận biết một số ion trong dung dịch (215 lượt thi)
- Trắc nghiệm Nhận biết một số ion trong dung dịch có đáp án (Nhận biết) (254 lượt thi)
- Trắc nghiệm Nhận biết một số ion trong dung dịch có đáp án (Thông hiểu) (294 lượt thi)
- Trắc nghiệm Nhận biết một số ion trong dung dịch có đáp án (Vận dụng) (223 lượt thi)
Các bài thi hot trong chương
- Trắc nghiệm Luyện tập: Nhận biết một số chất vô cơ (có đáp án) (464 lượt thi)
- 40 câu trắc nghiệm Phân biệt một số chất vô cơ cơ bản (407 lượt thi)
- 40 câu trắc nghiệm Phân biệt một số chất vô cơ nâng cao (404 lượt thi)
- Trắc nghiệm Nhận biết một số chất khí (có đáp án) (394 lượt thi)
- 15 Câu trắc nghiệm luyện tập nhận biết một số chất vô cơ, chuẩn độ dung dịch có đáp án (276 lượt thi)
- Trắc nghiệm Luyện tập: Nhận biết một số chất vô cơ có đáp án (Nhận biết) (269 lượt thi)
- Trắc nghiệm Luyện tập: Nhận biết một số chất vô cơ có đáp án (Vận dụng) (262 lượt thi)
- Trắc nghiệm Luyện tập: Nhận biết một số chất vô cơ có đáp án (Thông hiểu) (254 lượt thi)
- Trắc nghiệm Nhận biết một số chất khí có đáp án (Thông hiểu) (243 lượt thi)
- Trắc nghiệm Nhận biết một số chất khí có đáp án (Nhận biết) (239 lượt thi)
