Giải KHTN 9 trang 78 Chân trời sáng tạo
Với giải bài tập Khoa học tự nhiên lớp 9 trang 78 trong Bài 17: Dãy hoạt động hoá học của kim loại. Một số phương pháp tách kim loại sách Chân trời sáng tạo hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập KHTN 9 trang 78.
Giải KHTN 9 trang 78 Chân trời sáng tạo
Trả lời:
Do kim loại sodium, potassium hoạt động mạnh, dễ dàng phản ứng với các tác nhân (oxygen, hơi nước …) có trong không khí. Do đó, để bảo quản cần ngâm chúng vào trong dầu hoả.
Trả lời:
- Học sinh tiến hành thí nghiệm theo các bước:
+ Bước 1: Cố định 3 ống nghiệm trên giá ống nghiệm, đánh số thứ tự 3 ống nghiệm.
+ Bước 2: Thêm vào lần lượt mỗi ống nghiệm 2 mL dung dịch HCl.
+ Bước 3: Cho vào ống nghiệm (1) một mảnh magnesium, ống nghiệm (2) một đinh sắt và ống nghiệm (3) một mảnh đồng phoi bào.
- Hiện tượng:
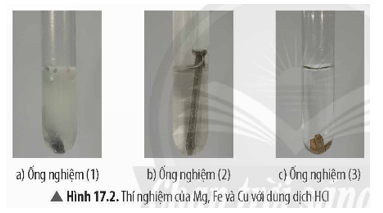
+ Ống nghiệm 1: Phản ứng xảy ra mãnh liệt. Mảnh Mg tan dần, có khí thoát ra mạnh.
+ Ống nghiệm 2: Có phản ứng xảy ra, phản ứng êm dịu hơn so với ở ống nghiệm 1. Đinh sắt tan dần, có khí thoát ra.
+ Ống nghiệm 3: Không có hiện tượng gì xuất hiện.
- Phương trình hoá học:
+ Ống nghiệm 1: Mg + 2HCl → MgCl2 + H2.
+ Ống nghiệm 2: Fe + 2HCl → FeCl2 + H2.
Câu hỏi thảo luận 4 trang 78 KHTN 9: Nhận xét mức độ hoạt động hoá học của kim loại Fe, Cu, Mg.
Mức độ hoạt động hoá học của các kim loại giảm dần theo thứ tự: Mg, Fe, Cu.
Khí hydrogen sinh ra khi kim loại phản ứng với dung dịch HCl.
Ví dụ: Cho kim loại Zn phản ứng với dung dịch HCl sinh ra muối chloride và giải phóng khí hydrogen.
Phương trình hoá học:
Zn + 2HCl → ZnCl2 + H2
Trả lời:
- Học sinh tiến hành thí nghiệm theo các bước sau:
+ Cố định 2 ống nghiệm trên giá để ống nghiệm, đánh số thứ tự 2 ống nghiệm.
+ Cho vào ống nghiệm (1) 2mL dung dịch ZnSO4 và ống nghiệm (2) 2 mL dung dịch AgNO3.
+ Nhúng vào mỗi ống nghiệm một đoạn dây đồng, quan sát hiện tượng.
- Hiện tượng:
+ Ống nghiệm 1: Không có hiện tượng gì xuất hiện.
+ Ống nghiệm 2: Có lớp kim loại trắng sáng bám ngoài dây đồng; dung dịch chuyển từ không màu sang màu xanh.
- Phương trình hoá học:
Cu + ZnSO4 → không phản ứng
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Câu hỏi thảo luận 6 trang 78 KHTN 9: Nhận xét mức độ hoạt động hoá học của kim loại Cu, Zn, Ag.
Trả lời:
+ Cu không phản ứng với ZnSO4 ⇒ Cu hoạt động hoá học kém hơn Zn.
+ Cu đẩy được Ag ra khỏi muối ⇒ Cu hoạt động hoá học mạnh hơn Ag.
Mức độ hoạt động hoá học của các kim loại giảm dần theo thứ tự: Zn, Cu, Ag.
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 9 Chân trời sáng tạo hay, chi tiết khác:
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 9 Chân trời sáng tạo hay, chi tiết khác:
Câu hỏi thảo luận 1 trang 77 KHTN 9: Kim loại sodium và magnesium phản ứng với nước có hiện tượng...
Câu hỏi thảo luận 2 trang 77 KHTN 9: Nhận xét mức độ hoạt động hoá học của kim loại Na và Mg....
Vận dụng trang 78 KHTN 9: Giải thích vì sao trong phòng thí nghiệm, kim loại sodium, potassium...
Câu hỏi thảo luận 3 trang 78 KHTN 9: Tiến hành Thí nghiệm 1 và nêu hiện tượng quan sát được...
Câu hỏi thảo luận 4 trang 78 KHTN 9: Nhận xét mức độ hoạt động hoá học của kim loại Fe, Cu, Mg....
Câu hỏi củng cố trang 78 KHTN 9: Khí nào sinh ra khi kim loại phản ứng với dung dịch HCl?...
Câu hỏi thảo luận 5 trang 78 KHTN 9: Tiến hành Thí nghiệm 2 và và nêu hiện tượng quan sát được....
Câu hỏi thảo luận 6 trang 78 KHTN 9: Nhận xét mức độ hoạt động hoá học của kim loại Cu, Zn, Ag....
Câu hỏi củng cố trang 79 KHTN 9: Hoàn thành phương trình hoá học của các phản ứng sau:...
Câu hỏi thảo luận 8 trang 80 KHTN 9: Người ta đã dùng phương pháp nào để tách Zn...
Vận dụng trang 80 KHTN 9: Hãy giải thích vì sao vàng, đồng, sắt được con người biết đến...
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 9 Chân trời sáng tạo hay, chi tiết khác:
Bài 16: Tính chất chung của kim loại
Xem thêm các chương trình khác:
- Soạn văn 9 Chân trời sáng tạo (hay nhất)
- Văn mẫu 9 - Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn 9 – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn 9 - Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn 9 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn 9 – Chân trời sáng tạo
- Soạn văn 9 Chân trời sáng tạo (ngắn nhất)
- Giải sgk Toán 9 – Chân trời sáng tạo
- Lý thuyết Toán 9 – Chân trời sáng tạo
- Giải sbt Toán 9 – Chân trời sáng tạo
- Giải sgk Tiếng Anh 9 - Friends plus
- Trọn bộ Từ vựng Tiếng Anh lớp 9 Friends plus đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 9 Friends plus đầy đủ nhất
- Giải sbt Tiếng Anh 9 – Friends plus
- Giải sgk Lịch sử 9 – Chân trời sáng tạo
- Giải sbt Lịch sử 9 – Chân trời sáng tạo
- Giải sgk Địa lí 9 – Chân trời sáng tạo
- Giải sbt Địa lí 9 – Chân trời sáng tạo
- Giải sgk Tin học 9 – Chân trời sáng tạo
- Giải sbt Tin học 9 – Chân trời sáng tạo
- Giải sgk Công nghệ 9 – Chân trời sáng tạo
- Giải sgk Giáo dục công dân 9 – Chân trời sáng tạo
- Giải sbt Giáo dục công dân 9 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 9 – Chân trời sáng tạo