Trắc nghiệm Kim loại kiềm thổ và hợp chất quan trọng của kim loại kiềm thổ (có đáp án)
Trắc nghiệm Bài 26: Kim loại kiềm thổ và hợp chất quan trọng của kim loại kiềm thổ
-
490 lượt thi
-
30 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Thạch cao nung (CaSO4.H2O) có khả năng kết dính tốt nên trong y học dùng để bó bột; trong xây dựng dùng để sản xuất xi măng chịu nước; đúc tượng, đúc các mẫu chi tiết tinh vi dùng trang trí nội thất; làm phấn viết.
Câu 2:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Tác hại của nước cứng:
- Đun tốn nhiệt, gây nổ nồi hơi.
- Tốn xà phòng, gây hư hại quần áo
- Giảm lưu lượng của đường ống dẫn nước.
- Giảm mùi vị của đồ ăn thức uống.
Nước cứng không gây ngộ độc khi uống.
Câu 3:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án D
A. Sai vì Trong nhóm IIA có Be và Mg không phản ứng với H2O ở nhiệt độ thường.
B. Sai vì cát (SiO2) có thể phản ứng với Mg ở nhiệt độ cao, do vậy dùng cát dập tắt sẽ làm đám cháy to hơn.
2Mg + SiO2 Si + 2MgO
C. Ca không thể đẩy Fe ra khỏi dung dịch muối vì Ca phản ứng với nước trong dung dịch.
Ca + 2H2O → Ca(OH)2 + H2
D. Đúng
Câu 4:
23/07/2024Phản ứng sản xuất vôi: CaCO3 (r) → CaO (r) + CO2 (k); ∆H > 0.
Biện pháp kĩ thuật tác động vào quá trình sản xuất vôi để tăng hiệu suất phản ứng là
 Xem đáp án
Xem đáp án
Đáp án B
Để làm câu hỏi này chú ý đến nguyên lí chuyển dịch cân bằng Lơ Sa-tơ-li-ê (Một phản ứng đang ở trạng thái cân bằng khi thay đổi các yếu tố nồng độ, nhiệt độ, áp suất, nhiệt độ thì cân bằng chuyển dịch theo hướng làm giảm tác động của các yếu tố đó)
Chiều thuận (∆H > 0): phản ứng thu nhiệt → tăng nhiệt độ cân bằng chuyển dịch theo chiều thuận
Giảm áp suất khí CO2 → Cân bằng chuyển dịch theo hướng tăng áp suất của hệ tức theo chiều thuận
Câu 5:
23/07/2024Cho các phát biểu sau:
Trong nhóm IIA của bảng tuần hoàn, đi từ Be đến Ba,
(1) bán kính nguyên tử tăng dần
(2) tính kim loại tăng dần.
(3) nhiệt độ nóng chảy giảm dần.
(4) nhiệt độ sôi giảm dần.
(5) khối lượng riêng thay đổi không theo quy luật
Trong các phát biểu trên, số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án B
Trong nhóm IIA của bảng tuần hoàn, đi từ trên xuống dưới theo chiều tăng điện tích hạt nhân bán kính nguyên tử tăng dần, tính kim loại của các nguyên tố mạnh dần đồng thời tính phi kim yếu dần.
Kim loại kiềm thổ không có cùng cấu tạo mạng tinh thể nên tính chất vật lí (nhiệt độ nóng chảy, nhiệt độ sôi, khối lượng riêng,...) biến đổi không có quy luật.
→ Các phát biểu đúng là (1), (2), (5)
Câu 6:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Chất X là MgCO3 có tên gọi là magie cacbonat.
MgCO3 là chất bột rắn, màu trắng, mịn, nhẹ có tác dụng hút ẩm rất tốt. Khi thi đấu, bàn tay của các vận động viên thường có nhiều mồ hôi, sẽ làm giảm độ ma sát khiến các vận động viên không thể nắm chắc các dụng cụ thi đấu. Điều này không chỉ ảnh hưởng xấu đến thành tích mà còn gây nguy hểm. MgCO3 có tác dụng thấm hút mồ hôi, đồng thời tăng cường độ ma sát giữa bàn tay các các dụng cụ thi đấu. Giúp các vận động viên thi đấu tốt hơn.
Câu 7:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Nước cứng tạm thời là nước cứng có chứa ion Ca2+, Mg2+,
Ca(OH)2 và Na2CO3 có khả năng làm mềm nước cứng tạm thời
Câu 8:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Phản ứng xảy ra khi hỗn hợp tác dụng với nước:
Na2O + H2O → 2NaOH
Các phản ứng xảy ra tiếp theo:
NH4Cl + NaOH → NH3↑ + H2O + NaCl
NaHCO3+ NaOH → Na2CO3 + H2O
Na2CO3 + BaCl2 → BaCO3↓ + 2NaCl
Vậy sau phản ứng dung dịch còn lại NaCl
Câu 9:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án D
= 0,02 mol;
nOH- = 0,03 mol;
= 0,012 mol
Ta có: T =
Vậy dung dịch sau phản ứng chứa (x mol) và (y mol)
Bảo toàn C có:
x + y = = 0,02 (1)
Bảo toàn số mol điện tích âm có:
2x + y = nOH- = 0,03 (2)
Từ (1) và (2) có x = y = 0,01 (mol)
Lại có:
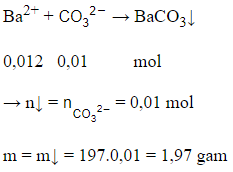
Câu 10:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Ca(HCO3)2 là chất lưỡng tính:
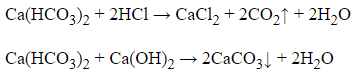
Vậy chất X là Ca(HCO3)2.
Câu 11:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Do là những kim loại hoạt động hóa học rất mạnh nên kim loại kiềm và kim loại kiềm thổ tồn tại ở dạng hợp chất trong tự nhiên.
Câu 12:
20/07/2024Từ hai muối X và Y thực hiện các phản ứng sau:
X → X1 + CO2
X1 + H2O → X2
X2 + Y → X + Y1 + H2O
X2 + 2Y → X + Y2 + H2O
Hai muối X, Y tương ứng là
 Xem đáp án
Xem đáp án
Đáp án C
Nhận thấy đáp án X đều là hợp chất muối cacbonat MCO3, X1 là MO.
X2 + H2O → X2.
Do đó X2 là M(OH)2 (loại D vì MgO không tan trong nước)
Để X2 + Y → X + Y2 + H2O và X2 + 2Y
→ X + Y2 + H2O thì chỉ có 1 trường hợp thỏa mãn là:
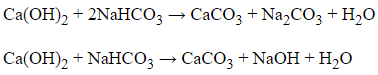
Câu 13:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Gọi công thức chung của hai kim loại là R.
Phương trình phản ứng:
R + 2HCl → RCl2 + H2
Bảo toàn nguyên tố:
nHCl = = 2 = 0,12 mol
mmuối = mkim loại +
= 1,76 + 0,12.35,5 = 6,02 gam.
Câu 14:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Đặt công thức chung 2 muối cacbonat là MCO3
Phản ứng:
MCO3 + H2SO4 → MSO4 + H2O + CO2
CO2 phản ứng với dung dịch Ba(OH)2
= 0,08 mol; = 0,09 mol
Dung dịch sau phản ứng có phản ứng kết tủa với nước vôi trong → trong dung dịch có muối axit
CO2 + Ba(OH)2 BaCO3 + H2O
2CO2 + Ba(OH)2 Ba(HCO3)2
Bảo toàn nguyên tố Ba:
→ = 0,09 – 0,08 = 0,01 mol
Bảo toàn nguyên tố C trong hai muối
→ = 0,08 + 2.0,01 = 0,1 mol
→ = = 0,1 mol
→ MM = 12 (g/mol)
→ Kim loại chắc chắn có mặt trong hỗn hợp có M < 12 là Be (MBe = 9 (g/mol))
Câu 15:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Bảo toàn electron:
2 = 2nMg
→ = nMg = 0,1 mol
V = 2,24 lít
Câu 16:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án B
= = 0,15 (mol),
= 0,4 (mol)
→ = 2,67
→ OH- dư, sản phẩm thu được là muối trung hòa
= 0,2.0,5 = 0,1 mol
→
Câu 17:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Đặt công thức chung của kim loại và oxit là MOx (0 < x < 1) với số mol là a
Sơ đồ phản ứng:
MOx MCl2 + H2O + H2
mhh = a(M + 16x) = 0,88 (1)
và mmuối = a(M + 71) = 2,85 (2)
Chia từng vế của (1) cho (2) ta được:
=
→ 1,97M = 62,48 – 45,6x
Vì 0 < x < 1 nên 8,7 < M < 31,7
Vậy M là Be hoặc Mg
Dựa trên 4 đáp án đề bài cho → chọn B.
Câu 18:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án A
CaCO3 CaO + CO2↑
Giả sử số mol CaCO3 trong hỗn hợp đầu là 1 mol
→ = = 1 mol
→ mtrước – msau =
= mtrước – 2/3mtrước
→ mtrước = 3.
= 3.1.44 = 132g
→ % =
= 75,76%
Câu 19:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Kim loại kiềm thổ chỉ được điều chế bằng phương pháp điện phân nóng chảy muối halogenua
MgCl2 Mg + Cl2
Câu 20:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Chỉ có kim loại kiềm và kiềm thổ (trừ Be và Mg) phản ứng với H2O ở điều kiện thường.
→ Các kim loại đề bài có Na, K, Ba và Ca thỏa mãn
→ Có 4 kim loại thỏa mãn
Câu 21:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Gọi số mol NaOH và Ba(OH)2 trong 50 ml dung dịch X lần lượt là x và y (mol)
= x + 2y (mol);
= y (mol)
Phản ứng trung hoà:
=
→ x + 2y = 0,1.0,1 = 0,01 mol
Phản ứng với CO2:
= 8.10-3 mol
= 1,25
→ Hai chất tham gia phản ứng hết, phản ứng tạo 2 muối
= 0,01 – 8.10-3 = 2.10-3 mol
= 0,2955 : 197
= 1,5.10-3 mol >
→ Toàn bộ Ba2+ đã đi vào kết tủa
=
= 1,5.10-3 mol
→ b = = 0,03 (mol/l)
nNaOH = - 2
= 0,01 - 2.1,5.10-3 = 7.10-3 mol
→ a = = 0,14 (mol/l)
Câu 22:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Khi kết tủa lớn nhất: toàn bộ ion HCO3-, CO32-, SO42- đã chuyển hoá và đi vào kết tủa
Dung dịch còn lại NaOH
→ = a + b
→ 2.0,1.f = a + b
→
Câu 23:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Phương trình phản ứng
Ca(OH)2 + Ca(HCO3)2 → 2CaCO3 + 2H2O
Câu 24:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Kim loại kiềm thổ thuộc nhó IIA của bảng tuần hoàn nguyên tố hóa học.
Nguyên tử các nguyên tố nhóm IIA đều có 2 electron lớp ngoài cùng và có cấu hình electron chung là ns2 (n là số lớp electron)
Câu 25:
15/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Thành phần chính của đá vôi là CaCO3 có tên gọi là canxi cacbonat. CaCO3 là chất rắn ở điều kiện thường, không tan trong nước, có màu trắng
Câu 26:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Lớp cặn trong cặn ấm đun nước thường là CaCO3 (có thể do nước sử dụng là nước cứng tạm thời, toàn phần,...). Dùng giấm ăn (có chứa axit yếu là axit axetic CH3COOH) để hòa tan cặn
2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2 + H2O
Câu 27:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Áp dụng định luật bảo toàn điện tích
→
→ 2a + 2b = c + d
Câu 28:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án C
3m gam X tác dụng hết với dung dịch Ba(OH)2 dư, thu được 3,9 mol khí
→ m gam X tác dụng hết với dung dịch Ba(OH)2 dư, thu được 1,3 lít khí
Gọi x = nBa
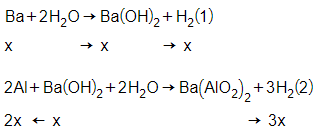
Do tác dụng với nước chỉ thu được 1 mol H2 mà tác dụng với dung dịch Ba(OH)2 dư lại tạo ra 1,3 mol H2 nên sau khi cho hỗn hợp X tác dụng với H2O thì Al vẫn còn dư tạo ra thêm 0,3 mol H2
Theo phương trình (1) và (2) ta có:
= x + 3x = 1
→ x = 0,25
→ m = mBa + mAl pư + mAl còn dư
= 137.x + 27.2x + 27.0,2 = 53,15g
Câu 29:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án D
= 0,04 mol
Gọi R là kí hiệu chung của Na và Ba, hóa trị của chúng là x.
2R + 2xH2O 2R(OH)x + xH2↑
= 2 = 0,08 mol
→ pOH = –lg[OH-]
= –lg(0,08/0,8) = 1
→ pH = 13
Câu 30:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Phản ứng Ca(HCO3)2 → CaCO3 + CO2 + H2O giải thích sự tạo thành thạch nhũ trong các hang động đá vôi, cặn trong ấm đun nước,..
Phản ứng CaCO3 + CO2 + H2O → Ca(HCO3)2 giải thích sự xâm thực đá vôi của nước mưa.
Có thể bạn quan tâm
- Trắc nghiệm Kim loại kiềm thổ và hợp chất quan trọng của kim loại kiềm thổ (có đáp án) (489 lượt thi)
- 15 Câu trắc nghiệm kim loại kiềm thổ và hợp chất quan trọng của kim loại kiềm thổ có đáp án (209 lượt thi)
- Trắc nghiệm Kim loại kiềm thổ có đáp án (Nhận biết) (308 lượt thi)
- Trắc nghiệm Kim loại kiềm thổ có đáp án (Thông hiểu) (240 lượt thi)
- Trắc nghiệm Kim loại kiềm thổ có đáp án (Vận dụng) (251 lượt thi)
Các bài thi hot trong chương
- Trắc nghiệm Kim loại kiềm và hợp chất của kim loại kiềm (có đáp án) (1191 lượt thi)
- 100 câu trắc nghiệm Kim loại kiềm, Kim loại kiềm thổ, Nhôm cơ bản (958 lượt thi)
- 100 câu trắc nghiệm Kim loại kiềm, Kiềm thổ, Nhôm nâng cao (909 lượt thi)
- Trắc nghiệm Luyện tập tính chất của nhôm và hợp chất của nhôm (có đáp án) (583 lượt thi)
- Trắc nghiệm Nhôm và hợp chất của nhôm (có đáp án) (512 lượt thi)
- Trắc nghiệm Luyện tập: Tính chất của kim loại kiềm, kiềm thổ và hợp chất của chúng (Thông hiểu) (331 lượt thi)
- Trắc nghiệm Nhôm và hợp chất của nhôm có đáp án (Nhận biết) (327 lượt thi)
- Trắc nghiệm Nhôm và hợp chất của nhôm có đáp án (Vận dụng) (309 lượt thi)
- Trắc nghiệm Kim loại kiềm và hợp chất quan trọng của kim loại kiềm có đáp án (Nhận biết) (306 lượt thi)
- Trắc nghiệm Luyện tập tính chất của kim loại kiềm, kiềm thổ và hợp chất của chúng (có đáp án) (298 lượt thi)
