Đề thi Học kì 2 Hóa 10 cực hay có đáp án
Đề thi Học kì 2 Hóa 10 cực hay có đáp án (Đề 6)
-
826 lượt thi
-
7 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
16/07/2024Viết các phương trình thực hiện chuỗi biến hóa sau (ghi rõ điều kiện nếu có).
FeSH2S S SO2SO3H2SO4SO2
 Xem đáp án
Xem đáp án
(1) FeS + 2HCl → FeCl2+ H2S↑
(2) 2H2S + SO2→ 3S↓ + 2H2O
(3) S + O2SO2
(4) 2SO2+ O22SO3
(5) SO3+ H2O → H2SO4
(6) 2H2SO4+ S → 3SO2+ 2H2O
Câu 2:
19/07/2024Bằng phương pháp hóa học hãy phân biệt các khí bị mất nhãn không màu sau: H2S, HCl, O2, N2
 Xem đáp án
Xem đáp án
- Cho lần lượt từng khí tác dụng với dung dịch CuCl2.
+ Xuất hiện kết tủa đen là H2S
H2S + CuCl2 → CuS↓ + 2HCl
+ Không hiện tượng là HCl, O2, N2 (1)
- Cho quỳ tím ẩm vào các mẫu thử nhóm (1)
+ Qùy tím hóa đỏ là HCl
+ Không đổi màu là O2, N2 (2)
- Cho que đóm còn tàn đỏ vào các mẫu còn lại nhóm (2)
+ Nếu que đóm bùng cháy là O2
C + O2 CO2
+ Nếu que đóm tắt là N2
Câu 3:
13/07/2024Tiến hành thí nghiệm như hình vẽ:
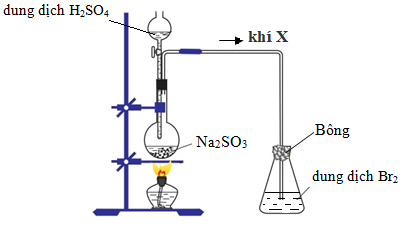
a. Hãy xác định khí X. Viết phương trình phản ứng xảy ra trong bình cầu.
b. Hãy cho biết hiện tượng xảy ra ở bình tam giác. Viết phương trình phản ứng minh họa.
 Xem đáp án
Xem đáp án
a. Khí X: SO2
Phương trình hóa học xảy ra trong bình cầu:
Na2SO3+ H2SO4Na2SO4+ SO2↑ + H2O
b. Hiện tượng xảy ra ở bình tam giác: dd brom bị mất màu.
Phương trình hóa học minh họa:
SO2+ Br2+ 2H2O → H2SO4+ 2HBr
Câu 4:
17/07/2024Cho các chất sau: H2, SO2, H2S, O2, NH3, CO2, N2, O3. Biết rằng:
- Khí A không có mùi, có vai trò quyết định sự sống của con người và động vật.
- Khí B tập trung nhiều ở lớp khí quyển cao, hấp thụ tia tử ngoại.
- Khí C có mùi trứng thối và bốc ra từ xác chết của người và động vật.
- Khi bầu đựng thủy ngân của một nhiệt kế bị vỡ, ta cần dùng bột D rắc lên thủy ngân rồi gom lại.
Hãy xác định công thức phân tử của các chất A, B, C, D nói trên.
 Xem đáp án
Xem đáp án
- Khí O2không có mùi, có vai trò quyết định sự sống của con người và động vật.
- Khí O3tập trung nhiều ở lớp khí quyển cao, hấp thụ tia tử ngoại.
- Khí H2S có mùi trứng thối và bốc ra từ xác chết của người và động vật.
- Khi bầu đựng thủy ngân của một nhiệt kế bị vỡ, ta cần dùng bột S rắc lên thủy ngân rồi gom lại.
Vậy A, B, C, D lần lượt là O2; O3; H2S; S
Câu 5:
07/07/2024Hòa tan hoàn toàn 10 gam hỗn hợp gồm Cu và Mg vào dung dịch H2SO4đặc nóng dư thu được 5,6 lít khí SO2(đktc) (là sản phẩm khử duy nhất) và dung dịch X.
a. Tính khối lượng mỗi muối trong dung dịch X.
b. Dẫn 5,6 lít khí SO2 (đktc) ở trên vào 500ml dung dịch KOH 1,25M, phản ứng xảy ra hoàn toàn thu được dung dịch Y. Tính nồng độ mol của các chất trong dung dịch Y. Giả sử thể tích dung dịch thay đổi không đáng kể. Xem đáp án
Xem đáp án
a. Có \({n_{S{O_2}}} = \frac{{5,6}}{{22,4}} = 0,25\)mol
Gọi số mol của Cu và Mg lần lượt là x và y (mol)
Suy ra 64x + 24y = 10 (1)
Phương trình hóa học:
Suy ra x + y = 0,25 (2)
Từ (1) và (2) suy ra x = 0,1, y = 0,15
Vậy \({m_{CuS{O_4}}}\)= 0,1.160 = 16 gam, \({m_{MgS{O_4}}}\)= 0,15.120 = 18 gam
b. Ta có: nKOH= 0,5.1,25 = 0,625 mol
Xét \(T = \frac{{{n_{KOH}}}}{{{n_{S{O_2}}}}} = \frac{{0,625}}{{0,25}} = 2,5 >2\)
Suy ra dung dịch X chứa K2SO3và KOH dư
Phương trình phản ứng:
Suy ra \({C_{M({K_2}S{O_3})}} = \frac{{0,25}}{{0,5}}\)= 0,5M
Có nKOHdư = 0,625 – 0,5 = 0,125 mol
Suy ra \({C_{M(KOH)}} = \frac{{0,125}}{{0,5}}\)= 0,25M
Câu 6:
03/07/2024a. Than tổ ong là nhiên liệu được người dân sử dụng rộng rãi. Hãy giải thích tại sao:
- Các viên than khi được sản xuất đều có các lỗ rỗng như hình bên.
- Trong quá trình sử dụng muốn giảm nhiệt độ của than hay kéo dài thời gian, người ta thường khép bớt cửa bếp lại.
b. Sữa chua là một thực phẩm bổ dưỡng, dễ ăn. Để làm được sữa chua, chỉ cần cho sữa tươi và sữa đặc vào cùng một cái nồi, quấy đều tay cho đến khi hỗn hợp sôi. Sau đó tắt bếp, để hỗn hợp nguội bớt rồi hòa cùng với hũ sữa chua cái. Rót vào hũ rồi đem hỗn hợp sữa ấm đi ủ trong khoảng 8-10 tiếng. Hãy cho biết vai trò của hũ sữa chua cái trong quy trình trên.

 Xem đáp án
Xem đáp án
a) - Lỗ rỗng của viên than tổ ong có tác dụng tăng diện tích tiếp xúc giữa than và oxi không khí
- Trong quá trình sử dụng muốn giảm nhiệt độ của than hay kéo dài thời gian, người ta thường khép bớt cửa lò lại để giảm bớt nồng độ oxi không khí.
b) Hũ sữa chua cái trong quy trình trên đóng vai trò làm chất xúc tác.
Câu 7:
05/07/2024Cho 47,04 lít SO3(đktc) hấp thụ hết vào 90 gam dung dịch H2SO498%, thu được oleum có công thức H2SO4.nSO3. Hãy xác định công thức của oleum.
 Xem đáp án
Xem đáp án
Có \({n_{S{O_3}}} = \frac{{47,04}}{{22,4}}\)= 2,1 mol
90g dung dịch H2SO498% có:
\({m_{{H_2}S{O_4}}}\)= \[\frac{{90.98}}{{100}}\] = 88,2g → \({n_{{H_2}S{O_4}}}\)= 0,9mol
\({m_{{H_2}O}}\)= 90 - 88,2 = 1,8g → \({n_{{H_2}O}}\) = 0,1mol
Phương trình hóa học:
Ta thấy: \({n_{{H_2}S{O_4}}}:{n_{S{O_3}}} = 1:2\) suy ra n = 2.
Vậy công thức của oleum là: H2SO4.2SO3
Bài thi liên quan
-
Đề thi Học kì 2 Hóa 10 cực hay có đáp án (Đề 1)
-
20 câu hỏi
-
50 phút
-
-
Đề thi Học kì 2 Hóa 10 cực hay có đáp án (Đề 2)
-
23 câu hỏi
-
50 phút
-
-
Đề thi Học kì 2 Hóa 10 cực hay có đáp án (Đề 3)
-
19 câu hỏi
-
50 phút
-
-
Đề thi Học kì 2 Hóa 10 cực hay có đáp án (Đề 4)
-
19 câu hỏi
-
50 phút
-
-
Đề thi Học kì 2 Hóa 10 cực hay có đáp án (Đề 5)
-
40 câu hỏi
-
50 phút
-
-
Đề thi Học kì 2 Hóa 10 cực hay có đáp án (Đề 7)
-
10 câu hỏi
-
90 phút
-
Có thể bạn quan tâm
- Đề thi Học kì 2 Hóa 10 cực hay có đáp án (825 lượt thi)
- Đề thi giữa kì 2 Hóa 10 cực hay có đáp án (395 lượt thi)
- Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (3252 lượt thi)
- Đề kiểm tra 15p Hóa 10 Học kì 2 (Bài số 1) (609 lượt thi)
- Đề kiểm tra 15 phút - Trắc nghiệm + Tự luận (674 lượt thi)
- Đề thi giữa kì 2 Hóa 10 (Bài số 1) (864 lượt thi)
- Đề kiểm tra 15p Hóa 10 Học kì 2 (Bài số 2) (1270 lượt thi)
- Đề thi giữa kì 2 Hóa 10 (Bài số 2) (685 lượt thi)
- Đề thi Hóa 10 Học kì 2 (Bài kiểm tra học kì) (654 lượt thi)
Các bài thi hot trong chương
- Đề kiểm tra 15 phút Hóa học 10 Học kì 1 có đáp án (Bài số 1) (2600 lượt thi)
- Đề thi giữa kì 1 Hóa học 10 có đáp án (Bài số 1) (757 lượt thi)
- Đề thi giữa kì 1 Hóa học 10 có đáp án (Bài số 2) (733 lượt thi)
- Đề kiểm tra 15 phút Hóa 10 Học kì 1 có đáp án (Bài số 2 - Đề 1) (618 lượt thi)
- Đề thi Hóa 10 Học kì 1 (554 lượt thi)
- Đề thi Hóa học 10 Giữa học kì 1 năm 2020 - 2021 có đáp án (501 lượt thi)
- Đề thi Hóa học 10 Giữa học kì 1 biên soạn (446 lượt thi)
- Đề thi Học kì 1 Hóa 10 có đáp án (328 lượt thi)
- Đề thi giữa kì 1 Hóa 10 cực hay có đáp án (Bài kiểm tra số 2) (306 lượt thi)
