Đề thi học kì 1 Hóa học 9 có đáp án ( đề 10 )
-
1989 lượt thi
-
19 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
23/07/2024Cho sơ đồ phản ứng:
X+HCl→Y+H2OY+NaOH→ZK+NaClZ+HCl→Y+H2O
X là chất nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Fe2O3+6HCl→2FeCl3+3H2OFeCl3+3NaOH→Fe(OH)3+3NaClFe(OH)3+3HCl→FeCl3+3H2O
Câu 2:
23/07/2024Cặp chất nào dưới đây không xảy ra phản ứng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Ag đứng sau Cu trong dãy hoạt động hóa học của kim loại nên không đẩy Cu ra khỏi dung dịch muối.
Câu 3:
23/07/2024Cho các phân bón: KNO3, NH4Cl, (NH4)2SO4, CaHPO4, (NH4)2HPO4. Số phân bón kép là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Phân bón kép là phân bón chứa hai hoặc cả ba nguyên tố dinh dưỡng N, P, K: KNO3, (NH4)2HPO4.
Câu 4:
23/07/2024Phản ứng nào sau đây không phải là phản ứng trao đổi?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Phản ứng Mg+FeCl3→MgCl2+Fe là phản ứng thế
Câu 5:
23/07/2024Có một hỗn hợp gồm oxit nhôm và oxit sắt, có thể tách được oxit sắt khỏi hỗn hợp bằng cách cho hỗn hợp tác dụng với lượng dư dung dịch
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Oxit nhôm Al2O3 là oxit lưỡng tính nên tác dụng với dung dịch kiềm, còn oxit của sắt là oxit bazơ nên không phản ứng với dung dịch kiềm. Do đó ta thu được chất rắn còn lại sau phản ứng là oxit sắt.
Al2O3+2NaOH+3H2O→2Na[Al(OH)4]
Câu 6:
23/07/2024Kim loại X có những tính chất sau:
- Phản ứng với oxi khi nung nóng
- Khi tác dụng với khí clo và axit clohiđric đều cho cùng một muối
- Phản ứng với dung dịch Cu(NO3)2 giải phóng Cu
X có thể là kim loại nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
2Zn+O2to→2ZnOZn+Cl2to→ZnCl2Zn+2HCl→ZnCl2+H2↑Zn+Cu(NO3)2→Zn(NO3)2+Cu
Câu 7:
23/07/2024Cho từ từ dung dịch NaOH vào dung dịch CuCl2 lọc lấy kết tủa đem nung trong không khí đến khối lượng không đổi. Chất rắn thu được là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
2NaOH+CuCl2→2NaCl+Cu(OH)2↓Cu(OH)2to→CuO+H2O
Câu 8:
23/07/2024Chọn câu đúng nhất khi nói đến tính chất hóa học của kim loại
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Đối với hầu hết các kim loại lưu huỳnh sẽ tác dụng ở nhiệt độ cao tạo muối sunfua, trừ kim loại Hg có thể tác dụng với lưu huỳnh ở nhiệt độ thường.
Fe+Sto→FeSHg+S→HgS
Câu 9:
23/07/2024Cho axit sunfuric đặc, dư tác dụng với 10 g hỗn hợp Cu và CuO thì thu được 2,24 lít khí (đktc). Khối lượng (gam) của CuO và Cu trong hỗn hợp lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Kim loại đồng tác dụng với dung dịch H2SO4 đặc nóng tạo khí SO2, CuO cũng tác dụng được với H2SO4 nhưng không sinh ra khí.
2H2SO4+Cuto→CuSO4+SO2+2H2OH2SO4+CuO→CuSO4+H2O
Số mol SO2 là: nSO2=VSO222,4=2,2422,4=0,1(mol)
Từ phương trình ⇒nCu=nSO2=0,1(mol)
Khối lượng của mỗi chất trong hỗn hợp ban đầu là:
mCu=nCu.MCu=0,1.64=6,4(g)mCuO=10−mCu=10−6,4=3,6(g)
Câu 10:
23/07/2024Đốt photpho đỏ trong bình có chứa một ít nước. Sau khi đốt xong lắc để bình một lúc, thả quỳ tím vào dung dịch thì quỳ tím chuyển màu như thế nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Đốt photpho trong oxi ta thu được điphotpho pentaoxit dưới dạng khói trắng:
4P+5O2to→2P2O5
Lắc bình cho khói trắng tan vào nước ta thu được axit photphoric, axit này làm quỳ tím hóa đỏ: P2O5+3H2O→2H3PO4
Câu 11:
23/07/2024Một oxit sắt có khối lượng mol là 160. Thành phần phần trăm về khối lượng của các nguyên tố trong oxit sắt là: sắt 70% và oxi 30%. Công thức phân tử của oxit là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Khối lượng của mỗi nguyên tố có trong 1 mol phân tử oxit là:
mFe = 160.70% = 112 (g)
mO = 160.30% = 48 (g)
Số mol của mỗi nguyên tử có trong một mol phân tử oxit là:
nFe=mFeMFe=11256=2(mol)nO=mOMO=4816=3(mol)
Vậy công thức hóa học của oxit là Fe2O3
Câu 12:
23/07/2024Cho dãy các oxit sau: CuO, Fe2O3, Al2O3, MgO, Ag2O, Na2O, CaO, PbO. Cho khí CO nóng đi qua các oxit đó thì có thể thu được những kim loại nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
CO có thể khử oxit của các kim loại đứng sau nhôm trong dãy hoạt động hóa học của kim loại thành kim loại
CO+CuOto→Cu+CO2CO+Fe2O3to→2Fe+3CO2CO+Ag2Oto→2Ag+CO2CO+PbOto→Pb+CO2
Câu 13:
23/07/2024Cho các chất sau: Fe2(SO4)3, Cu(OH)2, BaCl2, Ag, C, NaHCO3. Số chất tác dụng được với dung dịch H2SO4 đặc nóng là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Cu(OH)2+H2SO4→CuSO4+2H2OBaCl2+H2SO4→BaSO4↓+2HCl2Ag+2H2SO4(dac)to→Ag2SO4+SO2+2H2OC+2H2SO4(dac)to→CO2+2SO2+2H2O2NaHCO3+H2SO4→Na2SO4+2H2O+2CO2↑
Câu 14:
23/07/2024Sắt cháy trong khí clo tạo thành
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Sắt cháy trong khí clo tạo các tinh thể muối sắt (III) clorua màu nâu đỏ khuếch tán trong không khí dưới dạng khói.
2Fe+3Cl2to→2FeCl3
Câu 15:
23/07/2024Khí X được điều chế bằng cách cho axit phản ứng với kim loại hoặc muối và được thu vào ống nghiệm theo cách sau:
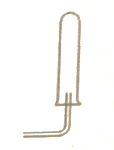
Khí X được điều chế bằng phản ứng nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Từ hình vẽ ta thấy khí X thu được bằng cách đẩy không khí và bình thu úp ngược nên khí X nhẹ hơn không khí, do đó đáp án đúng là thu khí hiđro.
Câu 16:
23/07/2024Hoàn thành sơ đồ chuyển hóa hóa học và viết các phương trình phản ứng:
A+HCl→B+NaOH→Cto→A+H2,to→Cu
 Xem đáp án
Xem đáp án
Các chất A, B, C lần lượt là CuO, CuCl2. Cu(OH)2
Các phương trình hóa học xảy ra:
CuO+2HCl→CuCl2+H2OCuCl2+2NaOH→Cu(OH)2+2NaClCu(OH)2to→CuO+H2OCuO+H2to→Cu+H2O
Câu 17:
23/07/2024Từ các chất KCl, MnO2, H2SO4 đặc. Hãy viết phương trình phản ứng điều chế khí clo.
 Xem đáp án
Xem đáp án
- Điều chế axit clohiđric từ KCl và H2SO4 đặc.
2KCl+H2SO4to→K2SO4+2HCl↑
Khí hido clorua thu được ở dạng khí hòa tan vào nước thu được dung dịch axit clohiđric
- Điều chế khí clo từ axit clohiđric HCl đặc và MnO2
MnO2+4HClto→MnCl2+Cl2↑+2H2O
Câu 18:
23/07/2024Ngâm một lá nhôm trong dung dịch đồng (II) sunfat màu xanh lam, sau một thời gian ta thấy dung dịch màu xanh nhạt dần và trên lá nhôm có bám bột màu đỏ. Giải thích hiện tượng và viết phương trình hóa học xảy ra.
 Xem đáp án
Xem đáp án
Kim loại nhôm đứng trước đồng trong dãy hoạt động hóa học của kim loại nên có thể đẩy đồng khỏi dung dịch muối, tạo thành muối nhôm sunfat và đồng. Vì muối nhôm sunfat sinh ra trong suốt không màu nên màu xanh của dung dịch đồng (II) sunfat nhạt dần, kim loại đồng sinh ra bám trên lá nhôm dưới dạng bột màu đỏ.
Câu 19:
23/07/2024Hòa tan hoàn toàn 24 gam hỗn hợp Al và Mg bằng dung dịch HCl 2M vừa đủ. Thêm một lượng NaOH dư vào dung dịch. Sau phản ứng xuất hiện một lượng kết tủa. Lọc lấy kết tủa rửa sạch rồi nung ở nhiệt độ cao cho đến khối lượng không đổi thu được 4g chất rắn.
a) Tính khối lượng của mỗi kim loại có trong hỗn hợp ban đầu.
b) Tính thể tích dung dịch HCl đã dùng
 Xem đáp án
Xem đáp án
Các phương trình hóa học xảy ra:
- Kim loại tác dụng với axit clohiđric
2Al+6HCl→2AlCl3+3H2↑(1) 2 60,8
- Dung dịch muối tác dụng với dung dịch NaOH
- Dung dịch NaOH tiếp tục hòa tan Al(OH)3
- Kết tủa còn lại là Mg(OH)2 đem nung đến khối lượng không đổi.
a) Khối lượng chất rắn MgO thu được là:
Áp dụng định luật bảo toàn nguyên tố cho nguyên tố Mg, ta có:
Khối lượng mỗi kim loại có trong hỗn hợp là:
mMg = nMg . MMg = 0,1.24 = 2,4 (g)
mAl = 24 – mMg = 24 – 2,4 = 21,6 (g)
b) Số mol Al là:
Từ phương trình (1) và (2), số mol của HCl đã phản ứng là:
Thể tích dung dịch HCl 2M đã dùng là:
(lít)
Bài thi liên quan
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 1 )
-
19 câu hỏi
-
45 phút
-
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 2 )
-
19 câu hỏi
-
45 phút
-
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 3 )
-
19 câu hỏi
-
45 phút
-
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 4 )
-
19 câu hỏi
-
45 phút
-
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 5 )
-
19 câu hỏi
-
45 phút
-
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 6 )
-
19 câu hỏi
-
45 phút
-
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 7 )
-
19 câu hỏi
-
45 phút
-
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 8 )
-
19 câu hỏi
-
45 phút
-
-
Đề thi học kì 1 Hóa học 9 có đáp án ( đề 9 )
-
19 câu hỏi
-
45 phút
-
