Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề)
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 14)
-
5325 lượt thi
-
40 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 3:
19/07/2024Trong công nghiệp, phương pháp nhiệt luyện được sử dụng để điều chế kim loại nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D
Câu 4:
21/07/2024Cho dãy kim loại sau: Na, Mg, Fe, Cu. Kim loại có tính khử yếu nhất trong dãy là
 Xem đáp án
Xem đáp án
Chọn A
Câu 6:
19/07/2024Chất nào sau đây tác dụng được với dung dịch HCl sinh ra muối và khí H2?
 Xem đáp án
Xem đáp án
Chọn C
Câu 12:
19/07/2024Cacbon(II) oxit là một loại khí độc, gây ra nhiều vụ ngạt khí do sự chưa cháy hết của nhiên liệu hóa thạch. Công thức của cacbon(II) oxit là
 Xem đáp án
Xem đáp án
Chọn D
Câu 14:
14/11/2024Trong cơ thể người, chất béo bị oxi hóa chậm thành
 Xem đáp án
Xem đáp án
Đáp án đúng là : A
- Trong cơ thể người, chất béo bị oxi hóa chậm thành H2O và CO2.
Chất béo được cấu tạo từ 3 nguyên tố: C, H, O.
Chất béo được cấu tạo từ 3 nguyên tố: C, H, O ⟹ bị oxi hóa chậm thành CO2, H2O.
Chất béo không chứa N ⟹ loại A, B, D vì có NH3, N2.
→ A đúng.B,C,D sai.
* Chất béo
1. Khái niệm
- Chất béo là trieste của glixerol với axit béo, gọi chung là triglixerit hay triaxylglixerol.
- Chú ý: Axit béo là axit đơn chức, có mạch cacbon dài, không phân nhánh. Các axit béo
thường có trong chất béo:
+ Axit panmitic: C15H31COOH
+ Axit stearic: C17H35COOH
+ Axit oleic: C17H33COOH
+ Axit linoleic: C17H31COOH
+ Axit linolenoic: C17H29COOH
- Công thức cấu tạo chung của chất béo:
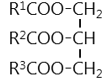 hoặc
hoặc 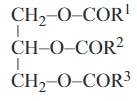
(Trong đó R1; R2; R3 là gốc hiđrocacbon, có thể giống hoặc khác nhau).
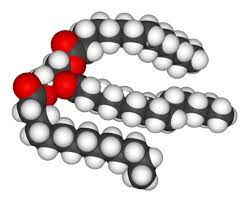
Hình 1: Mô hình phân tử chất béo
- Một số chất béo thường gặp:
+ Tripanmitin: (C15H31COO)3C3H5
+ Tristearin: (C17H35COO)3C3H5
+ Triolein: (C17H33COO)3C3H5
+ Trilinolein: (C17H31COO)3C3H5
+ Trilinolenin: (C17H29COO)3C3H5
- Mỡ động vật (bò, lợn, gà …), dầu thực vật (dầu lạc, dầu cọ, dầu oliu …) có thành phần chính là chất béo.
2. Tính chất vật lý
- Ở nhiệt độ thường, chất béo ở trạng thái lỏng hoặc rắn.
+ Các chất béo chứa chủ yếu các gốc axit béo no thường là chất rắn ở nhiệt độ phòng, như mỡ động vật.
+ Các chất béo chứa chủ yếu các gốc axit béo không no thường là chất lỏng ở nhiệt độ phòng và được gọi là dầu, thường có nguồn gốc thực vật hoặc từ động vật máu lạnh như dầu cá…
- Chất béo nhẹ hơn nước và không tan trong nước, tan trong các dung môi hữu cơ không phân cực như benzen, xăng, ete…
3. Tính chất hóa học
Về cấu tạo, chất béo là trieste nên có tính chất của este nói chung như: tham gia phản ứng thủy phân trong môi trường axit, phản ứng xà phòng hóa và phản ứng ở gốc hiđrocacbon.
a. Phản ứng thủy phân trong môi trường axit
- Khi đun nóng chất béo với nước có xúc tác axit, chất béo bị thủy phân tạo ra glixerol và các axit béo:
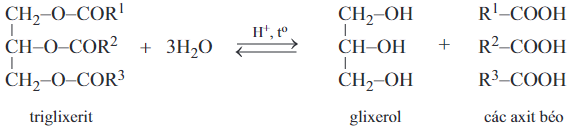
b. Phản ứng xà phòng hóa
- Khi đun nóng chất béo với dung dịch kiềm (NaOH hoặc KOH) thì tạo ra glixerol và hỗn hợp muối của các axit béo. Muối natri hoặc kali của các axit béo chính là xà phòng.
- Tổng quát:
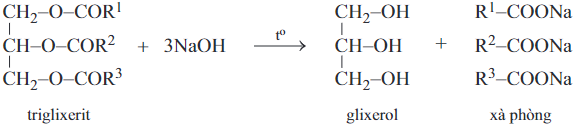
- Ví dụ:
(C15H31COO)3C3H5 + 3NaOH C3H5(OH)3 + 3C15H31COONa
- Phản ứng của chất béo với dung dịch kiềm được gọi là phản ứng xà phòng hóa. Phản ứng xà phòng hóa xảy ra nhanh hơn phản ứng thủy phân trong môi trường axit và không thuận nghịch.
- Mở rộng:
+ Chỉ số xà phòng hóa: là số mg KOH để trung hòa hết lượng axit tự do và xà phòng hóa hết lượng este trong 1 gam chất béo.
+ Chỉ số axit: số mg KOH dùng để trung hòa axit tự do có trong 1 gam chất béo.
c. Phản ứng cộng H2 của chất béo lỏng
- Chất béo có chứa các gốc axit béo không no tác dụng với hiđro ở nhiệt độ và áp suất cao
có Ni xúc tác. Khi đó hiđro cộng vào nối đôi C = C. Ví dụ:
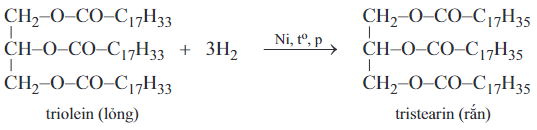
- Phản ứng này được dùng trong công nghiệp để chuyển hóa chất béo lỏng (dầu) thành mỡ rắn thuận tiện cho việc vận chuyển hoặc thành bơ nhân tạo và để sản xuất xà phòng.
d. Phản ứng oxi hóa
Nối đôi C = C ở gốc axit không no của chất béo bị oxi hóa chậm bởi oxi không khí tạo thành peoxit, chất này bị phân hủy thành các sản phẩm có mùi khó chịu. Đó là nguyên nhân của hiện tượng dầu mỡ để lâu bị ôi.
Xem thêm các bài viết liên quan,chi tiết khác:
Câu 19:
19/07/2024Phân bón nào sau đây không cung cấp nguyên tố ntiơ cho cây trồng và đất trồng?
 Xem đáp án
Xem đáp án
Chọn B
Câu 21:
19/07/2024Hỗn hợp X gồm hai chất có tỉ lệ mol 1 : 1. Cho X tác dụng với dung dịch H2SO4 loãng (vừa đủ), thu được dung dịch có chứa hai muối sắt có số mol bằng nhau. X là hỗn hợp nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D
Câu 22:
19/07/2024Thủy tinh hữu cơ (hay thủy tinh plexiglas) là một vật liệu quan trọng, được sử dụng làm kính lúp, thấu kính, kính chống đạn,..Thủy tinh hữu cơ được tổng hợp từ phản ứng trùng hợp chất nào sau đây?
 Xem đáp án
Xem đáp án
Chọn B
Câu 23:
19/07/2024Cho 6,4 gam Cu vào dung dịch AgNO3 dư đến khi phản ứng hoàn toàn, thu được chất rắn có khối lượng là
 Xem đáp án
Xem đáp án
Chọn D
Câu 24:
21/07/2024Chất nào sau đây khi tác dụng với dung dịch HNO3 đặc, nóng, dư, không giải phóng khí NO2?
 Xem đáp án
Xem đáp án
Chọn D
Câu 25:
19/07/2024Thủy phân hết m gam saccarozơ trong môi trường axit rồi cho toàn bộ sản phẩm tác dụng với AgNO3 dư trong dung dịch NH3, thu được tối đa 21,6 gam Ag. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn C
Câu 26:
19/07/2024Cho các este sau: etyl axetat (1), vinyl axetat (2), triolein (3), metyl acrylat (4), phenyl axetat (5). Dãy gồm các este đều làm mất màu dung dịch nước brom là
 Xem đáp án
Xem đáp án
Chọn D
Câu 27:
19/07/2024Cho dãy các chất sau: amilozơ, amilopectin, xenlulozơ, glicogen. Số chất trong dãy có công thức đơn giản C6H10O5 là
 Xem đáp án
Xem đáp án
Chọn C
Câu 28:
19/07/2024Cho m gam hỗn hợp gồm hai aminoaxit (đều có dạng H2N-CnH2n-COOH) tác dụng vừa đủ với 0,15 mol HCl trong dung dịch, thu được dung dịch chứa 17,425 gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B
Câu 29:
21/07/2024Nung m gam hỗn hợp Mg và Al trong khí oxi dư, thu được 5,6 gam hỗn hợp X chỉ chứa các oxit. Hòa tan hết X cần vừa đủ 425 ml dung dịch HCl 1M. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn A
Câu 30:
22/07/2024Cho các loại tơ sau: capron, xenlulozơ axetat, tằm, nitron và nilon-6,6. Có bao nhiêu tơ tổng hợp là
 Xem đáp án
Xem đáp án
Chọn C
Câu 31:
20/07/2024Hấp thụ hết một lượng khí CO2 vào dung dịch chứa a mol NaOH thu được dung dịch X. Nhỏ từ từ từng giọt cho đến hết lượng X vào 140 ml dung dịch HCl 1M và khuấy đều thu được 2,24 lít khí CO2 (đktc). Mặt khác, nếu cho toàn bộ X tác dụng với lượng dư dung dịch Ba(OH)2 thu được 24,625 gam kết tủa. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn A.
Dung dịch X chứa Na2CO3 (x mol) và NaHCO3 (y mol).
Khi cho X tác dụng với HCl thì:
Khi cho X tác dụng với Ba(OH)2 thì x + y = 0,125 x = 0,05; y = 0,075
Câu 32:
21/07/2024Cho các thí nghiệm sau:
(a) Nung hỗn hợp gồm Al và Fe2O3 ở nhiệt độ cao.
(b) Sục khí NH3 đến dư vào dung dịch FeCl3.
(c) Nung nóng Cu(NO3)2 ở nhiệt độ cao.
(d) Cho hỗn hợp Mg và Fe2(SO4)3 (tỉ lệ mol 1 : 1) vào nước dư.
(e) Điện phân dung dịch AgNO3 với điện cực trơ.
Số thí nghiệm sau khi các phản ứng xảy ra hoàn toàn, thu được đơn chất trong sản phẩm là
 Xem đáp án
Xem đáp án
Chọn A.
(a) 2Al + Fe2O3 Al2O3 + 2Fe.
(b) 3NH3 + FeCl3 + 3H2O Fe(OH)3 + 3NH4Cl.
(c) 2Cu(NO3)2 2CuO + 4NO2 + O2.
(d) Mg + Fe2(SO4)3 MgSO4 + 2FeSO4 (phản ứng vừa đủ nên không có kim loại tạo thành).
(e) 2AgNO3 + H2O 2Ag + 2HNO3 + 1/2O2.
Thí nghiệm thu được đơn chất là (a), (c), (e).
Câu 33:
22/07/2024Thủy phân hoàn toàn hỗn hợp E chứa hai triglixerit X và Y trong dung dịch NaOH (đun nóng, vừa đủ), thu được 3 muối C15H31COONa, C17H33COONa, C17H35COONa với tỉ lệ mol tương ứng 2,5 : 1,75 : 1 và 6,44 gam glixerol. Mặt khác đốt cháy hoàn toàn 47,488 gam E cần vừa đủ a mol khí O2. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn D.
Đặt số mol các muối tương ứng là 2,5x; 1,75x và x mol
Khi đó: 2,5x + 1,75x + x = 3nglixerol x = 0,04 mE = mmuối + mglixerol – mNaOH = 59,36 (g)
Trong 47,488 gam có 0,056 mol E (gấp 1/1,25 lần so với ban đầu) và CO2: 3,032 mol (tính từ tổng số mol C trong muối và C trong glixerol) mà
Câu 34:
19/07/2024Cho các phát biểu sau:
(a) Dầu ăn và mỡ động vật có chứa nhiều triglixerit.
(b) Giấm ăn có thể sử dụng để làm giảm mùi tanh của hải sản.
(c) Trong dung dịch, dạng tồn tại chủ yếu của alanin là dạng ion lưỡng cực.
(d) Tơ tằm thuộc loại polime thiên nhiên.
(e) Nhỏ dung dịch iot vào vết cắt quả chuối xanh, xuất hiện màu xanh tím.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn B.
Tất cả các ý đều đúng.
Câu 35:
21/07/2024Hỗn hợp X gồm CuO và MO (M là kim loại có hóa trị không đổi) có tỉ lệ mol tương ứng là 1 : 2. Cho khí CO dư đi qua 2,4 gam X nung nóng, thu được hỗn hợp chất rắn Y. Hòa tan hết Y trong 100 ml dung dịch HNO3 1M, thu được khí NO (sản phẩm khử duy nhất của N+5) và dung dịch chỉ chứa muối. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của CuO trong X là
 Xem đáp án
Xem đáp án
Chọn C.
Nếu M là kim loại trước Al rắn Y gồm Cu: x mol và MO: 2x mol
Ta có:
mà 0,015.80 + 0,03.(M + 16) = 2,4 M = 24: Mg (thỏa). Vậy %mCuO = 50%.
Câu 36:
23/07/2024Đốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm axit axetic, axit oxalic (HOOC-COOH), axit acrylic và 2 hiđrocacbon mạch hở cần vừa đủ V lít O2, thu được CO2 và 3,96 gam H2O. Mặt khác, nếu cho 0,5 mol X vào dung dich Br2 dư, số mol Br2 tham gia phản ứng tối đa là 0,35 mol. Giá trị của V là
 Xem đáp án
Xem đáp án
Chọn B.
X dạng CnH2n+2-2kOx trong đó liên kết đôi C=O không phản ứng với Br2 nên:
nBr2 = 0,5(k – 0,5x) = 0,35 k – 0,5x = 0,7 (1)
CnH2n+2-2kOx + (1,5n + 0,5 – 0,5k – 0,5x)O2 nCO2 + (n + 1 – k)H2O
Số H = 2n + 2 – 2k = = 4,4 n – k = 1,2 (2)
và nO2 = 0,1(1,5n + 0,5 – 0,5k – 0,5x) = 0,1[1,5(n – k) + (k – 0,5x) + 0,5]
Thế (1), (2) vào nO2 = 0,3 V = 6,72 lít.
Câu 37:
22/07/2024Đốt cháy m gam hỗn hợp X gồm Mg và Fe trong oxi một thời gian thu được (m + 4,16) gam hỗn hợp Y chứa các oxit. Hòa tan hoàn toàn Y trong dung dịch HCl vừa đủ thu được dung dịch Z chứa (3m + 1,82) gam muối. Cho AgNO3 dư vào dung dịch Z thu được (9m + 4,06) gam kết tủa. Mặt khác, hòa tan hết 3m gam Y bằng lượng vừa đủ dung dịch chứa hỗn hợp gồm NaNO3 và NaHSO4, thu được dung dịch T chỉ chứa x gam muối sunfat của kim loại và 0,025 mol khí NO (sản phẩm khử duy nhất). Giá trị của x gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D.
Khi cho X tác dụng với oxi thì:
Khi cho Y tác dụng với HCl thì: 3m + 1,82 = m + 35,5.2.0,26 m = 8,32 = 24x + 56.(y + z) (1)
Z chứa Mg2+ (x mol), Fe2+ (y mol), Fe3+ (z mol), Cl- (0,52 mol) (2)
Kết tủa thu được là AgCl (0,52 mol) và Ag (0,04 mol)
Từ (1), (2) suy ra: x = 0,16 và z = 0,04
Khi cho 3m (g) Y tác dụng với hỗn hợp trên thì:
Câu 38:
19/07/2024Hỗn hợp X gồm hai hiđrocacbon mạch hở (cùng số nguyên tử cacbon). Hỗn hợp Y gồm đimetylamin và trimetylamin. Đốt cháy hoàn toàn 0,17 mol hỗn hợp E gồm m gam X và m gam Y cần vừa đủ 0,56 mol O2, thu được hỗn hợp khí và hơi Z. Dẫn toàn bộ Z vào bình đựng dung dịch Ca(OH)2 dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng dung dịch giảm 12,96 gam so với dung dịch ban đầu và có 0,672 lít khí thoát ra. Biết m gam X tác dụng tối đa với a mol H2 (xúc tác Ni, to). Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn C.
Hidrocacbon = CH4 + ?CH2 – ?H2 và amin no, đơn chức (CnH2n+3N) = CH4 + ?CH2 + NH
Quy đổi hỗn hợp X thành CH4 (0,17 mol), CH2 (x mol), H2 (y mol) và NH (0,06 mol)
Theo phản ứng cháy ta có: = 0,17.2 + 1,5.x + 0,5.y + 0,25.0,06 = 0,56 (1)
Khối lượng dung dịch giảm: = –mdd giảm
44.(0,17 + x) + 18.(0,17.2 + x + y + 0,06.0,5) – 100.(0,17 + x) = -12,96 (2)
Từ (1), (2) suy ra: x = 0,19 và y = -0,16
Vậy khi cho X tác dụng với H2 thì a = -y = 0,16 mol.
Câu 39:
19/07/2024X, Y, Z là 3 este đều mạch hở và đều không chứa nhóm chức khác (trong đó X, Y đều đơn chức, Z hai chức). Đun nóng 19,28 gam hỗn hợp E chứa X, Y, Z với dung dịch NaOH vừa đủ thu được hỗn hợp F chỉ chứa 2 muối (tỉ lệ mol tương ứng là 1 : 1) và hỗn hợp gồm 2 ancol đều no, mạch hở có cùng số nguyên tử cacbon. Dẫn toàn bộ hỗn hợp 2 ancol này qua bình đựng Na dư thấy khối lượng bình tăng 8,1 gam. Đốt cháy hoàn toàn F thu được CO2, 0,39 mol H2O và 0,13 mol Na2CO3. Phần trăm khối lượng của Z có trong E là
 Xem đáp án
Xem đáp án
Chọn A.
m(ancol) = 8,1 + 0,13.2 = 8,36 gam (trong đó:
este + NaOH muối + ancol
Bảo toàn khối lượng: 19,28 + 0,26.40 = 8,36 + mmuối mmuối = 21,32 gam
Muối + O2 Na2CO3 + CO2 + H2O
x 0,13 y 0,39
x = 0,52 và y = 0,39 Muối đơn chức, no, mạch hở trong đó
Ancol đơn chức và hai chức là C2H5OH 0,02 mol và C2H4(OH)2 0,12 mol
Vậy Z là HCOOC2H4OOCC2H5 0,12 mol %mZ = 90,87%.
Câu 40:
23/07/2024Tiến hành các bước thí nghiệm như sau:
Bước 1: Cho một nhúm bông vào cốc đựng dung dịch H2SO4 70%, đun nóng đồng thời khuấy đều đến khi phản ứng hoàn toàn, thu được dung dịch đồng nhất.
Bước 2: Trung hòa dung dịch thu được bằng dung dịch NaOH 10%.
Bước 3: Lấy dung dịch sau khi trung hòa cho vào ống nghiệm đựng dung dịch AgNO3 trong NH3 dư, đun nóng nhẹ trên ngọn lửa đèn cồn.
Cho các nhận định sau đây
(a) Sau bước 1, trong cốc thu được một loại monosaccarit.
(b) Phản ứng xảy ra trong bước 1 là phản ứng thuận nghịch.
(c) Có thể thay dung dịch H2SO4 70% bằng dung dịch H2SO4 98%.
(d) Sau bước 3, trên thành ống nghiệm xuất hiện lớp kim loại màu trắng bạc.
(e) Trong bước 3, có thể thay việc đun trên ngọn lửa đèn cồn bằng cách ngâm trong cốc nước nóng.
(f) Thí nghiệm trên dùng để chứng minh xenlulozơ có chứa nhiều nhóm -OH.
Số nhận định đúng là
 Xem đáp án
Xem đáp án
Chọn C.
(b) Sai, Phản ứng xảy ra trong bước 1 là phản ứng một chiều.
(c) Sai, Dung dịch H2SO4 đặc ngăn cản quá trình thủy phân của xenlulozơ.
(f) Sai, Thí nghiệm trên dùng để chứng minh xenlulozơ có phản ứng thủy phân tạo glucozơ.
Bài thi liên quan
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 1)
-
40 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 2)
-
40 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 3)
-
40 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 4)
-
33 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 5)
-
40 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 6)
-
40 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 7)
-
40 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 8)
-
40 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 9)
-
32 câu hỏi
-
40 phút
-
-
Bộ đề thi Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) ( đề 10)
-
32 câu hỏi
-
40 phút
-
