Giáo án điện tử Một số hợp chất quan trọng của nitrogen | Bài giảng PPT Hóa 11 Cánh diều
Với Giáo án PPT Hóa 11 Bài 5: Một số hợp chất quan trọng của nitrogen sách Cánh diều sẽ giúp thầy cô dễ dàng biên soạn và giảng dạy bằng giáo án điện tử hay POWERPOINT Một số hợp chất quan trọng của nitrogen.
Chỉ từ 400k mua trọn bộ Giáo án Hóa 11 Cánh diều bản PPT trình bày khoa học, đẹp mắt (Chỉ 50k cho 1 bài giảng bất kì):
B1: Gửi phí vào tài khoản 0711000255837 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank (QR)
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận giáo án.
Xem thử tài liệu tại đây: Link tài liệu
Bài giảng điện tử Hóa 11 Bài 5: Một số hợp chất quan trọng của nitrogen







................................................
................................................
................................................
Tài liệu có 43 trang, trên đây trình bày tóm tắt 10 trang của Giáo án POWERPOINT Hóa 11 Cánh diều Bài 5: Một số hợp chất quan trọng của nitrogen.
Giáo án Bài 5: Một số hợp chất quan trọng của nitrogen
I. MỤC TIÊU
1. Kiến thức
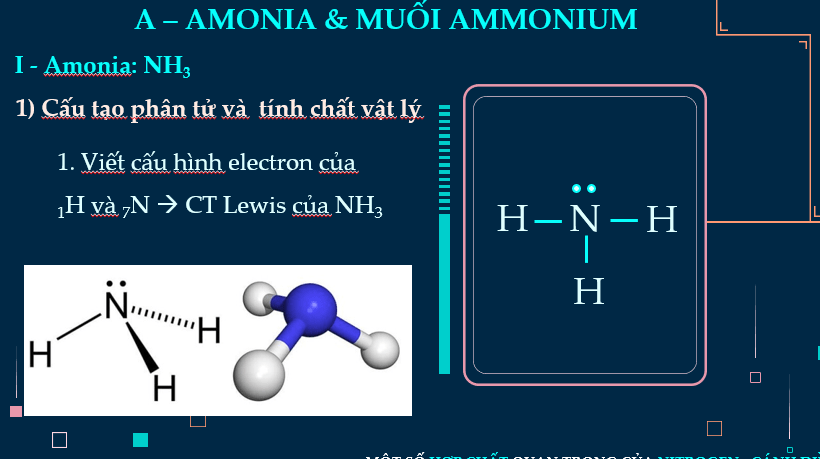
- Mô tả được công thức Lewis và dạng hình học của phân tử ammonia.
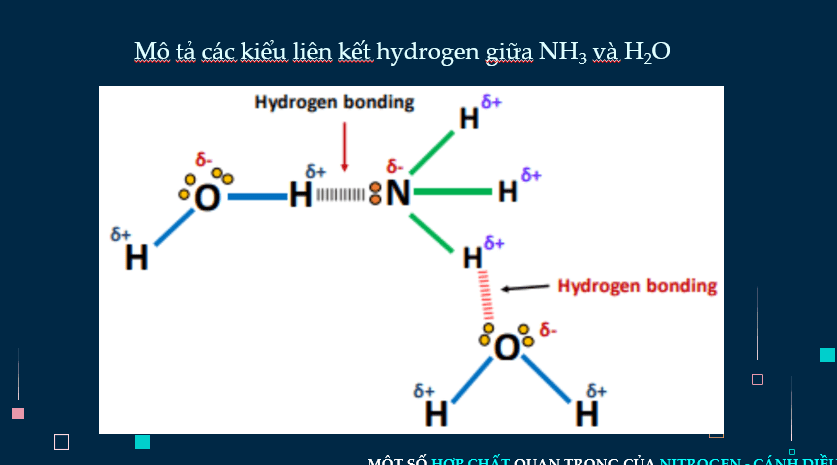
- Dựa vào đặc điểm cấu tạo của phân tử ammonia, giải thích được tính chất vật lý (tính tan), tính chất hóa học (tính base, tính khử). Viết được phương trình hóa học minh họa.
- Vận dụng được kiến thức về cân bằng hóa học, tốc độ phản ứng, biến thiên enthalpy cho phản ứng tổng hợp ammonia từ nitrogen và hydrogen trong quá trình Haber.
- Trình bày được các tính chất cơ bản của muối ammonium (dễ tan và phân li, chuyển hóa thành ammonia trong kiềm, dễ bị nhiệt phân) và nhận biết được ion ammonium trong dung dịch.
- Trình bày được ứng dụng của ammonia (chất làm lạnh; sản xuất phân bón như: đạm, ammophos; sản xuất axit nitric acid; làm dung môi, ...) của ammonium nitrate và một số muối ammonium tan trong phân đạm, phân ammophos,...
- Thực hiện được (hoặc quan sát video) thí nghiệm nhận biết ion amonium trong phân đạm chứa ion ammonium.
- Phân tích được nguồn gốc của các oxide của nitrogen trong không khí và nguyên nhân gây ra hiện tượng mưa acid.
- Nêu được cấu tạo của phân tử HNO3, tính acid, tính oxi hóa mạnh trong một số ứng dụng thực tiễn quan trọng của nitric acid.
- Giải thích được nguyên nhân, hệ quả của hiện tượng phú dưỡng (eutrophication).
2. Năng lực
* Năng lực chung:
- Năng lực tự chủ và tự học: Kĩ năng tìm kiếm thông tin trong SGK, quan sát hình ảnh để tìm hiểu về ammonia, muối ammonium và nitric acid.
- Năng lực giao tiếp và hợp tác: Làm việc nhóm tìm hiểu về ammonia, muối ammonium và nitric acid.
- Năng lực giải quyết vấn đề và sáng tạo: Giải thích được tính oxi hoá mạnh của nitric acid.
* Năng lực hóa học:
a. Nhận thức hoá học: Trình bày được:
- Cấu tạo và tính chất vật lý của ammonia.
- Tính chất hóa học cơ bản của muối ammonium.
- Tính chất hoá học của nitric acid.
- Cách xử lí, phòng tránh hiện tượng phú dưỡng.
b. Tìm hiểu tự nhiên dưới góc độ hóa học được thực hiện thông qua các hoạt động: Thảo luận, quan sát thí nghiệm tính chất vật lý, hoá học của ammonia, muối ammonium và nitric acid, hiện tượng mưa acid.
c. Vận dụng kiến thức, kĩ năng đã học để giải thích được hiện tượng mưa acid
3. Phẩm chất
- Chăm chỉ, tự tìm tòi thông tin trong SGK về tính chất vật lí, tính chất hoá học của ammonia; nitric acid .
- HS có trách nhiệm trong việc hoạt động nhóm, hoàn thành các nội dung được giao.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Giáo viên
- Hình ảnh, video về ammonia, ammonium và nitric acid
- Giáo án, slide, máy tính, máy chiếu.
- Phiếu bài tập số 1, số 2....
- 4 bộ dụng cụ hoá chất gồm:
+ Dụng cụ: ống nghiệm, giá để ống nghiệm, đèn cồn.
+ Hoá chất: dung dịch NaOH, dung dịch NH3 đặc, dung dịch HCl đặc, dung dịch MgCl2.
2. Học sinh
- SGK, SBT, vở ghi.
- Ôn tập bài cũ và chuẩn bị bài mới trước khi đến lớp.
III. TIẾN TRÌNH DẠY HỌC
Kiểm tra bài cũ: Không kiểm tra đầu giờ, kiểm tra kiến thức cũ lồng vào trong tiết học.
1. Hoạt động 1: Khởi động
a) Mục tiêu: Thông qua thí nghiệm giúp HS biết được tính chất vật lý của ammonia, muối ammonium.
b) Nội dung:
+ Trong các ao tù có thể tích tụ lượng đáng kể ion ammonium. Có thể nhận biết sự có mặt của ion ammonium trong các ao tù bằng những cách nào? Giải thích.
+ Tiến hành thí nghiệm: Đung nóng dung dịch nước ao trong kiềm, nếu sinh ra khí có mùi khai và xốc và làm quỳ tím ẩm hóa xanh chứng tỏ có ion ammonium trong ao.
c) Sản phẩm: HS dựa thí nghiệm, đưa ra dự đoán của bản thân.
d) Tổ chức thực hiện:
Giao nhiệm vụ học tập:
- GV nêu vấn đề: Trong các ao tù có thể tích tụ lượng đáng kể ion ammonium. Có thể nhận biết sự có mặt của ion ammonium trong các ao tù bằng những cách nào? Giải thích.
- HS nhận nhiệm vụ.
Thực hiện nhiệm vụ:
- HS thảo luận theo nhóm đưa ra hướng giải quyết và tiến hành thí nghiệm minh hoạ hướng giải quyết (nếu có thể).
Báo cáo thảo luận:
- HS trình bày kết quả.
Kết luận, nhận định:
GV tổng kết, chốt kiến thức và dẫn dắt HS vào bài mới.
2. Hoạt động 2: Hình thành kiến thức mới
Hoạt động 2.1. Tìm hiểu cấu tạo phân tử và tính chất vật lí của ammonia
a) Mục tiêu:
- Mô tả được công thức Lewis và dạng hình học của phân tử ammonia.
- Dựa vào đặc điểm cấu tạo của phân tử ammonia, giải thích được tính chất vật lý (tính tan).
b) Nội dung: GV thực hiện vấn đáp gợi mở tìm tòi để hình thành kiến thức ở HS.
c) Sản phẩm: Cấu tạo phân tử và tính chất vật lí của ammonia.
d) Tổ chức thực hiện
|
Hoạt động của GV và HS |
Nội dung |
|
Giao nhiệm vụ học tập: - Gv: + Dựa vào cấu tạo của ngtử N và H hãy mô tả sự hình thành phân tử ammonia? Viết công thức Lewis phân tử ammonia? + Quan sát video thí nghiệm thử tính tan của Ammonia. Dựa vào cấu tạo giải thích tính chất vật lý của ammonia. Thực hiện nhiệm vụ: Hs: Dựa vào kiến thức lớp 10 và sgk: Trong phân tử NH3 + Nguyên tử N liên kết với 3 nguyên tử H bằng 3 liên kết CHT có cực. + Nguyên tử N còn có 1 cặp e hoá trị. + Nguyên tử N có số oxi hoá thấp nhất -3 |
................................................
................................................
................................................
Xem thử tài liệu tại đây:
Xem thêm các chương trình khác:
- Giáo án Toán 11 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Sinh học 11 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Hóa 11 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Ngữ văn 11 Kết nối tri thức (mới nhất)
- Giáo án Vật lí 11 Kết nối tri thức (mới nhất)
- Giáo án PPT Vật lí 11 Kết nối tri thức
- Giáo án Lịch sử 11 Kết nối tri thức (mới nhất)
- Giáo án Tiếng Anh 11 Global success (mới nhất)
- Giáo án PPT Toán 11 Kết nối tri thức
- Giáo án PPT Lịch sử 11 Kết nối tri thức
- Giáo án Địa lí 11 Kết nối tri thức (mới nhất)
- Giáo án Chuyên đề học tập Địa lí 11 Kết nối tri thức (mới nhất)
- Giáo án PPT Sinh học 11 Kết nối tri thức
- Giáo án PPT Hóa 11 Kết nối tri thức
- Giáo án PPT Địa lí 11 Kết nối tri thức
- Giáo án PPT Kinh tế pháp luật 11 Kết nối tri thức
- Giáo án Toán 11 Chân trời sáng tạo năm 2024 (mới nhất)
- Giáo án Ngữ văn 11 Chân trời sáng tạo (mới nhất)
- Giáo án Hóa 11 Chân trời sáng tạo (mới nhất)
- Giáo án Vật lí 11 Chân trời sáng tạo (mới nhất)
- Giáo án PPT Vật lí 11 Chân trời sáng tạo
- Giáo án PPT Toán 11 Chân trời sáng tạo
- Giáo án PPT Ngữ văn 11 Chân trời sáng tạo
- Giáo án PPT Hóa 11 Chân trời sáng tạo
- Giáo án Lịch sử 11 Chân trời sáng tạo (mới nhất)
- Giáo án Địa lí 11 Chân trời sáng tạo (mới nhất)
- Giáo án Chuyên đề học tập Địa lí 11 Chân trời sáng tạo (mới nhất)
- Giáo án PPT Lịch sử 11 Chân trời sáng tạo
- Giáo án PPT Địa lí 11 Chân trời sáng tạo
- Giáo án PPT Sinh học 11 Chân trời sáng tạo
- Giáo án Sinh học 11 Chân trời sáng tạo năm 2024 (mới nhất)
- Giáo án PPT Kinh tế pháp luật 11 Chân trời sáng tạo
