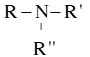Amine | Chuyên đề dạy thêm Hoá học 12 (chương trình mới)
Tài liệu Chủ đề 1: Amine gồm các dạng bài tập trắc nghiệm và tự luận từ cơ bản đến nâng cao giúp thầy cô có thêm tài liệu giảng dạy Hoá học lớp 12.
Chỉ từ 300k mua trọn bộ Chuyên đề dạy thêm Hóa 12 (cả 3 sách) bản word có lời giải chi tiết:
B1: Gửi phí vào tài khoản 0711000255837 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank (QR)
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận tài liệu.
Xem thử tài liệu tại đây: Link tài liệu
CHỦ ĐỀ 1. AMINE
* HỆ THỐNG LÝ THUYẾT
I. Khái niệm, phân loại, đồng phân, danh pháp
1. Khái niệm
- Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen trong phân tử ammonia được thay thế bằng gốc hydrocarbon.
VD: CH3NH2, C6H5NH2, CH3 – NH – CH3, (CH3)3N, …
2. Phân loại
|
Theo bậc amine |
Theo bản chất gốc hydrocarbon |
|
- Bậc amine = số gốc hydrocarbon (R) liên kết trực tiếp với nguyên tử nitrogen. ♦ Amine bậc một: R – NH2 ♦ Amine bậc hai: R – NH – R’ ♦ Amine bậc ba: |
- Được phân thành nhiều loại trong đó có hai loại điển hình: ♦ Alkylamine: Nhóm amine liên kết với gốc alkyl. Công thức: CnH2n+3N (n ≥ 1). VD: C2H5NH2, CH3 – NH – CH3, … ♦ Arylamine (amine thơm): Nhóm amine liên kết trực tiếp với nguyên tử carbon của vòng benzene. VD: C6H5-NH2 (C6H5-: phenyl), … |
3. Đồng phân
- Amine từ 2C trở lên có thể có các đồng phân: bậc amine, mạch carbon, vị trí nhóm amine.
- Khi viết đồng phân amine thì viết theo từng bậc, số đồng phân alkylamine: 2n-1 (n < 5).
4. Danh pháp
♦ Tên gốc chức = tên gốc hydrocabon + amine (viết liền).
♦ Tên thay thế
+ Tên amine bậc một = tên hydrocarbon (bỏ e) + vị trí nhóm amine + amine
+ Tên amine bậc hai = N – tên gốc hydrocarbon + tên gốc hydrocarbon mạch chính + vị trí nhóm amine + amine
+ Tên amine bậc ba = N – tên gốc HC thứ nhất – N – tên gốc HC thứ hai + tên gốc hydrocarbon mạch chính + vị trí nhóm amine + amine (nếu gốc giống nhau thì dùng tiền tố di (2), tri (3), …)
♦ Tên thông thường: VD: C6H5NH2: aniline.
|
Amine |
Tên gốc – chức |
Tên thay thế |
|
CH3NH2 |
methylamine |
methanamine |
|
CH3CH2NH2 |
ethylamine |
Ethanamine |
|
CH3CH2CH2NH2 |
propylamine |
Propan – 1 – amine |
|
CH3 – CH(NH2) – CH3 |
isopropylamine |
Propan – 2 – amine |
|
CH3 – NH – CH3 |
dimethylamine |
N – methylmethanamine |
|
(CH3)3N |
trimethylamine |
N, N – dimethylmethanamine |
II. Đặc điểm cấu tạo
|
|
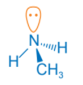
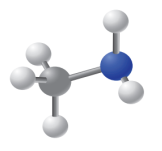
Methylamine (CH3NH2) |
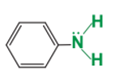
Aniline (C6H5NH2) |
|
Cấu trúc phân tử |
|
|
|
Mô hình phân tử |
|
|
- Trong phân tử amine, nguyên tử nitrogen còn cặp electron chưa liên kết tương tự ammonia ⇒ Amine có một số tính chất hóa học tương tự ammonia, riêng aniline còn dễ tham gia phản ứng thế nguyên tử hydrogen trong nhân thơm do ảnh hưởng của nhóm -NH2.
III. Tính chất vật lí
- Ở điều kiện thường, CH3NH2, C2H5NH2, CH3 – NH – CH3, (CH3)3N là những chất khí có mùi tanh của cá hoặc mùi khai; các amin có phân tử khối lớn hơn là chất lỏng hoặc rắn.
- Các amine có số carbon nhỏ thường tan tốt trong nước do tạo được liên kết hydrogen với nước, độ tan giảm khi số nguyên tử carbon trong gốc hydrocarbon tăng.
- Amine có nhiệt độ sôi cao hơn so với hydrocarbon có cùng số nguyên tử carbon.
Thứ tự giảm nhiệt độ sôi: Hợp chất ion > carboxylic acid > alcohol > amine > ester > hydrocarbon
- Ở điều kiện thường, aniline là chất lỏng, ít tan trong nước.
IV. Tính chất hóa học
1. Tính base và phản ứng tạo phức
(a) Tính base
- Tương tự ammonia, các amine thể hiện tính base yếu: RNH2 + H2O ⇌RNH3+ + OH-
- Tính base: aniline < NH3 < alkylamine.
- Thí nghiệm thể hiện tính base của amine:
|
|
Đĩa thủy tinh |
Ống nghiệm (1) |
Ống nghiệm (2) |
|
Bước 1 |
Đặt vào mẩu giấy quỳ tím. |
Lấy 2 mL dung dịch CH3NH2 và nhỏ thêm vài giọt phenolphthalein. |
Lấy khoảng 1 mL dung dịch FeCl3. |
|
Bước 2 |
Nhỏ vài giọt dung dịch CH3NH2 vào mẩu giấy quỳ tím. |
Nhỏ từ từ 2 mL dung dịch HCl vào, lắc đều. |
Nhỏ từ từ khoảng 3 mL dung dịch CH3NH2 vào, lắc đều. |
|
Hiện tượng |
Quỳ tím chuyển màu xanh. |
Dung dịch từ màu hồng chuyển thành mất màu. |
Xuất hiện kết tủa nâu đỏ. |
♦ Đổi màu chất chỉ thị: Alkylamine đổi màu quỳ tím → xanh, phenolphthalein → hồng, aniline không làm đổi màu quỳ tím và phenolphthalein vì là base yếu hơn.
♦ Tác dụng với acid → muối ammonium
TQ: RNH2 + HCl → RNH3Cl
CH3NH2 + HCl → CH3NH3Cl
C6H5NH2 + HCl → C6H5NH3Cl
♦ Tác dụng với dung dịch muối → Muối ammonium + base mới (kết tủa)
TQ: 3RNH2 + 3H2O + FeCl3 → 3RNH3Cl + Fe(OH)3↓nâu đỏ
3CH3NH2 + 3H2O + FeCl3 → CH3NH3Cl + Fe(OH)3↓nâu đỏ
(b) Khả năng tạo phức
♦ Thí nghiệm tạo phức của methylamine:
- Bước 1: Cho khoảng 2 mL dung dịch CuSO4 0,1 M vào ống nghiệm.
- Bước 2: Thêm từ từ dung dịch methylamine 0,1 M vào ống nghiệm, lắc đều.
- Hiện tượng: Xuất hiện kết tủa xanh lam sau đó kết tủa tan hết.
- Các amine như methylamine, ethylamine có khả năng hòa tan Cu(OH)2 tạo dung dịch phức chất có màu xanh lam. PTHH: 4CH3NH2 + Cu(OH)2 → [Cu(CH3NH2)4](OH)2
2. Phản ứng với nitrous acid (tính khử)
- Alkylamine bậc một tác dụng với nitrous acid ở nhiệt độ thường tạo alcohol và giải phóng N2.
TQ: RNH2 + HNO2 → ROH + N2↑ + H2O ⇒ PƯ dùng để nhận biết amine bậc một.
(HONO)
- Aniline tác dụng với nitrous acid ở nhiệt độ thấp (0 – 5 oC) tạo thành muối diazonium (thường dùng để tổng hợp phẩm nhuộm azo và dược phẩm).
PTHH: C6H5NH2 + HNO2 + HCl 0−5oC−−−→[C6H5N2]+Cl-
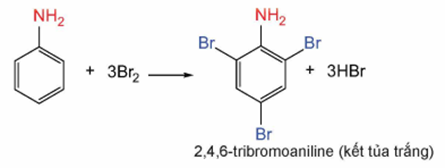
3. Phản ứng của aniline với nước bromine
♦ Thí nghiệm phản ứng của aniline với nước bromine.
- Bước 1: Cho khoảng 1mL nước bromine vào ống nghiệm
- Bước 2: Thêm từ từ vài giọt dung dịch aniline loãng vào ống nghiệm.
- Hiện tượng: Dung dịch bromine bị mất màu đồng thời xuất hiện kết tủa trắng.
- Tương tự phenol, aniline giam gia phản ứng thế nguyên tử H trong vòng benzene dễ hơn benzene do có nhóm -NH2 đẩy e vào vòng benzene. Phản ứng thế ưu tiên ở các vị trí ortho và para.
V. Ứng dụng và điều chế
1. Ứng dụng
- Aniline là nguyên liệu quan trọng để tổng hợp phẩm nhuộm (phẩm màu azo), dược phẩm (paracetamol) hay polymer.
- Một số diamine dùng làm nguyên liệu tổng hợp polymer. VD: hexamethylenediamine (H2N – (CH2)6 – NH2) được sử dụng để tổng hợp nylon-6,6.
2. Điều chế
♦ Alkyl hóa ammonia
- Alkylamine được điều chế từ ammonia và dẫn xuất halogen, tùy tỉ lệ mol các chất tham gia phản ứng có thể tạo được amine bậc một, bậc hai hoặc bậc ba.
![]()
♦ Khử hợp chất nitro
- Aniline và các arylamine thường được điều chế bằng cách khử hợp chất nitro (-NO2) tương ứng bởi một số kim loại (Zn, Fe, …) trong dung dịch HCl.
C6H5NO2 + 6[H] Fe+HCl−−−−→to C6H5NH2 + 2H2O
❖ BÀI TẬP TỰ LUẬN
Câu 1. [CD -SGK] Cho các chất có công thức cấu tạo sau:
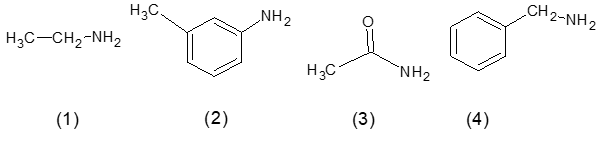
Trong các chất trên, hãy cho biết:
(a) Chất nào là amine.
(b) Chất nào thuộc loại arylamine.
Câu 2. [KNTT - SGK] Phân loại các amine dưới đây dựa trên bậc của amine và dựa trên đặc điểm cấu tạo
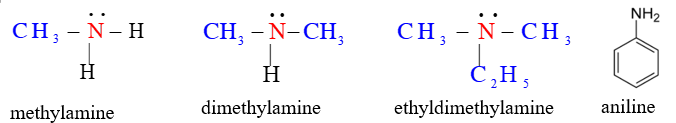
Câu 3. Viết đồng phân, gọi tên thay thế, tên gốc – chức, xác định bậc của các amine có công thức C2H7N, C3H9N, C4H11N.
Câu 4. Viết các đồng phân amin bậc hai và bậc ba của amine có công thức C5H13N.
Câu 5.
(a) Cho các chất: (1) CH3COOH, (2) C2H5OH, (3) C2H6, (4) CH3COONa, (5) HCOOCH3, (6) C2H5NH2. Sắp xếp các chất trên theo thứ tự nhiệt độ sôi giảm dần.
(b) Cho các chất: (1) C2H5NH2, (2) NH3, (3) C6H5NH2, (4) (C2H5)2NH, (5) (C6H5)2NH. Sắp xếp các chất trên theo thứ tự tính base tăng dần.
Câu 6. Viết phương trình phản ứng xảy ra khi cho:
(a) Methylamine lần lượt tác dụng với dung dịch: HCl, FeCl3, CuSO4, HNO2.
(b) Aniline lần lượt tác dụng với dung dịch: HCl, HNO2/HCl, Br2.
Câu 7. [CTST – SGK] Mùi tanh của cá chủ yếu do amine gây ra như trimethylamine. Làm thế nào để khử mùi tanh của cá?
Câu 8. [CD - SGK] Cho chuỗi chuyển hóa sau:
![]()
Cho biết công thức cấu tạo của các chất X, Y, Z trong chuỗi chuyển hóa trên và viết phương trình hóa học thực hiện chuỗi chuyển hóa.
Câu 9. Các phát biểu sau đúng hay sai? Nếu sai hãy giải thích.
(1) Amine thuộc loại hợp chất hữu cơ tạp chức.
(2) Tất cả amine đều là chất khí, mùi khai, dễ tan trong nước.
(3) Tính base của aniline yếu hơn tính base của methylamine.
(4) Amine là hợp chất hữu được hình thành khi thay thế ba nguyên tử H trong phân tử NH3 bằng ba gốc hydrocarbon.
(5) Alkylamine là những amine có nhóm amine liên kết với gốc alkyl có công thức chung là CnH2n+1N.
(6) Amine C2H7N là alkylamine, có đồng phân amine bậc 1, 2, 3.
(7) Tất cả amine đều có tính base, đều làm quỳ tím hoá xanh.
(8) Methylamine và ethylamine có khả năng hòa tan được Cu(OH)2 ở điều kiện thường tạo dung dịch xanh lam.
(9) Aniline là amine thơm, có tính base yếu hơn NH3.
(10) Ở điều kiện thường aniline (C6H5NH2) là chất khí, tan ít trong nước.
(11) Aniline tác dụng với nước bromine tạo thành kết tủa trắng.
(12) Methylamine và aniline đều tác dụng được với nitrous acid tạo alcohol và giải phóng khí N2.
V BÀI TẬP TRẮC NGHIỆM
♦ Mức độ BIẾT
Câu 1. Chất có chứa nguyên tố nitrogen là
A. methyl amine.
B. saccharose.
C. cellulose.
D. glucose.
Câu 2. [MH - 2022] Phân tử chất nào sau đây chứa nguyên tử nitrogen?
A. Acetic acid.
B. Methylamine.
C. Tinh bột.
D. Glucose.
Câu 3. Công thức chung của amine no, đơn chức, mạch hở (alkylamine) là
A. CnH2n-5N (n ≥ 6).
B. CnH2n+1N (n ≥ 2).
C. CnH2n-1N (n ≥ 2).
D. CnH2n+3N (n ≥ 1).
Câu 4. [QG.22 - 202] Chất X có công thức CH3NH2. Tên gọi của X là
A. trimethylamine.
B. ethylamine.
C. methylamine.
D. dimethylamine.
Câu 5. [QG.22 - 201] Công thức phân tử của ethylamine là
A. C4H11N.
B. CH5N.
C. C3H9N.
D. C2H7N.
Câu 6. (202 – Q.17). Công thức phân tử của dimethylamine là
A. C2H8N2.
B. C2H7N.
C. C4H11N.
D. CH6N2.
Câu 7. [QG.23 - 201] Hợp chất C2H5NHC2H5 có tên là
A. ethylmethylamine.
B. dimethylamine.
C. propylamine.
D. diethylamine.
Câu 8. [QG.23 - 203] Hợp chất CH3NHCH3 có tên là
A. propylamine
B. ethylmethylamine
C. dimethylamine
D. diethylamine.
Câu 9. [MH - 2023] Chất nào sau đây là amine bậc một?
A. CH3NHC2H5.
B. (CH3)2NH.
C. (C2H5)3N.
D. C6H5NH2.
Câu 10. (Q.15): Chất nào sau đây thuộc loại amine bậc một?
A. (CH3)3N.
B. CH3NHCH3.
C. CH3NH2.
D. CH3CH2NHCH3
.......................................................
.......................................................
.......................................................
Xem thêm các chương trình khác:
- Soạn văn 12 Kết nối tri thức (hay nhất)
- Văn mẫu 12 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 12 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn 12 - Kết nối tri thức
- Bố cục tác phẩm Ngữ văn 12 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn 12 – Kết nối tri thức
- Giải sgk Toán 12 – Kết nối tri thức
- Giải Chuyên đề học tập Toán 12 – Kết nối tri thức
- Lý thuyết Toán 12 – Kết nối tri thức
- Giải sbt Toán 12 – Kết nối tri thức
- Bài tập Tiếng Anh 12 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 12 - Global success
- Trọn bộ Từ vựng Tiếng Anh 12 Global success đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 12 Global success đầy đủ nhất
- Giải sbt Tiếng Anh 12 – Global Success
- Giải sgk Vật lí 12 – Kết nối tri thức
- Giải Chuyên đề học tập Vật lí 12 – Kết nối tri thức
- Lý thuyết Vật lí 12 – Kết nối tri thức
- Giải sbt Vật lí 12 – Kết nối tri thức
- Giải sgk Sinh học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Sinh học 12 – Kết nối tri thức
- Lý thuyết Sinh học 12 – Kết nối tri thức
- Giải sbt Sinh học 12 – Kết nối tri thức
- Giải sgk Lịch sử 12 – Kết nối tri thức
- Giải Chuyên đề học tập Lịch sử 12 – Kết nối tri thức
- Giải sbt Lịch sử 12 – Kết nối tri thức
- Giải sgk Địa lí 12 – Kết nối tri thức
- Giải Chuyên đề học tập Địa lí 12 – Kết nối tri thức
- Giải sbt Địa lí 12 – Kết nối tri thức
- Giải sgk Tin học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Tin học 12 – Kết nối tri thức
- Giải sbt Tin học 12 – Kết nối tri thức
- Lý thuyết Tin học 12 - Kết nối tri thức
- Giải sgk Công nghệ 12 – Kết nối tri thức
- Giải sgk Kinh tế pháp luật 12 – Kết nối tri thức
- Giải Chuyên đề học tập Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sbt Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng 12 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 12 – Kết nối tri thức