Câu hỏi:
12/11/2024 126
Trong thể dục thể thao, có một số vận động viên sử dụng các loại chất kích thích trong thi đấu, gọi là doping, dẫn đến thành tích đạt được của họ không thật so với năng lực vốn có. Một trong các loại doping thường gặp nhất là testosterone tổng hợp.
Tỉ lệ giữa hai đồng vị (98,98%) và (1,11%) là không đổi đối với testosterone tự nhiên trong cơ thể. Trong khi testosterone tổng hợp (tức doping) có phần trăm số nguyên tử đồng vị ít hơn testosterone tự nhiên. Đây chính là mấu chốt của xét nghiệm CIR (Carbon Isotope Ratio – Tỉ lệ đồng vị carbon) – một xét nghiệm với mục đích xác định xem vận động viên có sử dụng doping hay không.
Giả sử, thực hiện phân tích CIR đối với một vận động viên thu được kết quả phần trăm số nguyên tử đồng vị là x và là y. Từ tỉ lệ đó, người ta tính được nguyên tử khối trung bình của carbon trong mẫu phân tích có giá trị là 12,0098. Với kết quả thu được, em có nghi ngờ vận động viên này sử dụng doping hay không? Vì sao?
Trong thể dục thể thao, có một số vận động viên sử dụng các loại chất kích thích trong thi đấu, gọi là doping, dẫn đến thành tích đạt được của họ không thật so với năng lực vốn có. Một trong các loại doping thường gặp nhất là testosterone tổng hợp.
Tỉ lệ giữa hai đồng vị (98,98%) và (1,11%) là không đổi đối với testosterone tự nhiên trong cơ thể. Trong khi testosterone tổng hợp (tức doping) có phần trăm số nguyên tử đồng vị ít hơn testosterone tự nhiên. Đây chính là mấu chốt của xét nghiệm CIR (Carbon Isotope Ratio – Tỉ lệ đồng vị carbon) – một xét nghiệm với mục đích xác định xem vận động viên có sử dụng doping hay không.
Giả sử, thực hiện phân tích CIR đối với một vận động viên thu được kết quả phần trăm số nguyên tử đồng vị là x và là y. Từ tỉ lệ đó, người ta tính được nguyên tử khối trung bình của carbon trong mẫu phân tích có giá trị là 12,0098. Với kết quả thu được, em có nghi ngờ vận động viên này sử dụng doping hay không? Vì sao?
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
* Trả lời:
Tỉ lệ hai đồng vị (98,98%) và (1,11%) trong testosterone tự nhiên trong cơ thể là
Đối với kết quả mẫu phân tích ta có:
> 89, 171
⇒ Từ kết quả thu được, em nghi ngờ vận động viên này đã có sử dụng doping.
* Mở rộng:
Đồng vị, nguyên tử khối trung bình
1. Đồng vị
- Các nguyên tử của cùng một nguyên tố hóa học có số neutron khác nhau là đồng vị của nhau.
Do đó, đồng vị của cùng một nguyên tố hóa học (có cùng số proton) khác nhau về số khối do đó số neutron khác nhau.
Ví dụ: Helium có hai đồng vị bền là và .
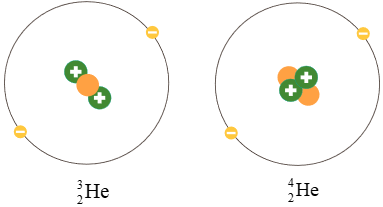
Hình 3.3. Minh họa cấu tạo nguyên tử hai đồng vị của nguyên tố helium
- Tất cả các nguyên tố hóa học đều có nhiều đồng vị.
Ví dụ: Hydrogen có ba đồng vị là (kí hiệu là H), (kí hiệu là D), (kí hiệu là T), oxygen có 17 đồng vị bắt đầu từ và kết thúc là , ...
2. Nguyên tử khối trung bình
a) Nguyên tử khối
- Nguyên tử khối là khối lượng tương đối của một nguyên tử, cho biết khối lượng của một nguyên tử nặng gấp bao nhiêu lần 1 amu.
Ví dụ: Nguyên tử khối của 16O là 16 do khối lượng của một nguyên tử 16O là 16 amu.
b) Nguyên tử khối trung bình
- Mỗi nguyên tố hóa học đều có nhiều đồng vị.
- Trong tự nhiên, một nguyên tố hóa học dù ở dạng đơn chất hay hợp chất thì tỉ lệ giữa các đồng vị của nguyên tố này là không đổi.
- Nguyên tử khối của nguyên tố hóa học có nhiều đồng vị là nguyên tử khối trung bình của các đồng vị (kí hiệu là ![]() ), có tính đến tỉ lệ số nguyên tử các đồng vị tương ứng (xác định từ phổ khối lượng).
), có tính đến tỉ lệ số nguyên tử các đồng vị tương ứng (xác định từ phổ khối lượng).
- Công thức tính nguyên tử khối trung bình như sau:
=
Trong đó:
+ X, Y, Z, ... lần lượt là số khối của các đồng vị.
+ x, y, z, ... là phần trăm số nguyên tử các đồng vị tương ứng.
Ví dụ: Trong tự nhiên, đồng có hai đồng vị bền là 63Cu và 65Cu chiếm tương ứng khoảng 73% và 27% về số nguyên tử. Nguyên tử khối trung bình của đồng là:
= = 63,64
Lưu ý: Nguyên tử khối của một nguyên tố hóa học ghi trong bảng tuần hoàn là nguyên tử khối trung bình của các đồng vị trong tự nhiên.
Xem thêm các bài viết liên quan,chi tiết khác:
Lý thuyết Hóa học 10 Bài 3: Nguyên tố hóa học
Giải bài tập Hóa lớp 10 Bài 3: Nguyên tố hóa học
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Quan sát Hình 3.1, cho biết nguyên tử nitrogen có bao nhiêu proton, neutron và electron.

Hình 3.1 Mô hình nguyên tử nitrogen theo Rutherford
Quan sát Hình 3.1, cho biết nguyên tử nitrogen có bao nhiêu proton, neutron và electron.

Hình 3.1 Mô hình nguyên tử nitrogen theo Rutherford
Câu 2:
Nguyên tử của nguyên tố magnesium (Mg) có 12 proton và 12 neutron. Nguyên tử khối của Mg là bao nhiêu?
Nguyên tử của nguyên tố magnesium (Mg) có 12 proton và 12 neutron. Nguyên tử khối của Mg là bao nhiêu?
Câu 3:
Hoàn thành những thông tin chưa biết trong bảng sau:
Đồng vị
?
?
?
?
Số hiệu nguyên tử
?
?
?
9
11
Số khối
?
?
?
?
23
Số proton
16
?
?
?
?
Số neutron
16
20
?
10
?
Số electron
?
20
?
?
?
Hoàn thành những thông tin chưa biết trong bảng sau:
|
Đồng vị |
? |
? |
|
? |
? |
|
Số hiệu nguyên tử |
? |
? |
? |
9 |
11 |
|
Số khối |
? |
? |
? |
? |
23 |
|
Số proton |
16 |
? |
? |
? |
? |
|
Số neutron |
16 |
20 |
? |
10 |
? |
|
Số electron |
? |
20 |
? |
? |
? |
Câu 4:
Trong tự nhiên, magnesium có 3 đồng vị bền là 24Mg, 25Mg và 26Mg. Phương pháp phổ khối lượng xác nhận đồng vị 26Mg chiếm tỉ lệ phần trăm số nguyên tử là 11%. Biết rằng nguyên tử khối trung bình của Mg là 24,32. Tính % số nguyên tử của đồng vị 24Mg, 25Mg.
Trong tự nhiên, magnesium có 3 đồng vị bền là 24Mg, 25Mg và 26Mg. Phương pháp phổ khối lượng xác nhận đồng vị 26Mg chiếm tỉ lệ phần trăm số nguyên tử là 11%. Biết rằng nguyên tử khối trung bình của Mg là 24,32. Tính % số nguyên tử của đồng vị 24Mg, 25Mg.
Câu 5:
Bổ sung những dữ liệu còn thiếu trong bảng 3.1.
Tên nguyên tố
Kí hiệu
P
N
Số khối (A)
E
Helium
He
2
2
4
2
Lithium
Li
3
4
7
?
Nitrogen
N
7
?
14
7
Oxygen
O
8
8
?
8
Bổ sung những dữ liệu còn thiếu trong bảng 3.1.
|
Tên nguyên tố |
Kí hiệu |
P |
N |
Số khối (A) |
E |
|
Helium |
He |
2 |
2 |
4 |
2 |
|
Lithium |
Li |
3 |
4 |
7 |
? |
|
Nitrogen |
N |
7 |
? |
14 |
7 |
|
Oxygen |
O |
8 |
8 |
? |
8 |
Câu 6:
Silicon là nguyên tố được sử dụng để chế tạo vật liệu bán dẫn, có vai trò quan trọng trong sản xuất công nghiệp. Trong tự nhiên, nguyên tố này có 3 đồng vị với số khối lần lượt là 28, 29, 30. Viết kí hiệu nguyên tử cho mỗi đồng vị của silicon. Biết nguyên tố silicon có số liệu nguyên tử là 14.
Silicon là nguyên tố được sử dụng để chế tạo vật liệu bán dẫn, có vai trò quan trọng trong sản xuất công nghiệp. Trong tự nhiên, nguyên tố này có 3 đồng vị với số khối lần lượt là 28, 29, 30. Viết kí hiệu nguyên tử cho mỗi đồng vị của silicon. Biết nguyên tố silicon có số liệu nguyên tử là 14.
Câu 7:
Kim cương và than chì có vẻ ngoài khác nhau. Tuy nhiên, chúng đều được tạo thành từ cùng một nguyên tố hóa học là nguyên tố carbon (C). Nguyên tố hóa học là gì? Một nguyên tử của nguyên tố hóa học có những đặc trưng cơ bản nào?

Kim cương và than chì có vẻ ngoài khác nhau. Tuy nhiên, chúng đều được tạo thành từ cùng một nguyên tố hóa học là nguyên tố carbon (C). Nguyên tố hóa học là gì? Một nguyên tử của nguyên tố hóa học có những đặc trưng cơ bản nào?

Câu 8:
Điện tích hạt nhân của nguyên tử nitrogen có giá trị là bao nhiêu?
Điện tích hạt nhân của nguyên tử nitrogen có giá trị là bao nhiêu?
Câu 9:
Một nguyên tử X gồm 16 proton, 16 electron và 16 neutron. Nguyên tử X có kí hiệu là:
A.
B.
C.
D.
Một nguyên tử X gồm 16 proton, 16 electron và 16 neutron. Nguyên tử X có kí hiệu là:
A.
B.
C.
D.
Câu 10:
Quan sát Hình 3.2, so sánh điểm giống và khác nhau giữa các loại nguyên tử của nguyên tố hydrogen.
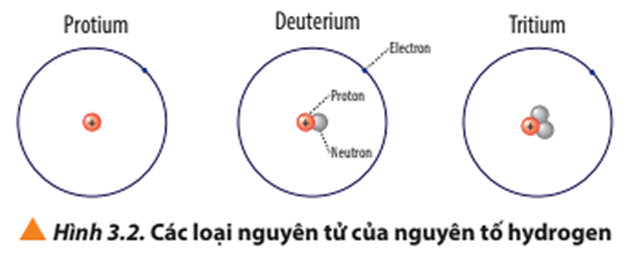
Quan sát Hình 3.2, so sánh điểm giống và khác nhau giữa các loại nguyên tử của nguyên tố hydrogen.

Câu 11:
Trong tự nhiên, nguyên tố copper có hai đồng vị với phần trăm số nguyên tử tương ứng là (69,15%) và (30,85%). Hãy tính nguyên tử khối trung bình của nguyên tố copper.
Trong tự nhiên, nguyên tố copper có hai đồng vị với phần trăm số nguyên tử tương ứng là (69,15%) và (30,85%). Hãy tính nguyên tử khối trung bình của nguyên tố copper.
Câu 12:
Nguyên tố carbon có số hiệu nguyên tử là 6. Xác định điện tích hạt nhân của nguyên tử này
Nguyên tố carbon có số hiệu nguyên tử là 6. Xác định điện tích hạt nhân của nguyên tử này
Câu 13:
Kim cương là một trong những dạng tồn tại của nguyên tố carbon trong tự nhiên. Nguyên tố này có hai đồng vị bền với số khối lần lượt là 12 và 13. Hãy viết kí hiệu nguyên tử của hai đồng vị này.
Kim cương là một trong những dạng tồn tại của nguyên tố carbon trong tự nhiên. Nguyên tố này có hai đồng vị bền với số khối lần lượt là 12 và 13. Hãy viết kí hiệu nguyên tử của hai đồng vị này.
Câu 14:
a) Viết kí hiệu các nguyên tử của nguyên tố hydrogen (Hình 3.2).
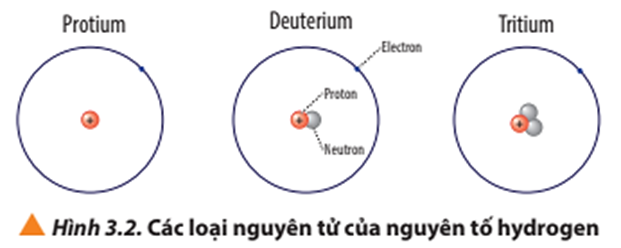
b) Viết kí hiệu nguyên tử của nguyên tố oxygen. Biết nguyên tử của nguyên tố này có 8 electron và 8 neutron.
a) Viết kí hiệu các nguyên tử của nguyên tố hydrogen (Hình 3.2).

b) Viết kí hiệu nguyên tử của nguyên tố oxygen. Biết nguyên tử của nguyên tố này có 8 electron và 8 neutron.


