Câu hỏi:
17/07/2024 135
Trình bày các bước trong quá trình lắp ráp mô hình phân tử NH3.
Trình bày các bước trong quá trình lắp ráp mô hình phân tử NH3.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Các bước trong quá trình lắp ráp mô hình phân tử NH3:
Bước 1: Xác định hình học phân tử của chất cần lắp ráp.
Phân tử NH3 có dạng:
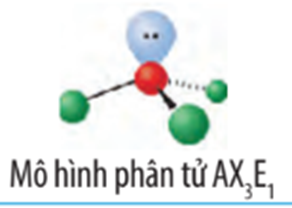
Công thức VESEPR của NH3 là AX3E1. Để giảm tối đa lực đẩy giữa 4 cặp electron hóa trị (gồm 3 cặp electron chung và 1 cặp electron riêng), 4 cặp electron này phải chiếm 4 khu vực điện tích âm sao cho lực đẩy giữa chúng là nhỏ nhất. Tuy nhiên cặp electron riêng đẩy mạnh hơn làm góc liên kết giảm, nên nhỏ hơn 109,5o
Bước 2: Xác định số lượng các loại liên kết và kiểu liên kết trong phân tử, qua đó xác định số lượng mỗi loại khối cầu và số thanh nối cần dùng.
Chọn 3 thanh nối biểu diễn 3 liên kết đơn N-H. Chọn 1 quả cầu biểu diễn nguyên tử N và 3 quả cầu (khác màu với N) biểu diễn 3 nguyên tử H.
Bước 3: Hoàn chỉnh mô hình phân tử

Các bước trong quá trình lắp ráp mô hình phân tử NH3:
Bước 1: Xác định hình học phân tử của chất cần lắp ráp.
Phân tử NH3 có dạng:

Công thức VESEPR của NH3 là AX3E1. Để giảm tối đa lực đẩy giữa 4 cặp electron hóa trị (gồm 3 cặp electron chung và 1 cặp electron riêng), 4 cặp electron này phải chiếm 4 khu vực điện tích âm sao cho lực đẩy giữa chúng là nhỏ nhất. Tuy nhiên cặp electron riêng đẩy mạnh hơn làm góc liên kết giảm, nên nhỏ hơn 109,5o
Bước 2: Xác định số lượng các loại liên kết và kiểu liên kết trong phân tử, qua đó xác định số lượng mỗi loại khối cầu và số thanh nối cần dùng.
Chọn 3 thanh nối biểu diễn 3 liên kết đơn N-H. Chọn 1 quả cầu biểu diễn nguyên tử N và 3 quả cầu (khác màu với N) biểu diễn 3 nguyên tử H.
Bước 3: Hoàn chỉnh mô hình phân tử

CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Trình bày sự hình thành liên kết cho – nhận trong phân tử sulfur dioxide (SO2).
Trình bày sự hình thành liên kết cho – nhận trong phân tử sulfur dioxide (SO2).
Câu 2:
Năng lượng liên kết của các hydrogen halide được liệt kê trong bảng sau:
Hydrogen halide
Năng lượng liên kết (kJ/mol)
HF
565
HCl
427
HBr
363
HI
295
Sắp xếp theo chiều tăng dần độ bền liên kết trong các phân tử HF, HCl, HBr và HI
Năng lượng liên kết của các hydrogen halide được liệt kê trong bảng sau:
|
Hydrogen halide |
Năng lượng liên kết (kJ/mol) |
|
HF |
565 |
|
HCl |
427 |
|
HBr |
363 |
|
HI |
295 |
Sắp xếp theo chiều tăng dần độ bền liên kết trong các phân tử HF, HCl, HBr và HI
Câu 3:
Hydrogen sulfide (H2S) và phosphine (PH3) đều là những chất có mùi khó ngửi và rất độc. Trình bày sự tạo thành liên kết cộng hóa trị trong phân tử các chất trên.
Hydrogen sulfide (H2S) và phosphine (PH3) đều là những chất có mùi khó ngửi và rất độc. Trình bày sự tạo thành liên kết cộng hóa trị trong phân tử các chất trên.
Câu 5:
Viết công thức electron, công thức Lewis và công thức cấu tạo của Cl2, H2O, CH4.
Viết công thức electron, công thức Lewis và công thức cấu tạo của Cl2, H2O, CH4.
Câu 6:
Vẽ sơ đồ xen phủ orbital giữa 2 nguyên tử carbon hình thành liên kết đôi trong phân tử ethylene (C2H4).
Vẽ sơ đồ xen phủ orbital giữa 2 nguyên tử carbon hình thành liên kết đôi trong phân tử ethylene (C2H4).
Câu 9:
Cho biết số liên kết σ và liên kết п trong phân tử acetylene (C2H2).
Cho biết số liên kết σ và liên kết п trong phân tử acetylene (C2H2).
Câu 10:
Nitrogen chiếm khoảng 78% thể tích không khí nhưng chỉ hoạt động ở nhiệt độ cao. Vì sao nitrogen là một chất khí không hoạt động ở điều kiện thường?
Nitrogen chiếm khoảng 78% thể tích không khí nhưng chỉ hoạt động ở nhiệt độ cao. Vì sao nitrogen là một chất khí không hoạt động ở điều kiện thường?
Câu 11:
Mô tả sự tạo thành liên kết trong phân tử chlorine bằng sự xen phủ của các AO.
Mô tả sự tạo thành liên kết trong phân tử chlorine bằng sự xen phủ của các AO.
Câu 13:
Giải thích sự hình thành liên kết trong các phân tử HCl, O2 và N2.
Giải thích sự hình thành liên kết trong các phân tử HCl, O2 và N2.
Câu 14:
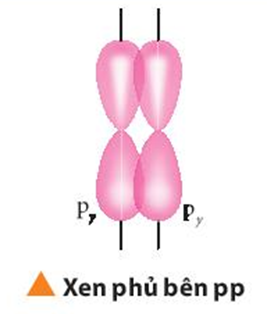
Sự xen phủ giữa hai orbital p trong trường hợp nào sẽ tạo thành liên kết σ? Trong trường hợp nào sẽ tạo thành liên kết π? Cho ví dụ.
Sự xen phủ giữa hai orbital p trong trường hợp nào sẽ tạo thành liên kết σ? Trong trường hợp nào sẽ tạo thành liên kết π? Cho ví dụ.
Câu 15:
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3.
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3.