Câu hỏi:
22/07/2024 266
Alkane (A) có công thức phân tử C8H18. (A) tác dụng với chlorine đun nóng chỉ tạo một dẫn xuất monochloro duy nhất. Tên gọi của (A) là
A. octane. B. 2-methylheptane.
C. 2,2-dimethylhexane. D. 2,2,3,3-tetramethylbutane.
Alkane (A) có công thức phân tử C8H18. (A) tác dụng với chlorine đun nóng chỉ tạo một dẫn xuất monochloro duy nhất. Tên gọi của (A) là
A. octane. B. 2-methylheptane.
C. 2,2-dimethylhexane. D. 2,2,3,3-tetramethylbutane.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là:D
Phương trình phản ứng của 2,2,3,3- tetramethylbutane phản ứng với chlorine:
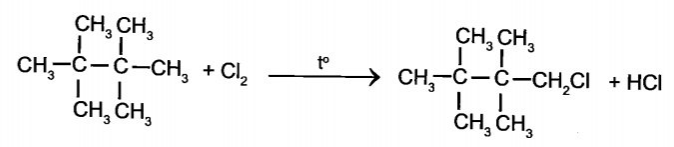
Đáp án đúng là:D
Phương trình phản ứng của 2,2,3,3- tetramethylbutane phản ứng với chlorine:

CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
(A) và (B) là 2 alkyne đồng phân có cùng công thức phân tử C4H6. Phân tích phổ hồng ngoại của (A) được kết quả sau
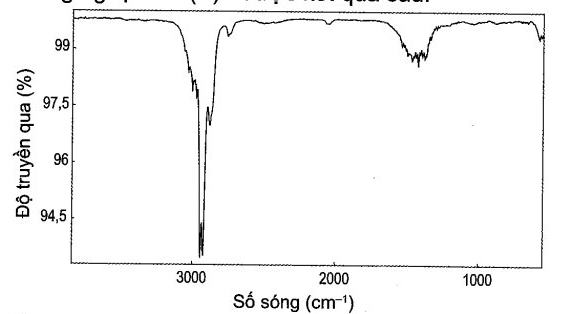
Gọi tên các alkyne (A) và (B) theo danh pháp thay thế
Câu 2:
Arene (B) có công thức phân tử C8H8. Khi có mặt bột sắt, (B) tác dụng với bromine tạo một sản phẩm thế monobromo duy nhất, số công thức cấu tạo phù hợp với (B) là
A. 3. B. 4. C. 1. D. 2.
Arene (B) có công thức phân tử C8H8. Khi có mặt bột sắt, (B) tác dụng với bromine tạo một sản phẩm thế monobromo duy nhất, số công thức cấu tạo phù hợp với (B) là
A. 3. B. 4. C. 1. D. 2.
Câu 4:
Quan sát biểu đồ thể hiện nhiệt độ sôi của 6 alkane đầu tiên.
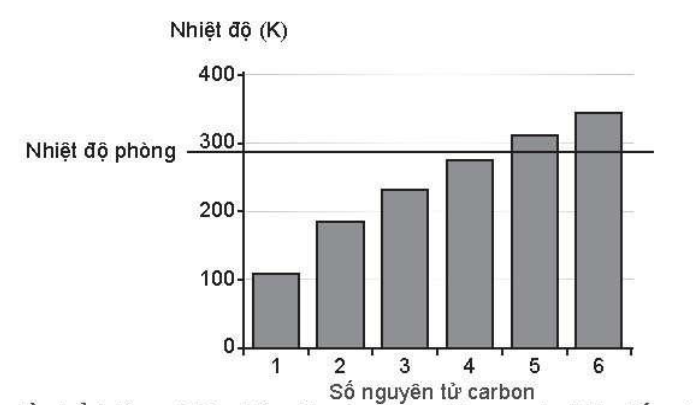
▲ Biểu đồ thể hiện nhiệt độ sôi của cac alkane từ CH4
a) Có bao nhiêu alkane ở thể khí trong điều kiện thường?
b) Giải thích tại sao neopentane cũng ở thể khí trong điều kiện thường.
c) Cho biết ưu điểm và nhược điểm của propane và butane khi sử dụng chúng làm khí hoá lỏng?
Quan sát biểu đồ thể hiện nhiệt độ sôi của 6 alkane đầu tiên.

▲ Biểu đồ thể hiện nhiệt độ sôi của cac alkane từ CH4
a) Có bao nhiêu alkane ở thể khí trong điều kiện thường?
b) Giải thích tại sao neopentane cũng ở thể khí trong điều kiện thường.
c) Cho biết ưu điểm và nhược điểm của propane và butane khi sử dụng chúng làm khí hoá lỏng?
Câu 5:
a) Gọi tên hydrocarbon sau theo danh pháp thay thế:
CH≡C-CH2-CH=CH2
b) Khi cho hydrocarbon trên tác dụng với bromine trong CCl4 ở -20 °C thu được 4,5-dibromopent-1-yne theo phương trình phản ứng:
4,5-dibromopent-1 -yne
Nhận xét về tốc độ phản ứng cộng bromine vào liên kết đôi và liên kết ba. Rút ra kết luận.
a) Gọi tên hydrocarbon sau theo danh pháp thay thế:
CH≡C-CH2-CH=CH2
b) Khi cho hydrocarbon trên tác dụng với bromine trong CCl4 ở -20 °C thu được 4,5-dibromopent-1-yne theo phương trình phản ứng:
4,5-dibromopent-1 -yne
Nhận xét về tốc độ phản ứng cộng bromine vào liên kết đôi và liên kết ba. Rút ra kết luận.
Câu 6:
Cục Quản Lí Thực Phẩm và Dược Phẩm Hoa Kì (FDA) đã công nhận ethylene là an toàn trong việc kích thích trái cây mau chín. Tuy nhiên khi vượt quá nồng độ cho phép, ví dụ đối với nồng độ 27 000 ppm, tức gấp khoảng 200 lần mức cần thiết để kích thích quá trình chín, một tia lửa điện có thể đốt cháy ethylene và gây ra vụ nổ chết người.
Trong phòng ủ chín, ethylene được sử dụng ở nồng độ 100 ppm-150 ppm. Khối lượng ethylene cần thiết sử dụng để phòng ủ chín có thể tích 50m3 đạt nồng độ 140 ppm ở 25oC và 1 bar là bao nhiêu?
Cục Quản Lí Thực Phẩm và Dược Phẩm Hoa Kì (FDA) đã công nhận ethylene là an toàn trong việc kích thích trái cây mau chín. Tuy nhiên khi vượt quá nồng độ cho phép, ví dụ đối với nồng độ 27 000 ppm, tức gấp khoảng 200 lần mức cần thiết để kích thích quá trình chín, một tia lửa điện có thể đốt cháy ethylene và gây ra vụ nổ chết người.
Trong phòng ủ chín, ethylene được sử dụng ở nồng độ 100 ppm-150 ppm. Khối lượng ethylene cần thiết sử dụng để phòng ủ chín có thể tích 50m3 đạt nồng độ 140 ppm ở 25oC và 1 bar là bao nhiêu?
Câu 7:
Giải thích tại sao m-xylene tham gia phản ứng nitro hoá nhanh hơn p-xylene 100 lần.
Giải thích tại sao m-xylene tham gia phản ứng nitro hoá nhanh hơn p-xylene 100 lần.
Câu 8:
Khi đốt cháy 1 mol propane toả ra lượng nhiệt là 2 220 kJ. Để đun nóng 1 gam nước tăng thêm 1°C cần cung cấp nhiệt lượng là 4,2 J. Tính khối lượng propane cần dùng để đun 1 L nước từ 25 °C lên 100 °C. Cho biết 75% nhiệt lượng toả ra khi đốt cháy propane dùng để nâng nhiệt độ của nước. Khối lượng riêng của nước là 1 g/mL.
Khi đốt cháy 1 mol propane toả ra lượng nhiệt là 2 220 kJ. Để đun nóng 1 gam nước tăng thêm 1°C cần cung cấp nhiệt lượng là 4,2 J. Tính khối lượng propane cần dùng để đun 1 L nước từ 25 °C lên 100 °C. Cho biết 75% nhiệt lượng toả ra khi đốt cháy propane dùng để nâng nhiệt độ của nước. Khối lượng riêng của nước là 1 g/mL.
Câu 9:
So sánh điều kiện và khả năng phản ứng thế bromine vào vòng benzene của toluene với anisole (C6H5OCH3). Giải thích.
So sánh điều kiện và khả năng phản ứng thế bromine vào vòng benzene của toluene với anisole (C6H5OCH3). Giải thích.
Câu 10:
Cho các alkene sau: CH2=CH-CH3; (CH3)2C=C(CH3)2; CH3CH=CHCH3 và CH3CH=CHC2H5. Số alkene có đồng phân hình học là
A. 2. B. 4. C. 1. D. 3.
Cho các alkene sau: CH2=CH-CH3; (CH3)2C=C(CH3)2; CH3CH=CHCH3 và CH3CH=CHC2H5. Số alkene có đồng phân hình học là
A. 2. B. 4. C. 1. D. 3.
Câu 11:
Ở các nước Mỹ, Úc và một số quốc gia khác, khí hoá lỏng (LPG - Liquefied Petroleum Gas) được sử dụng nhiều làm nhiên liệu là propane hoá lỏng. Em hãy tính xem một bình khí hoá lỏng chứa 12 kg propane có thể cung cấp bao nhiêu lít khí propane ở 25 °C, 1 bar.
Ở các nước Mỹ, Úc và một số quốc gia khác, khí hoá lỏng (LPG - Liquefied Petroleum Gas) được sử dụng nhiều làm nhiên liệu là propane hoá lỏng. Em hãy tính xem một bình khí hoá lỏng chứa 12 kg propane có thể cung cấp bao nhiêu lít khí propane ở 25 °C, 1 bar.
Câu 12:
Hoá lỏng một alkane ở thể khí là cách để tối ưu hoá khả năng lưu trữ alkane trong các thiết bị. Để hoá lỏng một alkane ở thể khí, người ta có thể tiến hành trong điều kiện nhiệt độ thấp hơn nhiệt độ sôi của alkane. Ví dụ chúng ta có thể hoá lỏng propane ở nhiệt độ thấp hơn -42 °C hay methane xuống thấp hơn nhiệt độ -162 °C.
Tuy nhiên cách làm này rất tốn kém, không đạt hiệu quả kinh tế nên ít được áp dụng, mà thay vào đó người ta hoá lỏng alkane bằng cách nén chúng dưới áp suất cao. Để propane là chất lỏng ở nhiệt độ phòng, propane phải được giữ trong bình ở áp suất khoảng 850 kPa, tức khoảng 8,5 atm. Với methane phải khoảng 32 000 kPa, tức khoảng 320 atm và butane khoảng 230 kPa, tức khoảng 2,3 atm.
a) Alkane nào trong số 3 alkane đã nêu dễ hoá lỏng hơn?
b) Khí hoá lỏng nào trong số 3 khí hoá lỏng trên cần phải lưu trữ trong thiết bị thép cực bền? Vì sao?
Hoá lỏng một alkane ở thể khí là cách để tối ưu hoá khả năng lưu trữ alkane trong các thiết bị. Để hoá lỏng một alkane ở thể khí, người ta có thể tiến hành trong điều kiện nhiệt độ thấp hơn nhiệt độ sôi của alkane. Ví dụ chúng ta có thể hoá lỏng propane ở nhiệt độ thấp hơn -42 °C hay methane xuống thấp hơn nhiệt độ -162 °C.
Tuy nhiên cách làm này rất tốn kém, không đạt hiệu quả kinh tế nên ít được áp dụng, mà thay vào đó người ta hoá lỏng alkane bằng cách nén chúng dưới áp suất cao. Để propane là chất lỏng ở nhiệt độ phòng, propane phải được giữ trong bình ở áp suất khoảng 850 kPa, tức khoảng 8,5 atm. Với methane phải khoảng 32 000 kPa, tức khoảng 320 atm và butane khoảng 230 kPa, tức khoảng 2,3 atm.
a) Alkane nào trong số 3 alkane đã nêu dễ hoá lỏng hơn?
b) Khí hoá lỏng nào trong số 3 khí hoá lỏng trên cần phải lưu trữ trong thiết bị thép cực bền? Vì sao?
Câu 13:
(H) và (K) là 2 hydrocarbon có cùng công thức phân tử C10H14 và đều không làm mất màu nước bromine, nhưng cả hai chất này đều làm mất màu dung dịch thuốc tím đã được acid hoá (ví dụ dung dịch KMnO4 trong H2SO4), trong đó (H) tạo terephthalic acid là sản phẩm hữu cơ duy nhất, (K) tạo 2 sản phẩm hữu cơ là terephthalic acid và chất (X). Xác định công thức cấu tạo của (H), (K), (X) và viết các phương trình phản ứng xảy ra.
(H) và (K) là 2 hydrocarbon có cùng công thức phân tử C10H14 và đều không làm mất màu nước bromine, nhưng cả hai chất này đều làm mất màu dung dịch thuốc tím đã được acid hoá (ví dụ dung dịch KMnO4 trong H2SO4), trong đó (H) tạo terephthalic acid là sản phẩm hữu cơ duy nhất, (K) tạo 2 sản phẩm hữu cơ là terephthalic acid và chất (X). Xác định công thức cấu tạo của (H), (K), (X) và viết các phương trình phản ứng xảy ra.