Trắc nghiệm tổng hợp Hóa 10 Chủ đề 5: Năng lượng hóa học có đáp án
Trắc nghiệm Hóa 10 Dạng 3. Tính biến thiên enthalpy phản ứng theo năng lượng liên kết có đáp án
-
985 lượt thi
-
12 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
21/07/2024Cho phản ứng hóa học sau:
CH4 (g) + Cl2 (g) → CH3Cl (g) + HCl (g)
Biết năng lượng liên kết (kJmol-1) trong các chất cho ở bảng sau:
|
C – H |
Cl – Cl |
C – Cl |
H – Cl |
|
414 |
243 |
339 |
431 |
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
\[{\Delta _r}H_{298}^0 = 1 \times {E_b}(C{H_4}) + 1 \times {E_b}(C{l_2}) - 1 \times {E_b}(C{H_3}Cl) - 1 \times {E_b}(HCl)\]
= 1 × 4EC – H + 1 × ECl – Cl – 1 × (3EC – H + EC – Cl) – 1 × EH – Cl
= 1 × 4 × 414 + 1 × 243 - 1×(3×414 + 339) - 1×431 = -113 (kJ).
Câu 2:
23/07/2024Cho phản ứng hóa học sau:
3H2 (g) + N2 (g) → 2NH3 (g)
Biết năng lượng liên kết (kJmol-1) trong các chất như sau:
|
H – H |
N ≡ N |
N – H |
|
432 |
945 |
391 |
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
\[{\Delta _r}H_{298}^0 = 3 \times {E_b}({H_2}) + {E_b}({N_2}) - 2 \times {E_b}(N{H_3})\]
= 3 × Eb (H – H) + Eb (N ≡ N) – 2 × 3 × Eb (N – H)
= 3 × 432 + 945 - 2 × 3 × 391 = -105 kJ.
Câu 3:
22/07/2024Cho phản ứng sau:
H2 (g) + Cl2 (g) → 2HCl (g)
Biến thiên enthalpy chuẩn của phản ứng là
Biết: Eb (H – H) = 436 kJ/mol, Eb (Cl – Cl) = 243 kJ/mol, Eb (H – Cl) = 432 kJ/ mol.
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Biến thiên enthalpy chuẩn của phản ứng là:
\[\begin{array}{l}{\Delta _r}H_{298}^0 = {E_b}_{(H - H)} + {E_{b(Cl - Cl)}} - 2{E_{b(H - Cl)}}\\ = 436 + 243 - 2.432 = - 185(kJ).\end{array}\]
Câu 4:
23/07/2024Cho phản ứng hóa học sau:
2H2(g) + O2(g) 2H2O(g)
Biến thiên enthalpy chuẩn của phản ứng là
Biết: Eb(H-H) = 432 kJ/mol; Eb(O=O) = 498 kJ/mol; Eb(O-H) = 467 kJ/mol.
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Biến thiên enthalpy chuẩn của phản ứng là:
\({\Delta _r}H_{298}^o = {\rm{ }}2.{E_b}\left( {{H_2}} \right){\rm{ }} + {\rm{ }}{E_b}\left( {{O_2}} \right){\rm{ }}--{\rm{ }}2.{E_b}\left( {{H_2}O} \right)\)
= 2.Eb(H-H) + Eb(O=O) – 2.2.Eb(O-H) = 2.432 + 498 – 2.2.467 = -506 (kJ).
B đúng.
* Tính biến thiên enthalpy phản ứng theo enthalpy tạo thành:
- Giả sử có phản ứng tổng quát:
aA + bB mM + nN
- Biến thiên enthalpy chuẩn phản ứng của phản ứng được tính theo công thức:
Δr = m× Δf(M) + n× Δf(N) - a× Δf(A) - b× Δf(B)
Trong đó: A, B, M, N là các chất trong phản ứng; a, b, m, n là hệ số tương ứng của các chất.
- Chú ý: Enthalpy tạo thành chuẩn của đơn chất bằng 0.
Ví dụ 1: Cho phản ứng: 2Na2O(s) 4Na(s) + O2(g)
Biến thiên enthalpy chuẩn phản ứng của phản ứng được tính như sau:
Δr = 4× Δf(Na(s)) + 1× Δf(O2(g)) - 2× Δf(Na2O(s))
= 4×0 + 1×0 - 2× (- 418,0) = 836,0 (kJ)
Do Δrcủa phản ứng rất dương nên phản ứng thu nhiệt.
Ví dụ 2: Biến thiên enthalpy của phản ứng đốt cháy hoàn toàn 1 mol C2H6(g) được tính như sau:
C2H6(g) + O2(g) 2CO2(g) + 3H2O(l)
Δr= 2×Δf(CO2(g)) + 3×Δf(H2O(l)) - 1×Δf(C2H6(s)) - ×ΔfO2(g))
= 2×(- 393,5) + 3×(- 285,8) - 1×(- 84) - ×0 = -1560,4 (kJ)
Do Δrủa phản ứng rất âm nên phản ứng tỏa nhiệt mạnh, rất thuận lợi và cung cấp nhiều năng lượng.
Xem thêm một số tài liệu liên quan hay, chi tiết khác:
Lý thuyết Hóa học 10 Bài 15 (Cánh diều): Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
Giải SGK Hóa lớp 10 Bài 15 (Cánh diều): Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
Câu 5:
14/07/2024Cho phản ứng hóa học sau:
C7H16(g) + 11O2(g) 7CO2(g) + 8H2O(g)
Biến thiên enthalpy chuẩn của phản ứng là
Biết: Eb(C-C) = 347 kJ/mol; Eb(C-H) = 413 kJ/mol; Eb(O=O) = 498 kJ/mol; Eb(C=O) = 745 kJ/mol; Eb(O-H) = 467 kJ/mol.
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Biến thiên enthalpy chuẩn của phản ứng là
\({\Delta _r}H_{298}^o = {\rm{ }}{E_b}\left( {{C_7}{H_{16}}} \right){\rm{ }} + {\rm{ }}11.{E_b}\left( {{O_2}} \right){\rm{ }}--{\rm{ }}7.{E_b}\left( {C{O_2}} \right){\rm{ }}--{\rm{ }}8.{E_b}\left( {{H_2}O} \right)\)
= 6.Eb(C-C) + 16Eb(C-H) + 11.Eb(O=O) – 7.2.Eb(C=O) – 8.2.Eb(O-H)
= 6.347 + 16.413 + 11.498 – 7.2.745 – 8.2.467 = -3734 kJ.
Câu 6:
06/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
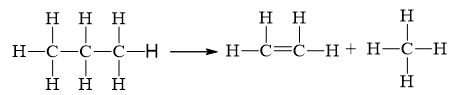
\({\Delta _r}H_{298}^o = 2.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}C} \right)}{\rm{ }} + {\rm{ }}8.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}H} \right)} - 1.{E_b}_{\left( {C{\rm{ }} = {\rm{ }}C} \right)}{\rm{ - }}8.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}H} \right)}\)
= 2.346 + 8.418 - 1.612 - 8.418 = +80 kJ.
Câu 7:
16/07/2024Cho phản ứng hóa học sau:
H2C=CH2(g) + H2(g) → H3C-CH3(g)
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
|
Liên kết |
C – H |
C – C |
C = C |
H - H |
|
Eb (kJ/mol) |
418 |
346 |
612 |
436 |
Biến thiên enthalpy chuẩn của phản ứng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
\({\Delta _r}H_{298}^o = {\rm{ }}{E_{C = C}} + {\rm{ }}4.{E_{C - H}} + {\rm{ }}{E_{H - H}}--{\rm{ }}{E_{C - C}}--{\rm{ }}6{E_{C - H}}\)
= EC=C + EH-H – EC-C – 2EC-H = 612 + 436 – 346 – 2.418 = -134 (kJ).
Câu 8:
15/07/2024Cho phản ứng tạo thành propene từ propyne:
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
|
Liên kết |
C – H |
C – C |
C = C |
C ≡ C |
H - H |
|
Eb (kJ/mol) |
413 |
347 |
614 |
839 |
432 |
Biến thiên enthalpy chuẩn của phản ứng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
\[{\Delta _r}H_{298}^0 = {E_b}_{\left( {C \equiv C} \right)} + {E_b}_{\left( {C - C} \right)} + 4.{E_b}_{\left( {C - H} \right)} + {E_b}_{\left( {H - H} \right)} - {E_b}_{\left( {C = C} \right)} - {E_b}_{\left( {C - C} \right)} - 6.{E_b}_{\left( {C - H} \right)}\]
= Eb (C≡C) – Eb(C=C) + Eb(H-H) – 2Eb(C-H)
= 839 – 614 + 432 – 2.413 = -169 kJ.
Câu 9:
15/07/2024Cho phản ứng đốt cháy octane như sau:
C8H18 (g) + \[\frac{{25}}{2}{O_2}(g)\]→ 8CO2 (g) + 9H2O (l) \[{\Delta _r}H_{298}^0 = - 5030\,kJ\]
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
|
Liên kết |
C – H |
C – C |
O = O |
C = O |
H - O |
|
Eb (kJ/mol) |
414 |
347 |
498 |
799 |
x |
Giá trị của x là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Ta có:
\[{\Delta _r}H_{298}^0 = {E_b}({C_8}{H_{18}}) + \frac{{25}}{2}{E_b}({O_2}) - 8{E_b}(C{O_2}) - 9{E_b}({H_2}O)\]\[ \Leftrightarrow - 5030 = {\rm{ }}7{E_{C - C}} + {\rm{ }}18{E_{C{\rm{ }}--{\rm{ }}H}} + \frac{{25}}{2}{E_{O = O}} - 8.2.{E_{C = O}} - 9.2.{E_{O - H}}\]
\[ \Leftrightarrow - 5030 = {\rm{ }}7.347{\rm{ }} + {\rm{ }}18.414{\rm{ }} + \frac{{25}}{2}.498 - 16.799 - 18x\]
Þ x = 464
Câu 10:
22/07/2024Cho phản ứng tổng quát: aA + bB → mM + nN. Hãy chọn phương án tính đúng \[{\Delta _r}H_{298}^o\] của phản ứng:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
- Cách tính enthalpy của phản ứng hoá học dựa vào năng lượng liên kết:
\[{\Delta _r}H_{298}^0 = \sum\limits_{}^{} {{E_b}} \left( {c{\rm{d}}} \right) - \sum\limits_{}^{} {{E_b}\left( {sp} \right)} \]
Hay \[{\Delta _r}H_{298K}^o = a \times {E_b}\left( A \right) + b \times {E_b}\left( B \right) - m \times {E_b}\left( M \right) - n \times {E_b}\left( N \right)\]
- Cách tính enthalpy của phản ứng hoá học dựa vào enthalpy tạo thành:
\[{\Delta _r}H_{298}^0 = \sum\limits_{}^{} {{\Delta _f}H_{298}^0} \left( {sp} \right) - \sum\limits_{}^{} {{\Delta _f}H_{298}^0\left( {cd} \right)} \]
Hay \[{\Delta _r}H_{298K}^o = m \times {\Delta _f}H_{298}^o\left( M \right) + n \times {\Delta _f}H_{298}^o\left( N \right) - a \times {\Delta _f}H_{298}^o\left( A \right) - b \times {\Delta _f}H_{298}^o\left( B \right)\]
Câu 11:
23/07/2024Phosgene (COCl2) được điều chế bằng cách cho hỗn hợp CO và Cl2 đi qua than hoạt tính. Biết ở điều kiện chuẩn: Eb(Cl-Cl) = 243 kJ/mol; Eb(C-Cl) = 339 kJ/mol; Eb(C=O) = 745 kJ/mol; Eb(C ≡ O) = 1075 kJ/mol. Biến thiên enthalpy chuẩn của phản ứng tạo thành phosgene từ CO và Cl2 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Áp dụng công thức:
\[{\Delta _r}H_{298}^0 = {E_b}(CO) + {E_b}(C{l_2}) - {E_b}(COC{l_2})\]
= EC≡O + ECl – Cl – EC=O – 2EC – Cl
= 1075 + 243 – 745 – 2.339 = - 105 kJ.
Câu 12:
15/07/2024Cho phương trình hóa học của phản ứng:
\[{C_2}{H_4}\left( g \right) + {H_2}O\left( l \right) \to {C_2}{H_5}OH\left( l \right)\]
Công thức tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành chuẩn của các chất là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Phản ứng: \[{C_2}{H_4}\left( g \right) + {H_2}O(l){\rm{ }} \to {C_2}{H_5}OH\left( l \right)\]
Biến thiên enthalpy của phản ứng tính theo nhiệt tạo thành chuẩn:
\[{\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0\left( {{C_2}{H_5}OH} \right){\rm{ }} - {\Delta _f}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ }} - {\Delta _f}H_{298}^0\left( {{H_2}O} \right)\]
Bài thi liên quan
-
Trắc nghiệm Hóa 10 Dạng 1. Câu hỏi lí thuyết Năng lượng hóa học có đáp án
-
25 câu hỏi
-
45 phút
-
-
Trắc nghiệm Hóa 10 Dạng 2. Tính biến thiên enthalpy phản ứng theo enthalpy tạo thành có đáp án
-
11 câu hỏi
-
45 phút
-
Có thể bạn quan tâm
Các bài thi hot trong chương
- Trắc nghiệm tổng hợp Hóa 10 Chủ đề 6: Tốc độ phản ứng hóa học có đáp án (5867 lượt thi)
- Trắc nghiệm tổng hợp Hóa 10 Chủ đề 1: Cấu tạo nguyên tử có đáp án (1150 lượt thi)
- Trắc nghiệm tổng hợp Hóa 10 Chủ đề 4: Phản ứng oxi hóa - khử có đáp án (977 lượt thi)
- Trắc nghiệm tổng hợp Hóa 10 Chủ đề 3: Liên kết hóa học có đáp án (932 lượt thi)
- Trắc nghiệm tổng hợp Hóa 10 Chủ đề 2: Bảng tuần hoàn các nguyên tố hóa học có đáp án (783 lượt thi)
- Trắc nghiệm tổng hợp Hóa 10 Chủ đề 7: Nguyên tố nhóm VIIA (Nhóm halogen) có đáp án (764 lượt thi)
