160 Bài trắc nghiệm Ôn thi THPTQG Hóa Học cực hay có lời giải chi tiết
160 Bài trắc nghiệm Ôn thi THPTQG Hóa Học cực hay có lời giải chi tiết ( đề 1)
-
378 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
26/06/2024Tơ nilon-6,6 có tính dai, bền, mềm mại, óng mượt được dùng để dệt vải may mặc. Nilon-6,6 thuộc loại:
 Xem đáp án
Xem đáp án
Công thức của tơ Nilon-6,6 là:
![]()
Nilon – 6,6 có nhiều nhóm -NHCO- => Nilon – 6,6 thuộc loại tơ poliamit.
Đán án B.
Câu 2:
20/07/2024Chất X có công thức cấu tạo CH3CH2COOCH3. Tên gọi của X là:
 Xem đáp án
Xem đáp án
CH3CH2COOCH3: metyl propionat.
Đáp án D.
Câu 3:
23/07/2024Thủy phân 8,8 gam etyl axetat bằng 200 ml dung dịch NaOH 0,2M.Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch, thu được m gam chất rắn khan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Số mol các chất là:
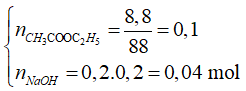
Phương trình phản ứng: CH3COOC2H5 + NaOH CH3COONa + C2H5OH
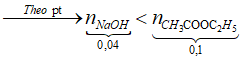 => NaOH hết, CH3COOC2H5 dư
=> NaOH hết, CH3COOC2H5 dư
=> Chất rắn thu được chỉ có CH3COONa
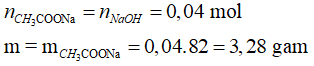
Đáp án D.
Câu 4:
21/07/2024Từ 16,20 tấn xenlulozơ người ta sản xuất được m tấn xenlulozơ trinitrat. Biết hiệu suất phản ứng tính theo xenlulozơ là 90%. Giá trị của m là:
 Xem đáp án
Xem đáp án
Phương trình phản ứng:
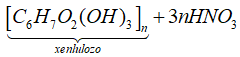
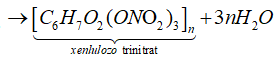
Lấy hệ số polime hóa n = 1.
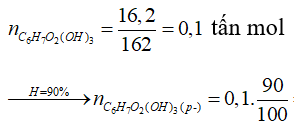 tấn mol
tấn mol
![]() tấn mol
tấn mol
![]() = 26,73 tấn mol
= 26,73 tấn mol
Đáp án A.
Câu 5:
19/07/2024Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy không tác dụng với H2O tạo thành dung dịch bazơ là:
 Xem đáp án
Xem đáp án
Các kim loại tác dụng với nước tạo thành dung dịch bazơ gồm: Na, Ca, K
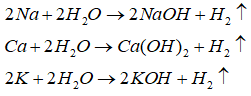
Các kim loại không tác dụng với H2O tạo thành dung dịch bazơ gồm: Fe, Cu.
Đáp án A.
Câu 6:
02/07/2024H2SO4 đặc được dùng để làm khô khí ẩm nào sau đây?
 Xem đáp án
Xem đáp án
H2SO4 đặc là chất có tính oxi hóa mạnh và có tính axit => H2SO4 không được dùng để làm khô khí có tính khử và tính bazơ.
H2SO4 đặc không được dùng để làm khô các khí H2S, HBr, HI vì:
H2S + 3H2SO4(đặc) .. 4SO2 + 4H2O
2HBr + H2SO4(đặc) Br2 + SO2 + 2H2O
8HI + H2SO4(đặc) 4I2 + H2S + 4H2O
H2SO4 đặc được dùng để làm khô khí CO2.
Đáp án B.
Câu 7:
29/06/2024Ứng dụng nào dưới đây không phải là ứng dụng của glucozơ?
 Xem đáp án
Xem đáp án
Glucozơ không được dùng làm nguyên liệu để sản xuất PVC.
Đáp án B.
Câu 8:
22/07/2024Muối mononatri của amino axit nào sau đây được dùng làm bột ngọt (mì chính)?
 Xem đáp án
Xem đáp án
Muối mononatri của axit glutamic được dùng làm bột ngọt (mì chính).
Đáp án C
Câu 9:
17/07/2024Cá cần oxi để tăng trưởng tốt.Chúng không thể nào tăng trưởng tốt nếu nước quá ấm. Lí do cho hiện tượng trên là:
 Xem đáp án
Xem đáp án
Cá cần oxi để hô hấp, lượng oxi dùng để cho cá hô hấp chính là lượng oxi tan trong nước (khí oxi tan ít trong nước)
Độ tan của chất khí nói chung và của oxi nói riêng giảm khi nhiệt độ tăng, do đó với nước ấm oxi hòa tan sẽ kém hơn nước lạnh
Đáp án B.
Câu 10:
20/07/2024Cho các phát biểu sau:
(a) Chất béo nhẹ hơn nước, không tan trong nước nhưng tan trong các dung môi hữu cơ không phân cực.
(b) Chất béo là trieste của glixerol với các axit béo.
(c) Phản ứng thủy phân chất béo trong môi trường kiềm là phản ứng thuận nghịch.
(d) Tristearin có nhiệt độ nóng chảy cao hơn nhiệt độ nóng chảy của triolein
Số phát biểu đúng là:
 Xem đáp án
Xem đáp án
Chất béo nhẹ hơn nước, không tan trong nước nhưng tan trong các dung môi hữu cơ không phân cực => Phát biểu (a) đúng
Chất béo là trieste của glixerol với các axit béo => Phát biểu (b) đúng
Thủy phân chất béo trong môi trường kiềm là phản ứng bất thuận nghịch
![]()
![]()

![]()
![]()
![]()
=> Nhiệt độ nóng chảy: tristearin > triolein =>Phát biểu (d) đúng
Các phát biểu đúng là (a), (b) và (d).
Đáp án C.
Câu 11:
27/06/2024Cho dãy các chất sau: glucozơ, amilopectin,fuctozơ, saccarozơ,xelulozơ. Số chất trong dãy tham gia phản ứng thủy phân là:
 Xem đáp án
Xem đáp án
Các chất hữu cơ tham gia phản ứng thủy phân gồm:
Các hợp chất hữu cơ chứa chức este. Thí dụ:
![]()
![]()
![]()
![]()
Đissaccarit, polisaccarit tham gia phản ứng thủy phân khi có xúc tác axit hoặc enzim. Thí dụ:
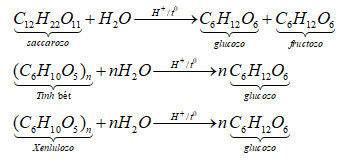
Các hợp chất hữu cơ có nhóm –CO-NH- như peptit, protein, nilon-6, nilon-6,6...
Các chất tham gia phản ứng thủy phân gồm (C6H10O5)n (amilopectin), C12H22O11 (saccarozo), (C6H10O5)n (xenlulozo)
Đáp án C.
Câu 12:
22/07/2024Cho C2H4(OH)2 phản ứng với hỗn hợp CH3COOH và HCOOH trong môi trường axit (H2SO4) thu được tối đa số đieste là:
 Xem đáp án
Xem đáp án
Các este thuần chức (chỉ chứa chức este) thỏa mãn là:
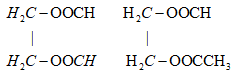

Vậy có 3 este thỏa mãn.
Đáp án A.
Câu 13:
07/07/2024Cho hỗn hợp X gồm Al, Fe, Cu. Dung dịch nào sau đây (khi lấy dư) không thể hòa tan hết X?
 Xem đáp án
Xem đáp án
X tan hết trong dung dịch HNO3 loãng dư:
Al + 4HNO3 (loãng) Al(NO3)3 + NO![]() + 2H2O
+ 2H2O
Fe + 4HNO3 (loãng) Fe(NO3)3 + NO![]() + 2H2O
+ 2H2O
3Cu + 8HNO3 (loãng) 3Cu(NO3)2 + 2NO![]() + 4H2O
+ 4H2O
X tan hết trong dung dịch NaNO3 và HCl dư:
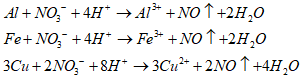
X tan hết trong H2SO4 đặc, nóng dư:
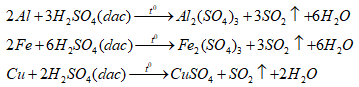
X không tan hết trong dung dịch H2SO4 loãng, nóng, dư vì Cu là kim loại đứng sau hidro trong dãy điện hóa nên không tác dụng với dung dịch H2SO4 loãng:
2Al + 3H2SO4 (loãng) Al2(SO4)3 + 3H2![]()
Fe + H2SO4 (loãng) ![]() FeSO4 + H2
FeSO4 + H2![]()
Cu + H2SO4 (loãng) không xảy ra
Chú ý: Al, Fe, Cu bị thụ động trong H2SO4 đặc nguội và HNO3 đặc nguội, tức là Al, Fe, Cr không tác dụng với H2SO4 đặc nguội và HNO3 đặc nguội.
Đáp án D.
Câu 15:
11/07/2024Cho NaOH dư phản ứng với các dung dịch sau: AlCl3, Ba(HCO3), CuSO4, HCl, NH4Cl, MgSO4, FeCl3. Sau khi các phản ứng kết thúc, số trường hợp thu được kết tủa là:
 Xem đáp án
Xem đáp án
Đối với dung dịch AlCl3: AlCl3 + 3NaOH Al(OH)3 + 3NaCl
Al(OH)3 + NaOH NaAlO2 + 2H2O
Đối với dung dịch Ba(HCO3)2: Ba(HCO3)2 + 2NaOH BaCO3 + Na2CO3 + 2H2O
Đối với dung dịch CuSO4: CuSO4 + 2NaOH Cu(OH)2+ Na2SO4
Đối với dung dịch HCl: HCl + NaOH NaCl + H2O
Đối với dung dịch NH4Cl: NH4Cl + NaOH NaCl + NH3 + H2O
Đối với dung dịch MgSO4: MgSO4 + 2NaOH Mg(OH)2+ Na2SO4
Đối với dung dịch FeCl3: FeCl3 + 3NaOH Fe(OH)3+ 3NaCl
Các dung dịch thu được kết tủa khi tác dụng với dung dịch NaOH dư gồm: Ba(HCO3)2, CuSO4, MgSO4, FeCl3.
Đáp án D.
Câu 16:
12/07/2024Sục 13,44 lít (đktc) khí CO2 vào 200ml dung dịch X gồm Ba(OH)2 1,5M và NaOH 1M, sau các phản ứng thu được dung dịch Y. Cho dung dịch Y tác dụng với 200ml dung dịch hỗn hợp BaCl2 1,2M và KOH 1,5M, thu được m gam kết tủa. Giá trị của m là:
 Xem đáp án
Xem đáp án
*Xét giai đoạn CO2 tác dụng với dung dịch X:
Số mol CO2 là: ![]()
Số mol các chất và ion trong dung dịch X là:
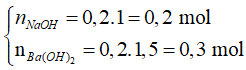
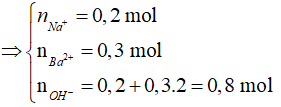
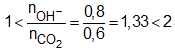
=> tạo 2 muối là ![]()
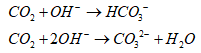
![]()
![]()
![]()
![]()
Phản ứng tạo kết tủa: 
![]()
![]()
=> Dung dịch Y gồm: Na+ (0,2 mol); Ba2+ (0,1 mol); HCO3- (0,4 mol)
*Dung dịch Y tác dụng với dung dịch hỗn hợp BaCl2 và KOH:
Số mol các chất và ion là:

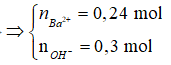
Các phương trình phản ứng:

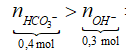
![]()
![]()
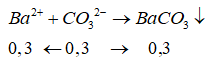
![]()
![]()
![]()
![]()
Đáp án D.
Câu 17:
15/07/2024Cho dãy các chất: NaOH, NaCl, Cu, HCl, NH3, Zn, Cl2, AgNO3. Số chất tác dụng được với dung dịch Fe(NO3)2 là:
 Xem đáp án
Xem đáp án
Các chất và dung dịch tác dụng với dung dịch Fe(NO3)2 gồm NaOH, HCl, NH3, Zn, Cl2 và AgNO3:
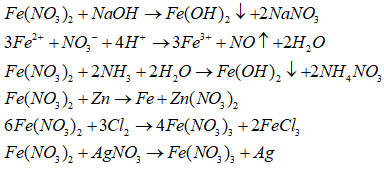
Đáp án D.
Câu 18:
03/07/2024Đốt cháy hoàn toàn 11,88 gam X gồm hai este mạch hở (trong đó có một este đơn chức và một este hai chức) cần 14,784 lít O2 (đktc), thu được 25,08 gam CO2. Đun nóng 11,88 gam X với 300ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thu được chất rắn Y và phần hơi chỉ chứa một ancol đơn chức Z. Cho Z vào bình Na dư, sau phản ứng thấy khối lượng bình Na tăng 5,85 gam. Trộn Y với CaO rồi nung trong điều kiện không có không khí, thu được 2,016 lít (đktc) một hiđrocacbon duy nhất. Biết các phản ứng xảy ra hoàn toàn. Phần trăm theo khối lượng của este hai chức trong hỗn hợp X là:
 Xem đáp án
Xem đáp án
*Xét giai đoạn đốt cháy X:
Số mol các chất là: 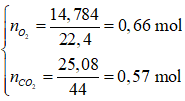
Sơ đò phản ứng: 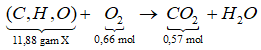
![]()
![]()
![]()
![]()
![]()

*Xét giai đoạn X tác dụng với dung dịch NaOH:
Số mol NaOH là: ![]()
Sơ đồ phản ứng: ![]()
![]() => X hết, Na dư => Y gồm –COONa và NaOH dư
=> X hết, Na dư => Y gồm –COONa và NaOH dư
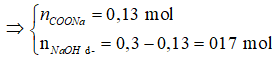
*Xét giai đoạn Z tác dụng với Na dư:
Z đơn chức => Đặt công thức của Z là ROH ![]()
Sơ đồ phản ứng: ![]()
![]()
![]()
![]()
![]()
![]()
![]()
*Xét giai đoạn nung Y với CaO:
Số mol hidrocacbonat thu được là: ![]()
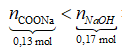 => COONa hết, NaOH dư
=> COONa hết, NaOH dư
Đặt công thức và số mol các muối trong Y là: RCOONa: a mol; R’(COONa)2: b mol
Phương trinhg phản ứng:
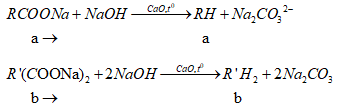
Do thu được một hidrocacbonat => R = R' + 1
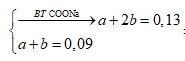
![]()
![]()
![]()
![]()
![]()
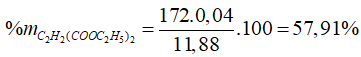
Đáp án C.
Câu 19:
16/07/2024Trong các chất: striren, axit acrylic, axit axetic, vinylaxetilen và butan. Số chất có khả năng tham gia phản ứng cộng hiđro (xúc tác Ni, đun nóng) là:
 Xem đáp án
Xem đáp án
C6H5CH=CH2 (stiren), CH2=CHCOOH (axit acrylic), CH3COOH (axit axetic), CH2=CH-C![]() CH (vinylaxetilen), CH3-CH2-CH2-CH3 (butan)
CH (vinylaxetilen), CH3-CH2-CH2-CH3 (butan)
Các chất tham gia phản ứng cộng với H2 (Ni, t0) là: C6H5CH=CH2 (stiren), CH2=CHCOOH (axit acrylic), CH2=CH-CCH (vinylaxetilen)
Đáp án D.
Câu 20:
21/07/2024Cho 21 gam hỗn hợp glyxin và axit axetic tác dụng vừa đủ với dung dịch KOH, thu được dung dịch X chứa 32,4 gam muối. Cho X tác dụng với dung dịch HCl dư, thu được dung dịch chứa m gam muối. Giá trị của m là:
 Xem đáp án
Xem đáp án
*Xét giai đoạn hỗn hợp ban đầu tác dụng vừa đủ với dung dịch KOH:
Sơ đồ phản ứng: 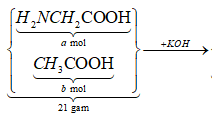

![]() => x = 0,3 mol
=> x = 0,3 mol
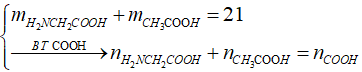
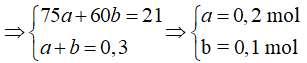
*Coi hỗn hợp ban đầu và KOH đồng thời phản ứng với dung dịch HCl dư:
Sơ đồ phản ứng:
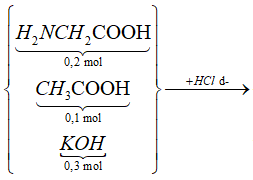
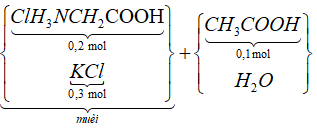
![]()
![]()
Đáp án C.
Câu 21:
22/07/2024Cho dãy chuyển hóa: . Biết X1, X2 là các chất hữu cơ. Công thức cấu tạo thu gọn của X2 là:
 Xem đáp án
Xem đáp án
Sơ đồ phản ứng:
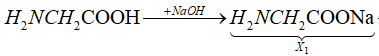
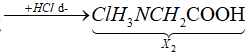
Các phương trình phản ứng:
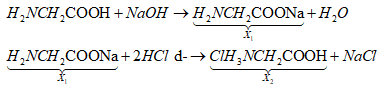
Đáp án A.
Câu 22:
23/07/2024Hỗn hợp X gồm hai chất hữu cơ mạch hở (đều chứa C,H,O), trong phân tử mỗi chất có hai nhóm trong số các nhóm –CHO, -COOH, -CH2OH. Đốt cháy hoàn toàn 17,1 gam X thu được 11,2 lít khí CO2 (đktc) và m gam H2O. Cho 17,1 gam X tác dụng hết với Na dư, thu được 2,8 lít H2 (đktc). Mặt khác cho 17,1 gam X phản ứng hoàn toàn với lượng dư AgNO3/NH3 dư thu được 54 gam Ag. Gía trị của m là:
 Xem đáp án
Xem đáp án
*Xét giai đoạn X tác dụng với AgNO3/NH3:
Số mol Ag thu được là: ![]()
Mỗi chất trong X có hai nhóm chức => Các chất trong X là HCHO
![]()
Sơ đồ phản ứng:
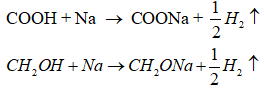
![]()
![]()
*Xét giai đoạn đốt cháy X:
Số mol CO2 thu được là: 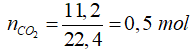
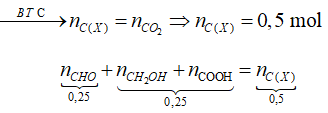
=> X gồm OHC – CH2OH và OHC – COOH
Đặt số mol các chất trong X là: OHC – CH2OH: a mol; OHC – COOH: b mol. Ta có:
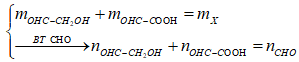
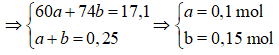
*Sơ đồ phản ứng đốt cháy X: 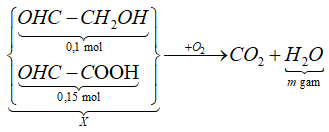
![]()
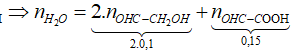
![]()
Đáp án B.
Câu 23:
22/07/2024Tiến hành các thí nghiệm sau:
(a) Sục khí Cl2 vào dung dịch NaOH ở điều kiện thường.
(b) Hấp thụ hết 2 mol CO2 vào dung dịch chứa 3 mol NaOH.
(c) Cho KMnO4 vào dung dịch HCl đặc dư
(d) Cho CuO vào dung dịch HNO3.
(e) Cho KHS vào dung dịch NaOH vừa đủ.
Số thí nghiệm thu được hai muối là:
 Xem đáp án
Xem đáp án
![]()
=> Thí nghiệm (a) thu được hai muối là NaCl và NaClO
![]() => Tạo hai muối NaHCO3, Na2CO3.
=> Tạo hai muối NaHCO3, Na2CO3.
![]()
![]()
=>. Thí nghiệm (c) thu được hai muối là MnCl2 và KCl
![]()
=> Thí nghiệm (d) thu được một muối là Cu(NO3)2.
![]()
=> Dung dịch thu được gồm: Na+, K+, S2-
=> Thí nghiệm (e) thu được hai muối là Na2S và K2S.
Các thí nghiệm thu được hai muối là: (a), (b), (c), (e).
Đáp án D.
Câu 24:
21/07/2024Cho các phát biểu sau:
(a) Fructozơ và saccarozơ đều là chất rắn, vị ngọt, dễ tan trong nước.
(b) Tinh bột và xenlulozơ là polisaccarit, khi đun với dung dịch H2SO4 loãng thì sản phẩm thu được đều có phản ứng tráng bạc.
(c) Dung dịch glucozơ và dung dịch saccarozơ đều hòa tan Cu(OH)2 tạo phức màu xanh lam.
(d) Khi thủy phân hoàn toàn hỗn hợp gồm xenlulozơ và saccarozơ trong môi trường axit, chỉ thu được một loại monosaccarit duy nhất.
(e) Glucozơ bị oxi hóa bởi dung dịch AgNO3 trong amoniac.
(f) Glucozơ tác dụng với H2 (xúc tác Ni, đun nóng) thu được sobitol.
Số phát biểu đúng là:
 Xem đáp án
Xem đáp án
Fructozơ và saccarozơ đều là chất rắn, vị ngọt, dễ tan trong nước.=> Phát biểu (a) đúng.
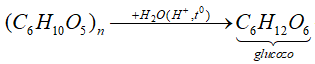
![]()
(C6H10O5)n là polisaccarit (tinh bột hoặc xenlulozơ) => Phát biểu (b) đúng.
C6H12O6 (glucozơ) và C12H22O11 (saccarozơ) đều có 2OH liền kề, do đó chúng đều hòa tan Cu(OH)2 tạo phức màu xanh lam. => Phát biểu (c) đúng.
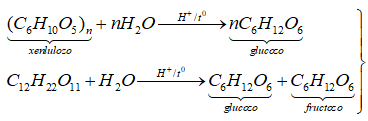
=> Phát biểu (d) sai.
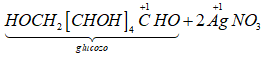
![]()
![]()
Glucozơ là chất khử, AgNO3 là chất oxi hóa => Glucozơ bị oxi hóa bởi AgNO3/NH3 => Phát biểu (e) đúng.
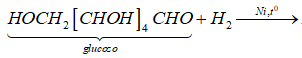
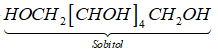
=> Phát biểu (g) đúng.
Các phát biểu đúng gồm: (a), (b), (c), (e), (g). Đáp án B.
Câu 25:
04/07/2024Xà phòng hóa hoàn toàn 17,00 gam triglixerit cần vừa đủ 0,06 mol NaOH. Cô cạn dung dịch sau phản ứng thu được khối lượng xà phòng nguyên chất là:
 Xem đáp án
Xem đáp án
Sơ đồ phản ứng:
![]()
![]()
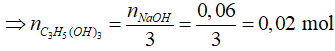
![]()
![]()
![]()
![]()
Đáp án A.
Câu 26:
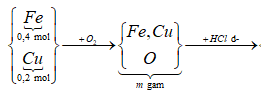
19/07/2024Đốt hỗn hợp gồm 0,4 mol Fe và 0,2 mol Cu trong bình khí đựng oxi, sau một thời gian thu được m gam hỗn hợp chất rắn. Cho toàn bộ chất rắn này vào dung dịch HCl dư, sau khi các phản ứng xảy ra hoàn toàn thu được 3,36 lít (đktc) khí và 6,4 gam kim loại không tan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Kim loại không tan là Cu dư.
Cu dư => Muối thu được gồm FeCl2 và CuCl2 vì: Cu + 2FeCl3 CuCl2 + 2FeCl2
Số mol các chất là: 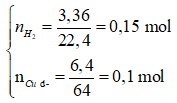
Sơ đồ phản ứng:
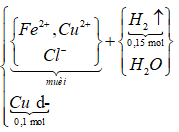
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Đáp án A.
Câu 27:
21/07/2024Đốt cháy hoàn toàn m gam hỗn hợp X gốm 2 este đồng phân cần dùng 4,704 lít khí O2, thu được 4,032 lít khí CO2 và 3,24 gam H2O. Nếu cho m gam X tác dụnghết với 110ml dung dịch KOH 1M. Cô cạn dung dịch sau phản ứng thu được 7,98 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY > MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỷ lệ a:b là:
 Xem đáp án
Xem đáp án
*Xét giai đoạn đốt cháy X:
Số mol các chất là:
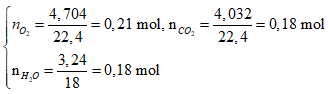
![]() => X gồm hai este no, đơn chức, mạch hở, có dạng: CnH2nO2
=> X gồm hai este no, đơn chức, mạch hở, có dạng: CnH2nO2
Sơ đồ phản ứng: ![]()
![]()
![]()

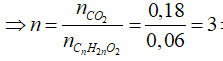
=> X: C3H6O2
C3H6O2 chỉ có hai este là HCOOC2H5 và CH3COOCH3
*Xét giai đoạn X tác dụng với dung dịch KOH:
Số mol KOH là: ![]()
Phương trình phản ứng: ![]()
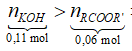 => RCOOR’ hết, KOH dư.
=> RCOOR’ hết, KOH dư.
![]()
![]()
Sơ đồ phản ứng:

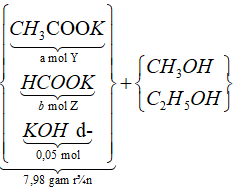
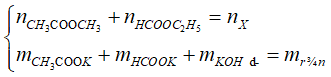
![]()
![]()
Đáp án D
Câu 28:
19/07/2024Cho sơ đồ chuyển hóa sau:
Biết Y và Z đều có phản ứng tráng bạc. Hai chất Y và Z tương ứng là:
 Xem đáp án
Xem đáp án
Y và Z đều tham gia phản ứng tráng bạc => C3H4O2 là este của axit fomic và ancol không bền chuyển thành andehit => C3H4O2 là HCOOCH=CH2
Các phương trình phản ứng:
![]()

![]()
![]()
Vậy Y là CH3CHO, Z là HCOOH
Đáp án D.
Câu 29:
20/07/2024Cho hai hợp chất hữu cơ X, Y có cùng công thức phân tử C3H7NO2. Khi phản ứng với dung dịch NaOH, X tạo ra sản phẩm gồm H2NCH2COONa và chất hữu cơ Z; Y tạo ra sản phẩm gồm CH2=CHCOONa và khí T. Các chất Z và T lần lượt là:
 Xem đáp án
Xem đáp án
![]()
![]()
![]()
![]()
Các phương trình phản ứng:
![]()
![]()
![]()
![]()
=> Z là CH3OH, T là NH3. Đáp án A.
Câu 30:
04/07/2024Cho 86,3 gam hỗn hợp X gồm Na, K, Ba và Al2O3 (trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước, thu được dung dịch Y. Sau khi các phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là:
 Xem đáp án
Xem đáp án
Số mol các chất là:
![]()
![]()
![]()

![]()
![]()
![]()
Gọi M là kim loại chung cho Na, K và Ba
Các phương trình phản ứng khi cho X tan hết trong H2O:
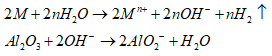
Dung dịch Y gồm Mn+, OH- dư và AlO2-
Dung dịch Y tác dụng với dung dịch HCl:

![]()
![]()
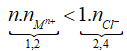 => dung dịch sau cùng gồm:
=> dung dịch sau cùng gồm: ![]()
Sơ đồ phản ứng:
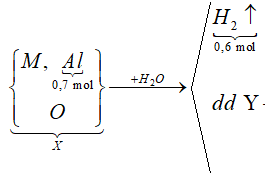

![]()
![]()
![]()
![]()
![]()
Đáp án B.
Câu 31:
17/07/2024Cho các phát biểu sau:
(a) Thủy phân hoàn toàn vinyl axetat bằng NaOH, thu được natri axetat và anđehit fomic.
(b) Polietilen được điều chế bằng phản ứng trùng ngưng.
(c) Ở điều kiện thường, anilin là chất khí.
(d) Tinh bột thuộc loại polisaccarit.
(e) Ở điều kiện thích hợp, triolein tham gia phản ứng cộng H2.
Số phát biểu đúng là:
 Xem đáp án
Xem đáp án
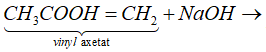
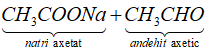
=> Phát biểu (a) sai.
Polietilen được điều chế bằng phản ứng trùng hợp etilen:

=> Phát biểu (b) sai.
Ở điều kiện thường, anilin là chất lỏng. => Phát biểu (c) sai.
Tinh bột thuộc loại polisaccarit => Phát biểu (d) đúng.
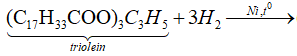
![]()
=> Phát biểu (e) đúng.
Các phát biểu đúng là: (d) và (e). Đáp án B.
Câu 32:
23/07/2024Hòa tan chất X vào nước thu được dung dịch trong suốt, rồi thêm tiếp dung dịch chất Y thì thu được chất Z (làm vẩn đục dung dịch). Các chất X,Y,Z lần lượt là:
 Xem đáp án
Xem đáp án
Các chất X,Y,Z lần lượt là natri phenolat, axit clohidric, phenol vì:
C6H5ONa (natri phenolat) tan tốt trong nước, do đó hòa tan C6H5Ona vào nước thu được dung dịch trong suốt.
![]()
Đáp án D.
Câu 33:
21/07/2024Hỗn hợp X gồm Fe2O3, FeO và Cu (trong đó nguyên tố sắt chiếm 52,5% về khối lượng). Cho m gam X tác dụng với 420ml dung dịch HCl 2M (dư), thu được dung dịch Y và còn lại 0,2m gam chất rắn không tan. Cho dung dịch AgNO3 dư vào Y, thu được khí NO và 141,6 gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là:
 Xem đáp án
Xem đáp án
Số mol HCl là: ![]()
Quy đổi hỗn hợp X thành Fe: a mol; Cu: b mol; O: c mol
![]()
![]()
![]()
Chất rắn không tan là Cu dư => Dung dịch Y gồm FeCl2, CuCl2 và HCl dư => Dung dịch Y gồm các ion ![]()
![]()
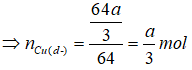
![]()
![]()
Các phương trình phản ứng tạo kết tủa:
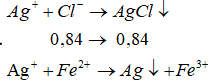
![]()
![]()
Sơ đồ phản ứng:
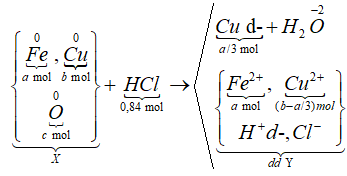
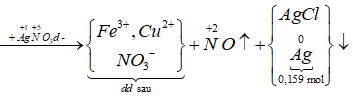
![]()
![]()
![]()
![]()
*Xét giai đoạn dung dịch Y tác dụng với dung dịch AgNO3 dư:

Các bán phản ứng oxi hóa – khử:
![]()
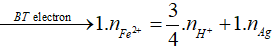
![]()
![]()
![]()
Đáp án A.
Câu 34:
21/07/2024Cho 34 gam hỗn hợp X gồm hai este đơn chức và đều thuộc loại hợp chất thơm (tỉ khối hơi của X đối với O2 luôn bằng 4,25 với mọi tỷ lệ số mol giữa hai este) tác dụng vừa đủ với 175ml dung dịch NaOH 2M. Cô cạn dung dịch sau phản ứng thu được hỗn hợp Y gồm hai muối khan. Thành phần phần trăm về khối lượng của hai muối trong Y là:
 Xem đáp án
Xem đáp án
![]()
không phục thuộc vào tỷ lệ mol của các este
=> 2 este là đồng phân của nhau
=> 2 este là C8H8O2
Số mol các chất là: 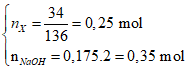
![]() X gồm 1 este – ancol và 1 este – phenol
X gồm 1 este – ancol và 1 este – phenol
Đặt số mol các chất trong X là este - ancol: a mol; este – phenol: b mol

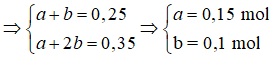
X + NaOH ![]() 2 muối => X gồm HCOOCH2C6H5 (0,15 mol) và HCOOC6H4CH3 (0,1 mol)
2 muối => X gồm HCOOCH2C6H5 (0,15 mol) và HCOOC6H4CH3 (0,1 mol)
Sơ đồ phản ứng:


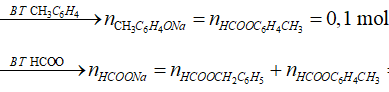 = 0,15 + 0,1 = 0,25 mol
= 0,15 + 0,1 = 0,25 mol
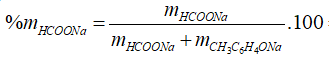
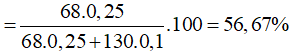
![]()
Đáp án C.
Câu 35:
26/06/2024Hỗn hợp E gồm chất X (C3H10N2O4) và chất Y (C3H12N2O3). X là muối của axit hữu cơ đa chức, Y là muối của một axit vô cơ. Cho 3,86 gam E tác dụng với dung dịch NaOH dư, đun nóng, thu được 0,06 mol hai khí (có tỷ lệ mol 1:5) và dung dịch chứa m gam muối. Giá trị của m là:
 Xem đáp án
Xem đáp án
Các chất trong E có thể là:
X: H4NOOC – COOH3NCH3 hoặc H4NCOOC – CH2 - COONH4
Y: (CH3NH3)2CO3 hoặc (NH4)(C2H5CH3)CO3 hoặc (NH4)((CH3)2NH2)CO3.
X, Y luôn tác dụng với NaOH theo tỷ lệ 1:2 và thu được số mok khí luôn gấp 2 lần số mol X và Y
Đặt số mol các chất là: C3H10N2O4: a mol; C3H12N2O3: b mol

Do 2 khí thu được với tỷ lệ số mol là 1:5![]() X là H4NOOC – COOH3NCH3; Y là (CH3NH3)2CO3
X là H4NOOC – COOH3NCH3; Y là (CH3NH3)2CO3
Phương trình phản ứng:
![]()
![]()
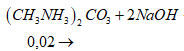
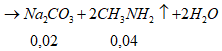
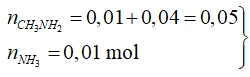
![]() => Thỏa mãn
=> Thỏa mãn
![]()
![]()
Đáp án A.
Câu 36:
12/07/2024Hòa tan hoàn toàn 15,6 gam hỗn hợp Fe, Fe3O4, Fe2O3, Mg, MgO và CuO vào 200 gam dung dịch H2SO4 và NaNO3 thu được dung dịch X chỉ chứa muối sunfat trung hòa của kim loại, hỗn hợp khí Y gòm 0,01 mol N2O và 0,02 mol NO. Cho X phản ứng với dung dịch Ba(OH)2 dư, thu được 89,15 gam kết tủa. Lọc kết tủa nung trong không khí đến khối lượng không đổi, thu được 84,386 gam chất rắn. Nồng độ phần trăm của FeSO4 trong X có giá trị gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Đặt khối lượng kim loại trong hỗn hợp ban đầu là m gam; số mol O trong hoonx hợp ban đầu là a mol; số mol H2SO4 là b mol.
![]()
Sơ đồ phản ứng:


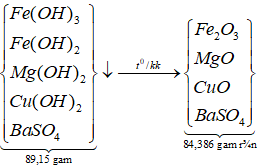
![]()
![]()
Các quá trình tham gia phản ứng của H+: 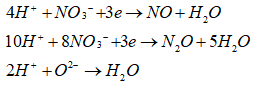
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
*Xét giai đoạn nung kết tủa đến khối lượng không đổi:
Sơ đồ phản ứng:
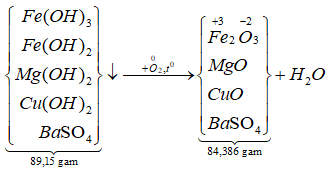
![]()
![]()
![]()
![]()

![]()
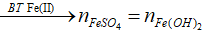
![]()
![]()
![]()
![]() = 85%.
= 85%.
Đáp án A.
Câu 37:
20/07/2024Khi nhỏ từ từ đến dư dung dịch KOH vào dung dịch hỗn hợp chứa AlCl3 và HCl, kết quả thí nghiệm được biểu diễn trên đồ thị sau (số liệu tính theo đơn vị mol).
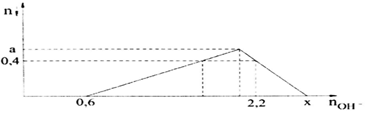
Tỷ lệ x : a là:
 Xem đáp án
Xem đáp án
Các phương trình phản ứng: 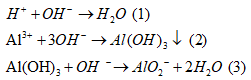
Tại 0,6 mol KOH thì chỉ xảy ra phản ứng (1):
![]()
![]()
*Cách 1: Khi kết tủa cực đại thì AlCL3 chuyển hết về Al(OH)3
![]()
Tại 2,2 mol KOH thì xảy ra cả (1), (2), (3), khi đó lượng kết tủa bị hòa tan một phần
Sơ đồ phản ứng:
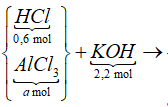
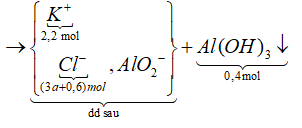
![]()
![]()
![]()
![]()
Tại thời điểm x mol KOH thì xảy ra cả (1), (2) (3), khi đó lượng kết tủa bị hòa tan hoàn toàn:
Sơ đồ phản ứng: 
![]()
![]()
![]()
![]()
![]()
*Cách 2:
· Xét 2,2 mol KOH và 0,4 mol Al(OH)3:
Xảy ra cả (1), (2), (3): kết tủa tan một phần
![]()
![]()
![]()
Khi kết tủa cực đại thì AlCl3 chuyển hết về Al(OH)3

![]()
· Xét tại x mol KOH: kết tủa tan hoàn toàn:
![]()
![]()
![]()
Đáp án D.
Câu 38:
08/07/2024Hòa tan hoàn toàn hỗn hợp X gồm CuSO4 và KCl vào H2O, thu được dung dịch Y. Điện phân Y (có màng ngăn, điện cực trơ) đến khi H2O bắt đầu điện phân ở cả hai điện cực thì dừng điện phân. Số mol khí thoát ra ở anot bằng 4 lần số mol khí thoát ra từ catot. Phần trăm khối lượng của CuSO4 trong X là:
 Xem đáp án
Xem đáp án
Dung dịch Y gồm các ion Cu2+, K+, SO42- và Cl-
Các ion K+ và SO42- không bị điện phân trong dung dịch
Chọn: nkhí catot = 1 mol![]() nkhí anot = 4 mol
nkhí anot = 4 mol
Thứ tự xảy ra các quá trình ở các điện cực là:
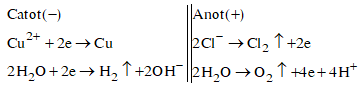
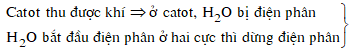
![]() Anot, H2O bắt đầu điện phân
Anot, H2O bắt đầu điện phân ![]() có thể coi ở anot, H2O không bị điện phân
có thể coi ở anot, H2O không bị điện phân
Các quá trình xảy ra ở các điện cực:
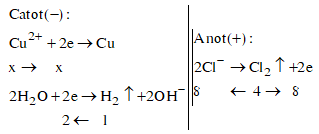
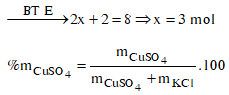
![]()
Đáp án B
Câu 39:
17/07/2024Cho các chất hữu cơ mạch hở: X là axit không no có hai liên kết trong phân tử, Y là axit no đơn chức, Z là ancol hai chức, T là este của X, Y với Z. Đốt cháy hoàn toàn a gam hỗn hợp M gồm X và T, thu được 0,1 mol CO2 và 0,07 mol H2O. Cho 6,9 gam M phản ứng vừa đủ với dung dịch NaOH, cô cạn dung dịch sau phản ứng thu được hỗn hợp muối khan E. Đốt cháy hoàn toàn E, thu được Na2CO3, 0,195 mol CO2 và 0,135 mol H2O. Phần trăm khối lượng của T trong M có giá trị gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Xét quá trình đốt cháy E:
![]()
![]()
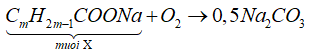
![]()
![]()
![]()
M gồm RCOOH (X); RCOO – R’ – OOCR’ (T) ![]()
Xét giai đoạn đốt cháy a gam M: ![]()
Ø Xét giai đoạn đốt cháy 6,9 gam M:
![]()
Đặt số mol CO2: 10z; H2O: 7z mol
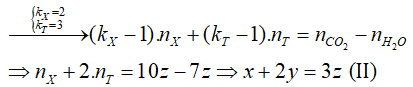
![]()
![]()
![]()
![]()
![]()

![]()
![]()
![]()
Đáp án A.
Câu 40:
22/07/2024Hòa tan hoàn toàn m gam hỗn hợp X gồm Ba, BaO, Al và Al2O3 vào nước dư, thu được 0,896 lít khí (đktc) và dung dịch Y. Hấp thụ hoàn toàn 1,2096 lít khí CO2 (đktc) vào Y, thu được 4,032 gam kết tủa. Lọc kết tủa thu được dung dịch Z chỉ chứa một chất tan. Mặt khác, dẫn từ từ CO2 đến dư vào Y thì thu được 3,12 gam kết tủa. Giá trị của m là:
 Xem đáp án
Xem đáp án
X tác dụng với H2O dư:
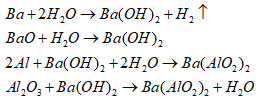
=> Dung dịch Y gồm , Ba(OH)2 hay gồm các ion: ![]()
Ø Sục CO2 dư vào dung dịch Y:
Các phương trình hóa học: 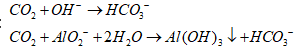
Kết tủa thu được là Al(OH)3 ![]()
![]()
Ø Sục 1,2096 lít CO2 vào dung dịch Y:
![]()
Chất tan duy nhất là Ba(HCO3)2
Sơ đồ phản ứng:


![]()
![]()
![]()
![]()
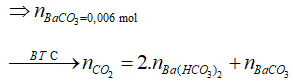
![]()
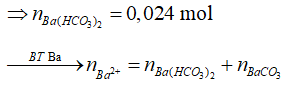
![]()
Ø Xét giai đoạn m gam X tác dụng với H2O dư:
Khí thu được là H2 ![]()
Quy đổi X thành Ba: 0,03 mol; Al: 0,04 mol và O
Sơ đồ phản ứng:

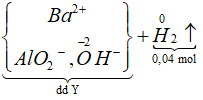
![]()
![]()

![]()
Đáp án D.
Bài thi liên quan
-
160 Bài trắc nghiệm Ôn thi THPTQG Hóa Học cực hay có lời giải chi tiết ( đề 2)
-
39 câu hỏi
-
50 phút
-
-
160 Bài trắc nghiệm Ôn thi THPTQG Hóa Học cực hay có lời giải chi tiết ( đề 3)
-
40 câu hỏi
-
50 phút
-
-
160 Bài trắc nghiệm Ôn thi THPTQG Hóa Học cực hay có lời giải chi tiết ( đề 4)
-
40 câu hỏi
-
50 phút
-
