Giải Hóa 9 Bài 33: Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng
Lời giải bài tập Hóa học lớp 9 Bài 33: Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa 9 Bài 33. Mời các bạn đón xem:
Giải Hóa 9 Bài 33: Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng
Video giải Hóa 9 Bài 33: Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng
Thí nghiệm 1 trang 104 Hóa học 9: Cacbon khử CuO ở nhiệt độ cao
- Tiến hành thí nghiệm:
+ Lấy một ít (bằng hạt ngô) hỗn hợp đồng(II) oxit và cacbon (bột than gỗ) vào ống nghiệm.
+ Lắp đặt dụng cụ như hình:
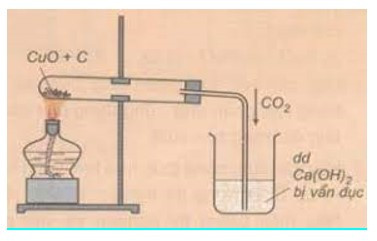
+ Đun nóng đáy ống nghiệm bằng ngọn lửa đèn cồn.
+ Quan sát sự thay đổi màu của hỗn hợp phản ứng và hiện tượng xảy ra trong ống nghiệm đựng Ca(OH)2.
+ Mô tả hiện tượng xảy ra, giải thích và viết phương trình hóa học.
- Hiện tượng: Hỗn hợp CuO + C đun nóng có sự chuyển đổi từ màu đen → màu đỏ.
Dung dịch nước vôi trong vẩn đục.
Giải thích:
2CuO (đen) + C to→to→ 2Cu (đỏ) + CO2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
- Kết luận: Cacbon có tính khử.
Thí nghiệm 2 trang 104 Hóa học 9: Nhiệt phân muối NaHCO3
- Tiến hành thí nghiệm:
+ Lấy 1 thìa nhỏ muối NaHCO3 vào ống nghiệm.
+ Lắp dụng cụ như hình:
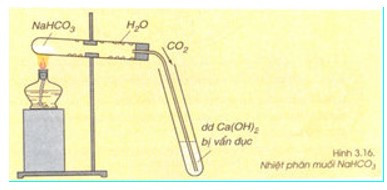
+ Đun nóng đáy ống nghiệm bằng ngọn lửa đèn cồn.
+ Quan sát hiện tượng xảy ra trên thành ống nghiệm và sự thay đổi ở ống nghiệm đựng Ca(OH)2.
+ Mô tả hiện tượng, giải thích và viết phương trình hóa học.
- Hiện tượng: Lượng muối NaHCO3 giảm dần → NaHCO3 bị nhiệt phân.
Phần miệng ống nghiệm có hơi nước ngưng đọng → có nước tạo ra.
Dung dịch Ca(OH)2 bị vẩn đục.
- Giải thích:
2NaHCO3 to→to→ Na2CO3 + H2O + CO2.
Ca(OH)2 + CO2 → CaCO3↓ + H2O.
- Kết luận: NaHCO3 dễ bị nhiệt phân hủy.
Thí nghiệm 3 trang 104 Hóa học 9: Nhận biết muối cacbonat và muối clorua
* Phương án nhận biết 3 chất: NaCl, Na2CO3, CaCO3
- Đánh số thứ tự từng lọ mất nhãn, trích mỗi lọ một ít sang ống nghiệm đánh số tương ứng.
- Cho lần lượt từng mẫu thử vào nước:
+ Mẫu thử không tan là CaCO3.
+ Mẫu thử tan trong nước là NaCl và Na2CO3 (nhóm I).
- Tiếp tục cho dung dịch HCl lần lượt vào các dung dịch ở nhóm I
+ Nếu có khí thoát ra thì mẫu thử là Na2CO3
Na2CO3 + 2HCl → 2NaCl + CO2 ↑ + H2O
+ Nếu không có hiện tượng gì xuất hiện, mẫu thử là NaCl.
- Dán nhãn các lọ hóa chất vừa xác định.
Xem thêm lời giải bài tập Hóa học lớp 9 hay, chi tiết khác:
Bài 34: Khái niệm về hợp chất hữu cơ và hóa học hữu cơ
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 9 (hay nhất) | Để học tốt Ngữ văn 9 (sách mới)
- Soạn văn 9 (ngắn nhất)
- Văn mẫu 9 (sách mới) | Để học tốt Ngữ văn 9 Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 9 (sách mới) | Giải bài tập Toán 9 Tập 1, Tập 2
- Giải sbt Toán 9
- Lý thuyết Toán 9
- Các dạng bài tập Toán lớp 9
- Giáo án Toán lớp 9 mới nhất
- Bài tập Toán lớp 9 mới nhất
- Chuyên đề Toán lớp 9 mới nhất
- Giải sgk Tiếng Anh 9 (thí điểm)
- Giải sgk Tiếng Anh 9 (sách mới) | Để học tốt Tiếng Anh 9
- Giải sbt Tiếng Anh 9
- Giải sbt Tiếng Anh 9 (thí điểm)
- Giải sgk Sinh học 9 (sách mới) | Giải bài tập Sinh học 9
- Giải vở bài tập Sinh học 9
- Lý thuyết Sinh học 9
- Giải sbt Sinh học 9
- Giải sgk Vật Lí 9 (sách mới) | Giải bài tập Vật lí 9
- Giải sbt Vật Lí 9
- Lý thuyết Vật Lí 9
- Các dạng bài tập Vật lí lớp 9
- Giải vở bài tập Vật lí 9
- Giải sgk Địa Lí 9 (sách mới) | Giải bài tập Địa lí 9
- Lý thuyết Địa Lí 9
- Giải Tập bản đồ Địa Lí 9
- Giải sgk Tin học 9 (sách mới) | Giải bài tập Tin học 9
- Lý thuyết Tin học 9
- Lý thuyết Giáo dục công dân 9
- Giải vở bài tập Lịch sử 9
- Giải Tập bản đồ Lịch sử 9
- Lý thuyết Lịch sử 9
- Lý thuyết Công nghệ 9
