Ba thí nghiệm được tiến hành với những khối lượng Zn bằng nhau và với
Với giải bài 32.6 trang 69 Sách bài tập Hóa học 10 được biên soạn lời giải chi tiết sẽ giúp học sinh biết cách làm bài tập môn Hóa 10. Mời các bạn đón xem:
Giải SBT Hóa 10 Bài 30: Hidro sunfua - Lưu huỳnh đioxit - Lưu huỳnh trioxit
Bài 32.6 trang 69 Sách bài tập Hóa học 10: Ba thí nghiệm được tiến hành với những khối lượng Zn bằng nhau và với 50cm3 dung dịch loãng H2SO4 2M.
PTHH của phản ứng :
Zn + H2SO4 → ZnSO4 + H2↑
Bảng dưới đây cho biết các điều kiện của mỗi thí nghiệm :
|
Thí nghiệm |
Kẽm |
Nhiệt độ (°C) |
|
1 |
bột |
30 |
|
2 |
lá |
20 |
|
3 |
lá |
30 |
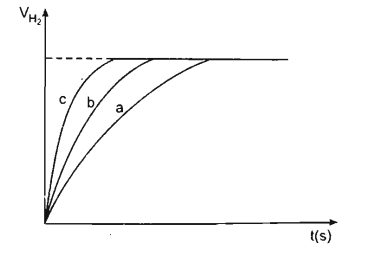
Khí hiđro thu được trong mỗi thí nghiệm được ghi lại theo những khoảng cách nhất định về thời gian cho đến khi phản ứng kết thúc, được biểu diễn bằng đồ thị sau :
a) Rút ra được những nhận xét gì khi so sánh hiện tượng phản ứng của :
- Thí nghiệm 1 và thí nghiệm 3 ?
- Thí nghiệm 2 và thí nghiệm 3 ?
b) Hãy quan sát đồ thị trên để cho biết các đường cong a, b, c biểu thị cho những thí nghiệm nào ?
c) Ghi thể tích khí H2 trên trục y khi phản ứng kết thúc. Biết rằng ở điều kiện phòng thí nghiệm, 1 mol khí có thể tích là 24 lít và Zn còn dư sau các thí nghiệm.
Lời giải
a) Nhận xét:
- Khí hiđro được giải phóng ở thí nghiệm 1 nhiều, nhanh hơn ở thí nghiệm 3. Vì diện tích tiếp xúc của Zn với H2SO4 ở thí nghiệm 1 lớn hơn. trong khi đó nhiệt độ của dung dịch axit là như nhau.
- Khí hiđro được giải phóng ở thí nghiệm 3 nhiều, nhanh hơn ở thí nghiệm 2. Vì nhiệt độ của dung dịch H2SO4 ở thí nghiệm 3 cao hơn, trong khi đó diện tích tiếp xúc giữa Zn và axit là như nhau.
b) Đồ thị biểu diễn các phản ứng :
Đường cong c biểu diễn cho thí nghiệm 1, phản ứng xảy ra nhanh nhất
Đường cong b biểu diễn cho thí nghiệm 3, phản ứng xảy ra nhanh trung bình.
Đường cong a biểu diễn cho thí nghiệm 2, phản ứng xảy ra chậm nhất.
c) Thể tích khí hiđro :
Sau các thí nghiệm, kẽm còn dư. Như vậy, thể tích khí hiđro được sinh ra phụ thuộc vào lượng H2SO4 tham gia phản ứng :
nH2=nH2SO4=2.501000=0,1 mol
Thể tích khí hiđro ở điều kiện phòng là :
VH2=24.0,1=2,4(lít) hoặc 2400 cm3
Ta ghi số 2400 cm3 trên trục y, nơi giao điểm giữa trục y và đường ngang của 3 đường cong kéo dài (nét chấm trên đồ thị).
Xem thêm lời giải sách bài tập Hóa học lớp 10 hay, chi tiết khác:
Bài 32.1 trang 68 SBT Hóa 10: Cho phản ứng...
Bài 32.2 trang 68 SBT Hóa 10: Oxit nào sau đây là hợp chất ion...
Bài 32.3 trang 68 SBT hóa 10: Chất nào sau đây vừa có tính oxi hóa, vừa có tính khử...
Bài 32.4 trang 68 SBT Hóa 10: Khí CO2 có lẫn tạp chất là SO2 ...
Bài 32.5 trang 69 SBT Hóa 10: Cho sơ đồ phản ứng...
Bài 32.8 trang 70 SBT Hóa 10: Từ những chất sau...
Bài 32.12 trang 71 SBT Hóa 10: Viết PTHH của chuỗi phản ứng sau...
Bài 32.13 trang 71 SBT Hóa 10: Tại sao dung dịch H2S trong nước để lâu ngày trở nên vẩn đục...
Bài 32.14 trang 72 SBT Hóa 10: Viết PTHH của các phản ứng của H2S với O2, SO2, nước clo...
Bài 32.17 trang 72 SBT Hóa 10: Dẫn từ từ 28 gam hỗn hợp X gồm (CO2, SO2)...
Xem thêm các chương trình khác:
- Giải sgk Vật Lí 10 | Giải bài tập Vật lí 10 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 10
- Tóm tắt tác phẩm Ngữ văn 10
- Soạn văn 10 (hay nhất) | Để học tốt Ngữ Văn 10 (sách mới)
- Soạn văn 10 (ngắn nhất) | Để học tốt Ngữ văn 10 (sách mới)
- Văn mẫu lớp 10 (cả ba sách) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Lịch sử 10 | Giải bài tập Lịch sử 10 Học kì 1, Học kì 2 (sách mới)
