Giải SBT Hoá học 10 Bài 3. Cấu trúc lớp vỏ electron nguyên tử có đáp án
Giải SBT Hoá học 10 Bài 3. Cấu trúc lớp vỏ electron nguyên tử có đáp án
-
242 lượt thi
-
25 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 1:
20/07/2024 Xem đáp án
Xem đáp án
Orbital nguyên tử là khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt electron lớn nhất.
Câu 2:
20/07/2024Sự phân bố electron trong một orbital dựa vào nguyên lí hay quy tắc nào sau đây?
 Xem đáp án
Xem đáp án
Sự phân bố electron trong một orbital dựa vào nguyên lí Pauli: Trong 1 orbital chỉ chứa tối đa 2 electron có chiều tự quay ngược nhau.
Câu 3:
22/07/2024Sự phân bố electron trên các phân lớp thuộc các lớp electron dựa vào nguyên lí hay quy tắc nào sau đây?
 Xem đáp án
Xem đáp án
Sự phân bố electron trên các phân lớp thuộc các lớp electron dựa vào nguyên lí vững bền và quy tắc Hund.
+ Nguyên lí vững bền: Các electron trong nguyên tử ở trạng thái cơ bản lần lượt chiếm các orbital có mức năng lượng từ thấp đến cao: 1s 2s 2p 3s 3p 4s …
+ Quy tắc Hund: Trong cùng một lớp, các electron sẽ phân bố trên các orbital sao cho số electron độc thân là tối đa và các electron này có chiều tự quay giống nhau.
Câu 4:
22/07/2024Sự phân bố electron vào các lớp và phân lớp căn cứ vào
 Xem đáp án
Xem đáp án
Sự phân bố electron vào các lớp và phân lớp căn cứ vào mức năng lượng electron.
Nguyên lí vững bền: Các electron trong nguyên tử ở trạng thái cơ bản lần lượt chiếm các orbital có mức năng lượng từ thấp đến cao: 1s 2s 2p 3s 3p 4s …
Câu 5:
22/07/2024Ở trạng thái cơ bản, trong nguyên tử, electron chiếm các mức năng lượng
 Xem đáp án
Xem đáp án
Ở trạng thái cơ bản, trong nguyên tử, electron chiếm các mức năng lượng lần lượt từ thấp đến cao.
Câu 6:
13/07/2024Các lớp electron được đánh số từ trong ra ngoài bằng các số nguyên dương: n = 1, 2, 3, ... với tên gọi là các chữ cái in hoa là
 Xem đáp án
Xem đáp án
|
n |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Tên lớp |
K |
L |
M |
N |
O |
P |
Q |
Câu 7:
20/07/2024Các phân lớp trong mỗi lớp electron được kí hiệu bằng các chữ cái viết thường theo thứ tự là
 Xem đáp án
Xem đáp án
Các phân lớp trong mỗi lớp electron được kí hiệu bằng các chữ cái viết thường theo thứ tự là s, p, d, f, …
Câu 8:
14/07/2024 Xem đáp án
Xem đáp án
- Những electron ở lớp gần hạt nhân bị hút mạnh hơn về phía hạt nhân, vì thế có năng lượng thấp hơn so với những electron ở lớp xa hạt nhân.
⇒ B sai, A đúng vì lớp K là lớp gần hạt nhân nhất.
- Electron ở orbital 3p có mức năng lượng cao hơn electron ở orbital 3s ⇒ C sai
- Các electron thuộc cùng một lớp có mức năng lượng gần bằng nhau ⇒ D sai
Câu 9:
13/07/2024Mỗi orbital nguyên tử chứa tối đa
 Xem đáp án
Xem đáp án
Mỗi orbital nguyên tử chứa tối đa 2 electron có chiều tự quay ngược nhau (nguyên lí loại trừ Pauli)
Câu 10:
23/07/2024Số orbital trong các phân lớp s, p, d lần lượt bằng
 Xem đáp án
Xem đáp án
Phân lớp s có 1 AO
Phân lớp p có 3 AO
Phân lớp d có 5 AO
Câu 11:
13/07/2024Phân lớp 3d có số electron tối đa là
 Xem đáp án
Xem đáp án
Phân lớp d có 5 AO. Mỗi AO chứa tối đa 2 electron
⇒ Phân lớp 3d có số electron tối đa là 5.2 = 10 electron.
Câu 12:
13/07/2024Lớp L có số phân lớp electron bằng
 Xem đáp án
Xem đáp án
Số phân lớp trong mỗi lớp bằng số thứ tự của lớp (n ≤ 4)
Phân lớp L (n = 2) có 2 phân lớp là 2s và 2p.
Câu 13:
21/07/2024 Xem đáp án
Xem đáp án
Trong lớp electron thứ n có n2 AO (n ≤ 4)
Lớp M (n = 3) có 32 = 9 AO
Câu 14:
13/07/2024Lớp M có số electron tối đa bằng
 Xem đáp án
Xem đáp án
Trong lớp electron thứ n có n2 AO (n ≤ 4)
Mỗi AO chứa tối đa 2 electron
⇒ Lớp M (n = 3) có số electron tối đa bằng 2.32 =18 electron.
Câu 15:
20/07/2024Các electron của nguyên tử nguyên tố X được phân bố trên ba lớp, lớp thứ ba có 6 electron. Số đơn vị điện tích hạt nhân của nguyên tử nguyên tố X là
 Xem đáp án
Xem đáp án
Theo chiều tăng của mức năng lượng: 1s 2s 2p 3s 3p 4s …
Lớp thứ 3 có 6 electron ⇒ 2 electron được điền vào 3s và 4 electron được điền vào 3p
Cấu hình electron của X là: 1s2 2s2 2p6 3s2 3p4
Câu 16:
14/07/2024Nguyên tố X có Z = 17. Electron lớp ngoài cùng của nguyên tử nguyên tố X thuộc lớp
 Xem đáp án
Xem đáp án
Xcó Z = 17 nên nguyên tử X có 17 electron.
- Viết thứ tự các lớp và phân lớp electron theo chiều tăng của năng lượng:
1s 2s 2p 3s 3p 4s …
- Điền các electron vào các phân lớp electron theo nguyên lí vững bền:
1s22s22p63s23p5.
⇒ Cấu hình electron của nguyên tử X là: 1s22s22p63s23p5.
⇒ Electron lớp ngoài cùng của X thuộc lớp thứ 3 (lớp M)
Câu 17:
19/07/2024Cách biểu diễn electron trong AO nào sau đây không tuân theo nguyên lí Pauli?
 Xem đáp án
Xem đáp án
Nguyên lí Pauli: Trong 1 orbital chỉ chứa tối đa 2 electron có chiều tự quay ngược nhau.
Nếu orbital có 1 electron thì biểu diễn bằng 1 mũi tên đi lên, nếu orbital có 2 electron thì được biểu diễn bằng 2 mũi tên ngược chiều nhau, mũi tên đi lên viết trước.
Câu 18:
23/07/2024Sự phân bố electron theo ô orbital nào dưới đây là đúng?
 Xem đáp án
Xem đáp án
Sự phân bố electron theo ô orbital trên các lớp và phân lớp cần tuân theo nguyên lí Pauli và quy tắc Hund.
Nguyên lí Pauli: Trong 1 orbital chỉ chứa tối đa 2 electron có chiều tự quay ngược nhau.
⇒ A, D sai.
Câu 19:
18/07/2024Dùng ô orbital để mô tả cách sắp xếp electron trong orbital s.
 Xem đáp án
Xem đáp án
Nếu orbital s chỉ chứa 1 electron: 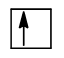
Nếu orbital s chứa 2 electron: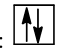
Chú ý: Trong 1 orbital chỉ chứa tối đa 2 electron có chiều tự quay ngược nhau (nguyên lí Pauli). Nếu orbital có 1 electron thì biểu diễn bằng 1 mũi tên đi lên ( 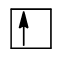 ), nếu orbital có 2 electron thì được biểu diễn bằng 2 mũi tên ngược chiều nhau, mũi tên đi lên viết trước (
), nếu orbital có 2 electron thì được biểu diễn bằng 2 mũi tên ngược chiều nhau, mũi tên đi lên viết trước ( 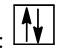 )
)
Câu 20:
23/07/2024Trường hợp trong orbital p có chứa hai electron thì có những cách nào biểu diễn electron trong orbital đó? Cách nào tuân theo quy tắc Hund?
 Xem đáp án
Xem đáp án
Trường hợp orbital p có chứa 2 electron, có rất nhiều cách để biểu diễn 2 electron trong AOp. Ví dụ một số cách:
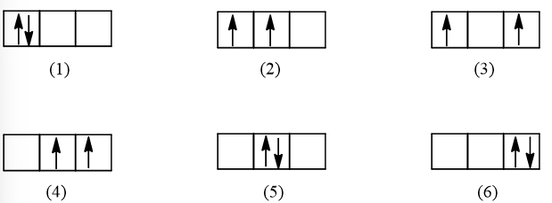
Tuy có nhiều cách biểu diễn nhưng chỉ có trường hợp (2) tuân theo quy tắc Hund (số electron độc thân là tối đa và các electron này có chiều tự quay giống nhau).
Chú ý:Theo nguyên lí Pauli: Trong 1 orbital chỉ chứa tối đa 2 electron có chiều tự quay ngược nhau. Nếu orbital có 1 electron thì biểu diễn bằng 1 mũi tên đi lên (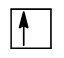 ), nếu orbital có 2 electron thì được biểu diễn bằng 2 mũi tên ngược chiều nhau, mũi tên đi lên viết trước (
), nếu orbital có 2 electron thì được biểu diễn bằng 2 mũi tên ngược chiều nhau, mũi tên đi lên viết trước ( 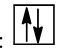 )
)
Câu 21:
18/07/2024 Xem đáp án
Xem đáp án
Mối quan hệ về năng lượng:
- Những electron ở lớp gần hạt nhân bị hút mạnh hơn về phía hạt nhân, vì thế có năng lượng thấp hơn so với những electron ở lớp xa hạt nhân. Mức năng lượng tăng dần theo lớp electron: K < L < M < N < O < …
- Các electron thuộc cùng một lớp có mức năng lượng gần bằng nhau. Mức năng lượng tăng dần theo AO: s < p < d < f.
- Các electron trên cùng một phân lớp có mức năng lượng bằng nhau.
Câu 22:
23/07/2024Cho biết tổng số electron tối đa chứa trong:
a) Phân lớp p;
b) Phân lớp d;
c) Lớp K;
d) Lớp M.
 Xem đáp án
Xem đáp án
a) Phân lớp p có 3 AO px, py, pz
Mỗi AO chứa tối đa 2 electron
⇒ Tổng số electron tối đa chứa trong phân lớp p là 2.3 = 6 electron
b) Phân lớp d có 5 AO 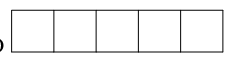
Mỗi AO chứa tối đa 2 electron
⇒ Tổng số electron tối đa chứa trong phân lớp d là 2.5 = 10 electron
c) Lớp K (n = 1) có 12 = 1 AO.
⇒ Số electron tối đa trong lớp K là 2.1 = 2 electron.
d) Lớp M (n = 3) có 32 = 9 AO
⇒ Số electron tối đa trong lớp M là 2.9 = 18 electron.
Câu 23:
22/07/2024Nguyên tố X có Z = 12 và nguyên tố Y có Z = 17.
Viết cấu hình electron nguyên tử của nguyên tố X và Y. Khi nguyên tử của nguyên tố X nhường đi hai electron và nguyên tử của nguyên tố Y nhận thêm một electron thì lớp electron ngoài cùng của chúng có đặc điểm gì?
 Xem đáp án
Xem đáp án
– Nguyên tử X (Z = 12) có cấu hình electron: 1s22s22p63s2
X nhường đi 2 electron: X → X2+ + 2e
Cấu hình electron của ion X2+ là 1s22s22p6
- Nguyên tử Y (Z = 17) có cấu hình electron: 1s22s22p63s23p5
Y nhận thêm 1 electron: Y + e → Y-
Cấu hình electron của Y- là 1s22s22p63s23p6
- Cấu hình electron của ion X2+ giống khí hiếm Ne, có 8 electron lớp ngoài cùng.
- Cấu hình electron của ion Y- giống với cấu hình electron của khí hiếm Ar, có 8 electron lớp ngoài cùng.
Câu 24:
13/07/2024Viết cấu hình electron theo ô orbital của nguyên tử các nguyên tố có Z = 9, Z = 14 và Z = 21. Chúng là nguyên tố kim loại, phi kim hay khí hiếm?
 Xem đáp án
Xem đáp án
+) Z = 9 (1s22s22p5): nguyên tử có 7 electron hóa trị, dễ thu electron, là phi kim.
Cấu hình electron theo ô orbital:
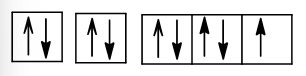
+) Z = 14 (1s22s22p63s23p2): nguyên tử có 4 electron hóa trị nên có thể thu electron hoặc nhường electron, là phi kim.
Cấu hình electron theo ô orbital:
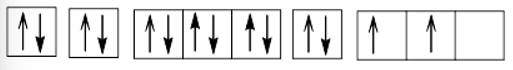
+) Z = 21 (1s22s22p63s23p63d14s2): nguyên tử có 3 electron hóa trị, dễ nhường electron, là kim loại.

Câu 25:
13/07/2024Hợp chất A có công thức M4X3. Tổng số hạt proton, electron và neutron trong phân tử A là 214. Tổng số hạt proton, neutron, electron của [M]4 nhiều hơn so với [X]3 trong A là 106.
a) Xác định công thức hóa học của A.
b) Viết cấu hình electron của các nguyên tử tạo nên A.
 Xem đáp án
Xem đáp án
a) Coi tổng số hạt trong [M] là x và [X] là y
Theo bài ra ta có: 4x + 3y = 214 (I)
và 4x – 3y = 106 (II)
Giải hệ (I) và (II), ta được: x = 40 và y = 18.
Số p = số e nên ta có:
2pM + nM = 40 với và pM < 20
⇒ pM = 13 và nM = 14
⇒ M là 13Al.
2pX + nX = 18 với và pX < 9
⇒ pX = 6 và nX = 6
⇒ X là 6C.
Công thức hóa học của A là Al4C3.
b) Cấu hình electron: 13Al (1s22s22p63s23p1) và 6C (1s22s22p2)
