Giải SBT Hóa 10 Bài 5: Lớp, phân lớp và cấu hình electron có đáp án Chạm vào số sao để đánh giá.
Giải SBT Hóa 10 Bài 5: Lớp, phân lớp và cấu hình electron có đáp án Chạm vào số sao để đánh giá.
-
81 lượt thi
-
20 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 1:
17/07/2024Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Electron trong cùng một phân lớp có năng lượng bằng nhau.
A sai vì: Electron trong cùng một lớp có năng lượng gần bằng nhau.
C sai vì: Electron ở các phân lớp 1s; 2s; 3s có năng lượng khác nhau.
D sai vì: Electron ở lớp bên ngoài có năng lượng cao hơn electron ở lớp bên trong.
Câu 2:
21/07/2024Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phát biểu A không đúng vì: Electron càng ở xa hạt nhân thì có năng lượng càng cao.
Câu 3:
22/07/2024Mỗi phát biểu sau đây là đúng hay sai?
(1) Số lượng orbital trong các phân lớp 1s, 2s, 3s là bằng nhau.
(2) Số lượng orbital trong các phân lớp 3s, 3p, 3d là bằng nhau.
(3) Các electron trên các phân lớp 1s, 2s, 3s có năng lượng bằng nhau.
(4) Các electron trên các phân lớp 3s, 3p, 3d có năng lượng bằng nhau.
(5) Số lượng electron tối đa trong một lớp là 2n2.
(6) Số lượng các orbital trong một phân lớp (s, p, d, f) luôn là một số lẻ.
 Xem đáp án
Xem đáp án
Các phát biểu (1); (5); (6) đúng.
Phát biểu (2) sai vì: Số lượng orbital trong các phân lớp 3s, 3p, 3d là khác nhau.
Phát biểu (3) sai vì: Các electron trên các phân lớp 1s, 2s, 3s có năng lượng khác nhau.
Phát biểu (4) sai vì: Các electron trên các phân lớp 3s, 3p, 3d có năng lượng gần bằng nhau.
Câu 4:
13/07/2024Điền từ/ cụm từ hoặc số thích hợp vào chỗ trống trong mỗi phát biểu sau:
a) Các electron trong lớp vỏ nguyên tử được phân bố vào các ...(1)... và ...(2)... dựa theo năng lượng của chúng. Các electron thuộc cùng một lớp có năng lượng ...(3)..., các electron thuộc cùng một phân lớp có năng lượng ...(4).... Các electron ở ...(5)... có vai trò quyết định đến tính chất hoá học đặc trưng của nguyên tố.
 Xem đáp án
Xem đáp án
a) Các electron trong lớp vỏ nguyên tử được phân bố vào các (1) lớp và (2) phân lớp dựa theo năng lượng của chúng. Các electron thuộc cùng một lớp có năng lượng (3) gần bằng nhau, các electron thuộc cùng một phân lớp có năng lượng (4) bằng nhau. Các electron ở (5) lớp ngoài cùng có vai trò quyết định đến tính chất hoá học đặc trưng của nguyên tố.
Câu 5:
18/07/2024b) Magnesium được sử dụng nhiều trong công nghiệp để chế tạo các bộ phận của máy bay, ô tô. Nguyên tử magnesium có 12 electron, được phân bố vào ...(1)... lớp. Lớp ngoài cùng của magnesium có ...(2)... electron.
 Xem đáp án
Xem đáp án
b) Magnesium được sử dụng nhiều trong công nghiệp để chế tạo các bộ phận của máy bay, ô tô. Nguyên tử magnesium có 12 electron, được phân bố vào (1) ba lớp. Lớp ngoài cùng của magnesium có (2) hai electron.
Câu 6:
15/07/2024Số phân lớp bão hòa trong các phân lớp: 1s2; 2s2; 2p3; 3d10; 3p4 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Phân lớp bão hòa là phân lớp đã chứa tối đa electron.
Các phân lớp bão hòa là: 1s2; 2s2; 3d10.
Câu 7:
13/07/2024Ghép mỗi biểu diễn ô orbital của phân lớp p ở cột A với mô tả thích hợp ở cột B.

 Xem đáp án
Xem đáp án
- Phân lớp bão hòa đã có tối đa electron.
- Phân lớp bán bão hòa chứa một nửa số electron tối đa.
- AO trống là AO không chứa electron nào.
Vậy a ghép với 3; b ghép với 2; c ghép với 1.
Câu 8:
21/07/2024Nguyên tử O có 8 electron. Biểu diễn sự sắp xếp electron trong nguyên tử O theo orbital nào sau đây là đúng?
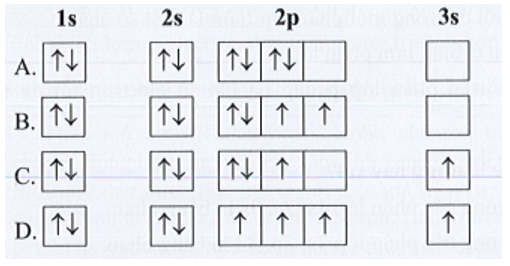
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Cách biểu diễn cấu hình electron theo orbital:
- Viết cấu hình electron của nguyên tử.
- Biểu diễn mỗi AO bằng một ô vuông, các AO trong cùng một phân lớp thì viết liền nhau, các AO khác phân lớp thì viết tách nhau. Thứ tự các ô orbital từ trái sang phải theo thứ tự như ở cấu hình electron.
- Điền electron vào từng ô AO theo thứ tự lớp và phân lớp, mỗi electron biểu diễn bằng 1 mũi tên.
+ Trong mỗi phân lớp, electron được phân bố sao cho số electron độc thân là lớn nhất.
+ Electron được điền vào các ô orbital theo thứ tự từ trái sang phải.
+ Trong một ô AO, electron đầu tiên được biểu diễn bằng mũi tên quay lên, electron thứ hai được biểu diễn bằng mũi tên quay xuống.
Sự sắp xếp electron trong nguyên tử O theo orbital là:

Câu 9:
13/07/2024Các nguyên tử Ne, Na và F có Z lần lượt là 10, 11 và 9. Cấu hình electron của Ne, Na+ và F- tương ứng là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
- Ne (Z = 10) có cấu hình electron: 1s22s22p6.
- Na (Z = 11) có cấu hình electron: 1s22s22p63s1
Na nhường 1 electron để tạo thành ion Na+.
Cấu hình electron của Na+ là: 1s22s22p6.
- F (Z = 9) có cấu hình electron: 1s22s22p5
F nhận 1 electron để tạo thành ion F-.
Cấu hình electron của F- là: 1s22s22p6.
Câu 10:
16/07/2024Biết rằng điện tích hạt nhân của C, N, O và F lần lượt là 6, 7, 8, 9. Ghép mỗi cấu hình electron ở cột A với nguyên tử/ ion thích hợp ở cột B.
|
Cột A |
Cột B |
|
a) 1s22s2 b) 1s22s22p4 c) 1s22s22p5 d) 1s22s22p6 |
1. O 2. C2+ 3. N3- 4. F 5. C2- |
 Xem đáp án
Xem đáp án
a ghép với 2; b ghép với 1; c ghép với 4; d ghép với 3.
Giải thích:
1. O (Z = 8) có cấu hình electron 1s22s22p4.
2. C (Z = 6) có cấu hình electron 1s22s22p2
C nhường 2 electron được ion C2+ có cấu hình electron: 1s22s2.
3. N (Z = 7) có cấu hình electron 1s22s22p3
N nhận 3 electron được ion N3- có cấu hình electron 1s22s22p6.
4. F (Z = 9) có cấu hình electron: 1s22s22p5.
Câu 11:
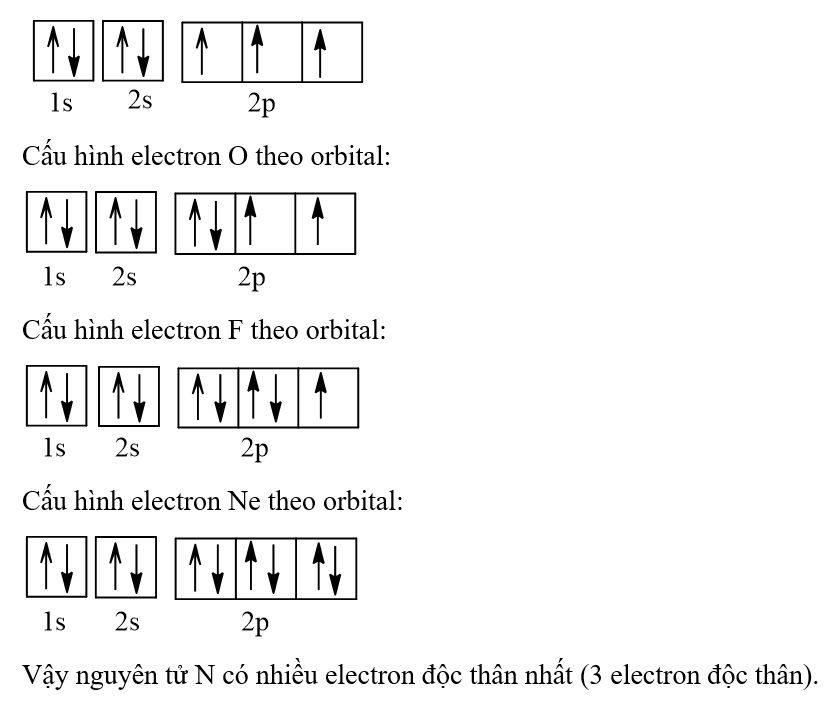
22/07/2024Trong các nguyên tử N (Z = 7), O (Z = 8), F (Z = 9) và Ne (Z = 10), nguyên tử có nhiều electron độc thân nhất là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Cấu hình electron N theo orbital:
Câu 12:
13/07/2024Nối mỗi cấu hình electron của nguyên tử ở cột A với các loại nguyên tố hóa học thích hợp ở cột B.
|
Cột A |
Cột B |
|
a) 1s22s22p6 b) 1s22s22p5 c) 1s22s22p63s1 d) 1s22s22p63s23p3 |
1. Kim loại 2. Phi kim 3. Khí hiếm |
 Xem đáp án
Xem đáp án
a ghép với 3; b và d ghép với 2; c ghép với 1.
Giải thích:
a) 1s22s22p6: Nguyên tử có 8 electron ở lớp ngoài cùng nên là nguyên tử của nguyên tố khí hiếm.
b) 1s22s22p5: Nguyên tử có 7 electron ở lớp ngoài cùng nên là nguyên tử của nguyên tố phi kim.
c) 1s22s22p63s1: Nguyên tử có 1 electron ở lớp ngoài cùng nên là nguyên tử của nguyên tố kim loại.
d) 1s22s22p63s23p3: Nguyên tử có 5 electron ở lớp ngoài cùng nên là nguyên tử của nguyên tố phi kim.
Câu 13:
13/07/2024Cấu hình electron của một nguyên tử được biểu diễn dưới dạng các ô orbital như sau:
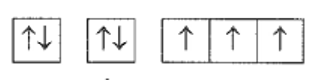
Số electron hóa trị và tính chất đặc trưng của nguyên tố hóa học này là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Dựa vào cấu hình electron theo orbital ta có cấu hình electron nguyên tử như sau:
1s22s22p3.
Vậy nguyên tử có 5 electron hóa trị, là phi kim (do có 5 electron ở lớp ngoài cùng).
Câu 14:
21/07/2024Cho các cấu hình electron của một số nguyên tử nguyên tố như sau:
(1) 1s22s22p6
(2) 1s22s22p63s2
(3) 1s22s22p63s23p63d64s2
(4) 1s22s22p63s23p63d14s2
(5) 1s22s22p63s23p4
(6) 1s22s22p63s23p5
Số lượng các nguyên tố kim loại trong số các nguyên tố ở trên là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các nguyên tử có 1, 2, 3 electron ở lớp ngoài cùng thường là nguyên tử của nguyên tố kim loại.
Các nguyên tố kim loại là:
(2) 1s22s22p63s2
(3) 1s22s22p63s23p63d64s2
(4) 1s22s22p63s23p63d14s2
Câu 15:
13/07/2024Từ các nguyên tử có thể tạo ra các ion bằng cách thêm hoặc bớt electron từ nguyên tử đó.
a) Oxygen là nguyên tố chiếm tỉ lệ phần trăm khối lượng cao nhất trong cơ thể con người (khoảng 65%). Hãy viết cấu hình electron của O và O2- (Z = 8). Cho biết để hình thành ion O2-, nguyên tử O sẽ nhận thêm electron vào orbital nào. Xác định số electron độc thân trong nguyên tử và ion này.
 Xem đáp án
Xem đáp án
a) Nguyên tử O (Z = 8) có cấu hình electron: 1s22s22p4
Biểu diễn dưới dạng ô AO:
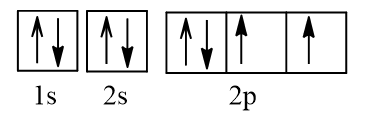
Vậy nguyên tử O có 2 electron độc thân.
O nhận 2 electron vào AO 2p hình thành nên ion O2- có cấu hình electron:
1s22s22p6.
Biểu diễn dưới dạng ô AO:
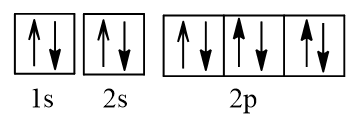
Ion O2- không có electron độc thân nào.
Câu 16:
22/07/2024b) Nhôm (aluminium) được sử dụng phổ biến trong đời sống (chế tạo dụng cụ nhà bếp, cửa, …) cũng như công nghiệp (chế tạo một số bộ phận của máy bay). Hãy biểu diễn cấu hình electron của Al và ion Al3+ (Z = 13) dưới dạng ô orbital. Cho biết để tạo thành ion Al3+, nguyên tử Al sẽ mất đi electron từ orbital nào. Xác định số electron độc thân trong các nguyên tử và ion này.
 Xem đáp án
Xem đáp án
b) Nguyên tử Al (Z = 13) có cấu hình electron: 1s22s22p63s23p1.
Biểu diễn dưới dạng ô orbital:
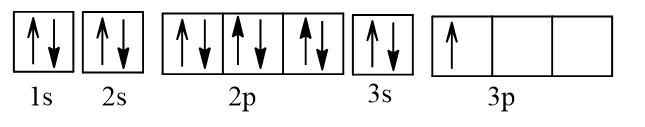
Vậy Al có 1 electron độc thân.
Nguyên tử Al nhường đi 3 electron từ các orbital 3p, 3s để tạo thành ion Al3+ có cấu hình electron: 1s22s22p6.
Biểu diễn dưới dạng ô orbital:
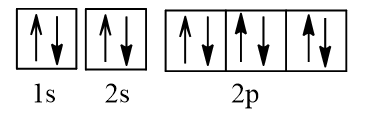
Vậy ion Al3+ không có electron độc thân nào.
Câu 17:
23/07/2024Hãy cho biết những nguyên tử và ion (cation mang điện tích 1+, 2+ hoặc anion mang điện tích 1-, 2-) nào có cấu hình electron là 1s22s22p6.
 Xem đáp án
Xem đáp án
Số lượng electron trong cấu hình 1s22s22p6 là 10 electron.
- Nếu đây là cấu hình electron của nguyên tử thì nguyên tử phải có 10 electron, do đó Z = 10, đó là nguyên tử Ne.
- Nếu đây là cấu hình electron của cation Mn+ (n = 1, 2) thì cation này được tạo ra từ nguyên tử M bằng cách tách đi n electron:
M → Mn+ (10 electron) + ne
Vậy số electron trong nguyên tử M là: 10 + n.
+ Nếu n = 1, M có 11 electron nên Z = 11 ⇒ ion Na+ có cấu hình electron: 1s22s22p6.
+ Nếu n = 2, M có 12 electron nên Z = 12 ⇒ ion Mg2+ có cấu hình electron: 1s22s22p6.
- Nếu đây là ion Xn- (n = 1, 2) thì anion này được tạo ra từ X bằng cách nhận vào n electron.
Vậy số electron trong nguyên tử X là: 10 – n.
+ Nếu n = 1, X có 9 electron nên Z = 9 ⇒ ion F- có cấu hình electron: 1s22s22p6.
+ Nếu n = 2, X có 8 electron nên Z = 8 ⇒ ion O2- có cấu hình electron: 1s22s22p6.
Câu 18:
13/07/2024Tại một khu vực của Úc, gia súc không phát triển mạnh mặc dù có thức ăn thô xanh thích hợp. Một cuộc điều tra cho thấy nguyên nhân là do không có đủ cobalt trong đất. Cobalt tạo thành cation ở hai dạng là Co2+ và Co3+ (Z = 27). Viết cấu hình electron của hai cation này và sơ đồ phân bố các electron vào các ô orbital. Cho biết số electron độc thân trong mỗi ion.
 Xem đáp án
Xem đáp án
Co có Z = 27 nên có cấu hình electron là: 1s22s22p63s23p63d74s2.
Khi Co mất đi 2 electron và 3 electron sẽ lần lượt tạo ra: Co2+ và Co3+. Các electron sẽ tách đi từ các lớp ngoài rồi tới lớp trong. Cấu hình electron của hai ion này là:
Co2+: 1s22s22p63s23p63d7
Co3+: 1s22s22p63s23p63d6
Sơ đồ phân bố electron vào các ô orbital:
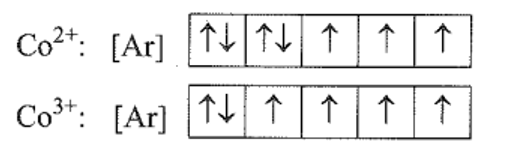
Số electron độc thân trong Co2+ và Co3+ lần lượt là 3 và 4.
Câu 19:
18/07/2024Bromine (Z = 35) dễ phản ứng, trong khi krypton (Z = 36) tương đối trơ về mặt hóa học. Giải thích sự khác biệt này dựa trên cấu hình electron của chúng.
 Xem đáp án
Xem đáp án
- Cấu hình electron của bromine (Z = 35): [Ar]3d104s24p5.
Nguyên tử bromine có 7 electron ở lớp ngoài cùng là phi kim điển hình.
- Cấu hình electron của krypton (Z = 36): [Ar]3d104s24p6.
Nguyên tử krypton có 8 electron ở lớp ngoài cùng nên là khí hiếm.
Câu 20:
17/07/2024Cũng giống như nam châm, mỗi nguyên tử/ ion cũng có thể có từ tính (bị nam châm hút). Nếu nguyên tử/ ion có electron độc thân thì nó có từ tính và được gọi là chất thuận từ. Ngược lại, nguyên tử/ ion nếu không có electron độc thân thì được gọi là chất nghịch từ. Hãy giải thích vì sao nguyên tử Cu (Z = 29) thuận từ nhưng ion Cu+ lại nghịch từ.
 Xem đáp án
Xem đáp án
- Cấu hình electron của Cu (Z = 29): 1s22s22p63s23p63d104s1.
Viết gọn: [Ar]3d104s1.
Biểu diễn dưới dạng ô orbital nguyên tử:
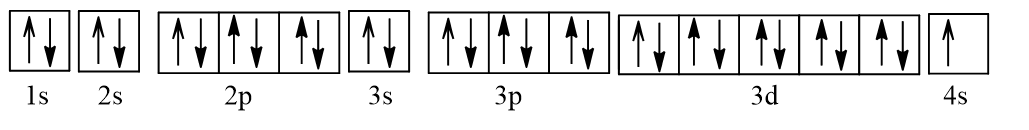
Như vậy Cu có 1 electron độc thân nên thuận từ.
- Cu nhường đi 1 electron tạo thành ion Cu+ có cấu hình electron: 1s22s22p63s23p63d10.
Viết gọn: [Ar]3d10.
Biểu diễn dưới dạng ô orbital nguyên tử:
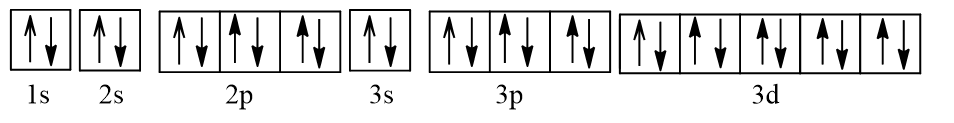
Như vậy Cu+ không có electron độc thân nên nghịch từ.
