Bài tập Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học có đáp án
Bài tập Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học có đáp án 31 lượt xem 23 câu hỏi
-
6142 lượt thi
-
23 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
14/07/2024Hầu như mọi phản ứng hóa học cũng như quá trình chuyển thể của chất luôn kèm theo sự thay đổi năng lượng.

Trong cả 2 ví dụ đều có phản ứng xảy ra với sự thay đổi năng lượng. Theo em, phản ứng có kèm theo sự thay đổi năng lượng dưới dạng nhiệt năng đóng vai trò gì trong đời sống?
 Xem đáp án
Xem đáp án
Phản ứng có kèm theo sự thay đổi năng lượng dưới dạng nhiệt năng đóng vai trò rất quan trọng trong đời sống.
Ví dụ:
- Phản ứng đốt cháy than tỏa một lượng nhiệt lớn giúp đun nấu và sưởi ấm.
C + O2 →t° CO2
- Phản ứng thủy phân collagen thành gelatin (là một loại protein dễ tiêu hóa) diễn ra khi hầm xương động vật là phản ứng thu nhiệt.
Câu 2:
23/07/2024Viết phương trình hóa học của phản ứng xảy ra ở Hình 13.1 và nêu nhận xét về sự thay đổi nhiệt của phản ứng đó

 Xem đáp án
Xem đáp án
- Phương trình hóa học của phản ứng nhiệt nhôm để hàn đường ray:
2Al + Fe2O3 Al2O3 + 2Fe
- Nhận xét về sự thay đổi nhiệt: Phản ứng tỏa nhiệt rất lớn (trên 2 500oC)
Câu 3:
21/07/2024Thực hiện thí nghiệm 1. Nêu hiện tượng xảy ra. Rút ra kết luận về sự thay đổi nhiệt độ chất lỏng trong cốc. Giải thích.
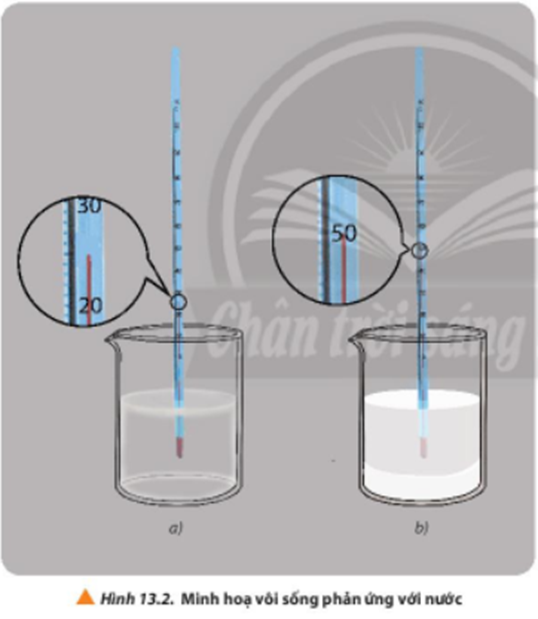
Thí nghiệm 1: Sự thay đổi nhiệt độ khi vôi sống phản ứng với nước.
Dụng cụ và thiết bị: Cốc chịu nhiệt 500 mL, cân, nhiệt kế, đũa thủy tinh, giá đỡ nhiệt kế.
Hóa chất: Vôi sống (CaO), nước cất.
Tiến hành:
Bước 1: Cho khoảng 25 mL nước cất vào cốc chịu nhiệt, đặt bầu nhiệt kế vào trong lòng chất lỏng (Hình 13.2a), ghi nhận giá trị nhiệt độ.
Bước 2: Cân khoảng 5g CaO. Cho nhanh CaO vào cốc, bắt đầu bấm giờ và ghi nhận nhiệt độ, đồng thời dùng đũa thủy tinh khuấy nhẹ (Hình 13.2b).
Bước 3: Ghi nhận giá trị nhiệt độ sau khoảng 2 phút.
 Xem đáp án
Xem đáp án
- Hiện tượng:
+ Ở bước 1 ghi nhận giá trị của nhiệt kế là khoảng 25oC.
+ Ở bước 2, CaO màu trắng tan trong nước, nhiệt độ tăng dần trên trên nhiệt kế.
+ Sau 2 phút ghi nhận giá trị của nhiệt kế là khoảng 50oC.
- Kết luận: Nhiệt độ chất lỏng trong cốc tăng lên từ 25oC đến 50oC
- Giải thích: CaO đã phản với nước theo phương trình: CaO + H2O → Ca(OH)2
Phản ứng này tỏa nhiệt nên làm nhiệt độ chất lỏng trong cốc tăng.
Câu 4:
22/07/2024Hãy nêu hiện tượng của các quá trình: đốt cháy than, ethanol trong không khí. Nhiệt độ môi trường xung quanh thay đổi như thế nào?
 Xem đáp án
Xem đáp án
- Hiện tượng: Cả hai quá trình đều xuất hiện khí bay ra.
- Phương trình hóa học:
+ Đốt cháy than: C + O2 CO2
+ Đốt cháy ethanol: C2H5OH + 3O2 2CO2 + 3H2O
- Cả hai quá trình trên đều làm nhiệt độ môi trường xung quanh tăng lên.
Câu 5:
22/07/2024Khi thả viên vitamin C sủi vào cốc nước như Hình 13.3, em hãy dự đoán sự thay đổi nhiệt độ của nước trong cốc

 Xem đáp án
Xem đáp án
Dự đoán sự thay đổi nhiệt độ của nước trong cốc:
Nhiệt độ của nước trong cốc sẽ giảm đi (hay nước sẽ mát hơn).
Câu 6:
14/07/2024 Xem đáp án
Xem đáp án
Trong phản ứng nung đá vôi (CaCO3), nếu ngừng cung cấp nhiệt, phản ứng không tiếp tục xảy ra.
Câu 7:
22/07/2024Thực hiện thí nghiệm 2. Nêu hiện tượng trước và sau khi đốt nóng hỗn hợp. Nếu ngừng đốt nóng thì phản ứng có xảy ra không?
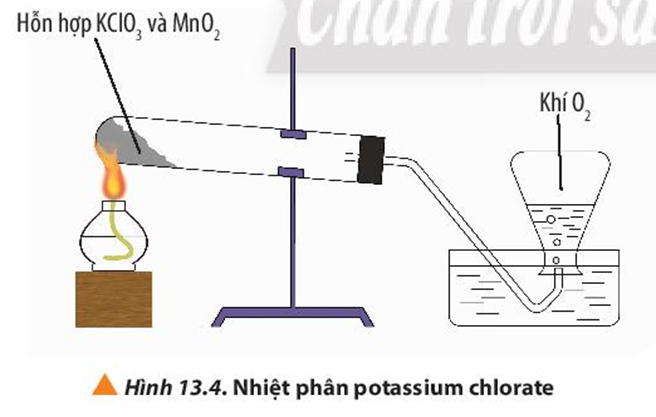
Thí nghiệm 2: Nhiệt phân potassium chlorate
Dụng cụ và thiết bị: Đèn cồn, ống nghiệm chịu nhiệt, nút cao su có gắn ống dẫn khí, chậu thủy tinh, bình tam giác, giá sắt.
Hóa chất: Potassium chlorate (KClO3), manganese dioxide (MnO2)
Tiến hành:
Bước 1: Trộn đều khoảng 4 g tinh thể KClO3 đã được nghiền nhỏ với 1 g MnO2. Cho hỗn hợp vào ống nghiệm chịu nhiệt, khô. Đậy ống nghiệm vào nút có gắn ống dẫn khí. Lắp hệ thống như Hình 13.4. Quan sát hiện tượng.
Bước 2: Dùng đèn cồn hơ nóng đều nửa đáy ống nghiệm, sau đó đun tập trung ở phần có chứa hóa chất. Quan sát hiện tượng.
Phương trình hóa học của phản ứng:
2KClO3(s) 3O2(g) + 2KCl(s)
 Xem đáp án
Xem đáp án
- Hiện tượng:
+ Trước khi đốt nóng hỗn hợp không có hiện tượng gì xảy ra.
+ Sau khi đốt nóng, có bọt khí nổi lên và đẩy nước ra khỏi bình tam giác
- Nếu ngừng đốt nóng thì phản ứng dừng lại, khí không được sinh ra thêm nữa.
Câu 8:
22/07/2024Biến thiên enthalpy chuẩn của một phản ứng hóa học được xác định trong điều kiện nào?
 Xem đáp án
Xem đáp án
Biến thiên enthalpy chuẩn của một phản ứng hóa học được xác định trong điều kiện chuẩn: Áp suất 1 bar (đối với chất khí), nồng độ 1 mol/L (đối với chất tan trong dung dịch) và thường chọn nhiệt độ 25oC (hay 298K).
Câu 9:
23/07/2024Phương trình nhiệt hóa học cho biết thông tin gì về phản ứng hóa học
 Xem đáp án
Xem đáp án
Phương trình nhiệt hóa học cho biết:
- Nhiệt phản ứng (Nhiệt lượng tỏa ra hay thu vào của phản ứng).
∆rH > 0 ⇒ Phản ứng thu nhiệt.
∆rH < 0 ⇒ Phản ứng tỏa nhiệt.
- Trạng thái của các chất đầu (cđ) và sản phẩm (sp).
(s): rắn
(aq): dung dịch
(l): lỏng
(g): khí.
Câu 10:
21/07/2024Cho hai phương trình nhiệt hóa học sau:
C(s) + H2O(g) CO(g) + H2(g) ∆ r= +131,25 kJ (1)
CuSO4 (aq) + Zn(s) → ZnSO4(aq) + Cu(s) ∆ r= -231,04 kJ (2)
Trong hai phản ứng trên, phản ứng nào là thu nhiệt, phản ứng nào là tỏa nhiệt?
 Xem đáp án
Xem đáp án
Phản ứng (1) là thu nhiệt vì ∆ r = +131,25 kJ > 0
Phản ứng (2) là tỏa nhiệt vì ∆ r = -231,04 kJ < 0
Câu 11:
19/07/2024Phân biệt enthalpy tạo thành của một chất và biến thiên enthalpy của phản ứng. Lấy ví dụ minh họa
 Xem đáp án
Xem đáp án
|
Enthalpy tạo thành của một chất |
Enthalpy của phản ứng |
|
- Chỉ tạo thành 1 mol chất. - Các chất tham gia phải ở dạng đơn chất bền nhất. |
- Sản phẩm có thể là 1 hay nhiều chất. - Các chất tham gia có thể ở dạng đơn chất hoặc hợp chất. |
|
Ví dụ: C (graphite) + O2(g) CO2 ∆ f(CO2, g) = -393,50 kJ/mol Carbon dạng graphite, oxygen dạng phân tử khí là các dạng đơn chất bền nhất của carbon và oxygen. |
Ví dụ: C2H5OH(l) + 3O2(g) 2CO2(g) + 3H2O(l) ∆r= -1366,89 kJ |
Câu 12:
21/07/2024Cho phản ứng sau:
S(s) + O2(g) SO2(g)
∆ f(SO2, g) = -296,80 kJ/mol
Cho biết ý nghĩa của giá trị ∆ f(SO2, g)

 Xem đáp án
Xem đáp án
∆ f(SO2, g) = -296,80 kJ/mol là lượng nhiệt tỏa ra khi tạo ra 1 mol SO2(g) từ các đơn chất ở trạng thái bền ở điều kiện chuẩn (sulfur ở trạng thái rắn, oxygen dạng phân tử khí chính là các dạng đơn chất bền nhất của sulfur và oxygen).
Câu 13:
16/07/2024Hợp chất SO2(g) bền hơn hay kém bền hơn về mặt năng lượng so với các đơn chất bền S(s) và O2(g)
 Xem đáp án
Xem đáp án
∆ f(SO2, g) = -296,80 kJ/mol < 0
⇒ Hợp chất SO2(g) bền hơn về mặt năng lượng so với các đơn chất bền S(s) và O2(g).
Câu 14:
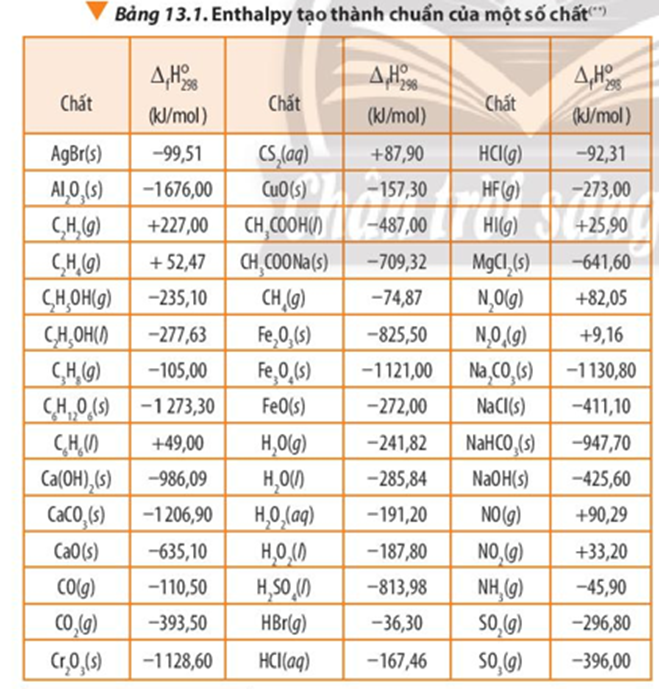
23/07/2024Từ Bảng 13.1 hãy liệt kê các phản ứng có enthalpy tạo thành dương (lấy nhiệt từ môi trường)
 Xem đáp án
Xem đáp án
Các phản ứng có enthalpy tạo thành dương (lấy nhiệt từ môi trường):
Phản ứng tạo thành các chất: C2H2(g), C2H4(g), C6H6(l), CS2(aq), HI(g), N2O(g), N2O4(g), NO(g), NO2(g).
Câu 15:
14/07/2024Em hãy xác định enthalpy tạo thành theo đơn vị (kcal) của các chất sau: Fe2O3(s), NO(g), H2O(g), C2H5OH(l). Cho biết 1J = 0,239 cal
 Xem đáp án
Xem đáp án
1J = 0,239 cal
⇒ 1 kJ = 0,239 kcal
∆ f(Fe2O3, s) = -825,50 kJ/mol = -825,50 . 0,239 kcal/mol = -197,29 kcal/mol
∆ f(NO, g) = +90,29 kJ/mol = +21,58 kcal/mol
∆ f(H2O, g) = -241,82 kJ/mol = -57,79 kcal/mol
∆ f(C2H5OH, l) = -277,63 kJ/mol = -66,35 kcal/mol
Câu 16:
22/07/2024Quan sát Hình 13.5, mô tả sơ đồ biểu diễn biến thiên enthalpy của phản ứng. Nhận xét về giá trị của ∆ f(sp) so với ∆ f(cđ)

 Xem đáp án
Xem đáp án
Biến thiên enthalpy của phản ứng: ∆ r = -111,68 kJ < 0
∆ f(sp) < ∆ f(cđ)
Câu 17:
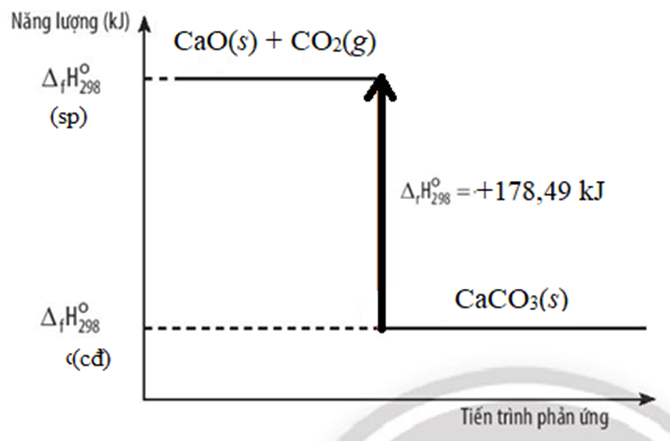
23/07/2024Vận dụng để vẽ sơ đồ biểu diễn biến thiên enthalpy của phản ứng nhiệt phân CaCO3 ở Ví dụ 5.
 Xem đáp án
Xem đáp án
CaCO3(s) CaO(s) + CO2(g) ∆ r = +178,49 kJ
Sơ đồ biểu diễn biến thiên enthalpy của phản ứng nhiệt phân CaCO3
Câu 18:
22/07/2024Cho hai phương trình nhiệt hóa học sau:
CO(g) + O2(g) → CO2(g) ∆ r = -283,00 kJ (1)
H2(g) + F2(g) → 2HF(g) ∆ r = -546,00 kJ (2)
So sánh nhiệt giữa hai phản ứng (1) và (2). Phản ứng nào xảy ra thuận lợi hơn?
 Xem đáp án
Xem đáp án
Nhiệt phản ứng (2) (∆ r = -546,00 kJ) âm hơn nhiệt phản ứng (1) (∆ r = -283,00 kJ)
⇒ Phản ứng (2) xảy ra thuận lợi hơn.
Câu 19:
20/07/2024Hãy làm cho nhà em sạch bong với hỗn hợp baking soda (NaHCO3) và giấm (CH3COOH). Hỗn hợp này tạo ra một lượng lớn bọt. Phương trình nhiệt hóa học của phản ứng:
NaHCO3(s) + CH3COOH(aq) → CH3COONa(aq) + CO2(g) + H2O(l) ∆ r= 94,30kJ
Phản ứng trên là tỏa nhiệt hay thu nhiệt? Vì sao? Tìm những ứng dụng khác của phản ứng trên.

 Xem đáp án
Xem đáp án
NaHCO3(s) + CH3COOH(aq) → CH3COONa(aq) + CO2(g) + H2O(l) ∆ r = 94,30kJ
- Phản ứng trên là thu nhiệt vì ∆ r= 94,30kJ > 0
- Một số ứng dụng khác của phản ứng trên:
+ Thông tắc cống, bồn cầu, máy giặt, bồn rửa bát,…
+ Làm xốp bánh.
+ Tẩy trắng quần áo, giày dép, răng miệng.
+ Vệ sinh cơ thể, tẩy tế bào chết cho da.
+ Hút ẩm giày, tủ quần áo.
Câu 20:
14/07/2024Phương trình nhiệt hóa học giữa nitrogen và oxygen như sau:
N2(g) + O2(g) → 2NO(g) ∆ r= +180 kJ
Kết luận nào sau đây đúng?
A. Nitrogen và oxygen phản ứng mạnh hơn khi ở nhiệt độ thấp.
B. Phản ứng tỏa nhiệt.
C. Phản ứng xảy ra thuận lợi ở điều kiện thường.
D. Phản ứng hóa học xảy ra có sự hấp thụ nhiệt năng từ môi trường.
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
∆ r= +180 kJ > 0
⇒ Phản ứng hóa học xảy ra có sự hấp thụ nhiệt năng từ môi trường
Câu 21:
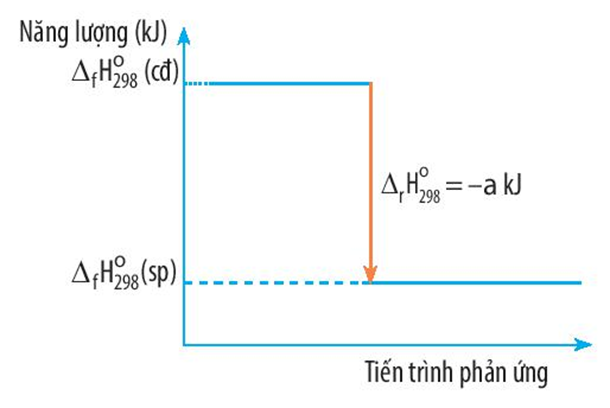
21/07/2024Biến thiên enthalpy của một phản ứng được ghi ở sơ đồ dưới. Kết luận nào sau đây là đúng?
A. Phản ứng tỏa nhiệt
B. Năng lượng chất tham gia phản ứng nhỏ hơn năng lượng chất sản phẩm
C. Biến thiên enthalpy của phản ứng là a kJ/mol
D. Phản ứng thu nhiệt
 Xem đáp án
Xem đáp án
Phản ứng có biến thiên enthalpy là ∆ r = -a kJ < 0 ⇒ Phản ứng tỏa nhiệt
Năng lượng chất tham gia phản ứng lớn hơn năng lượng chất sản phẩm.
Câu 22:
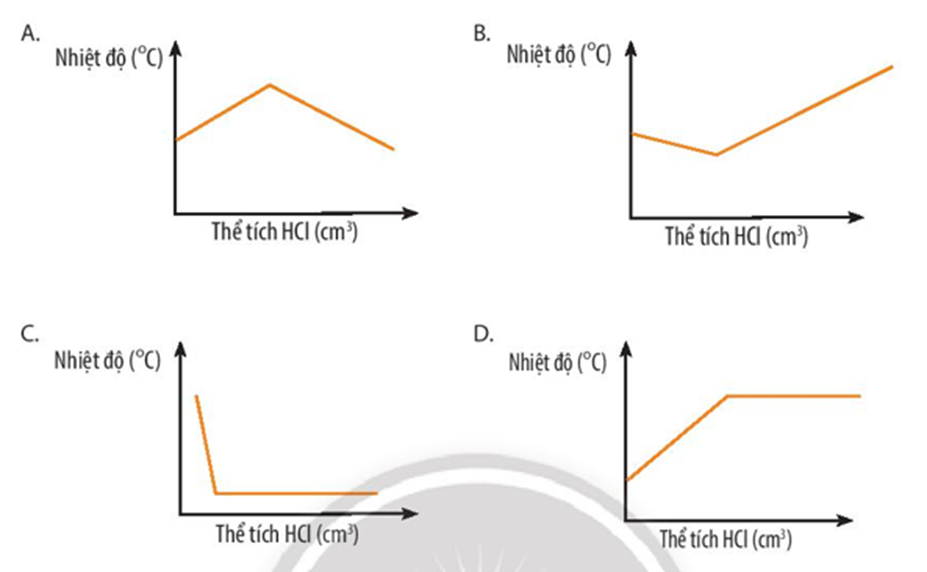
23/07/2024Đồ thị nào sau đây thể hiện đúng sự thay đổi nhiệt độ khi dung dịch hydrochloric acid được cho vào dung dịch sodium hydroxide tới dư?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phản ứng giữa hydrochloric acid (HCl) và sodium hydroxide (NaOH) là phản ứng tỏa nhiệt (∆ r= -57,3 kJ).
Khi hydrochloric acid (HCl) phản ứng với sodium hydroxide (NaOH) nhiệt độ tăng dần. Đến khi phản ứng kết thúc, nhiệt độ sẽ giảm dần để cân bằng với nhiệt độ môi trường.
Câu 23:
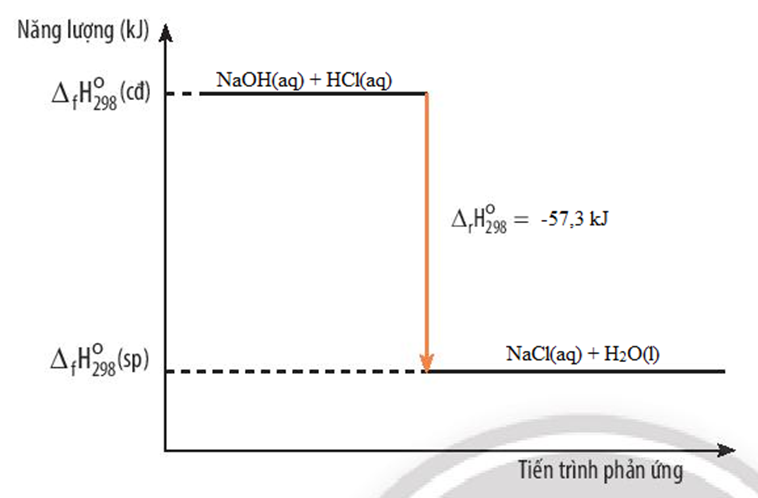
23/07/2024Cho phương trình nhiệt hóa học sau:
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l) ∆ r = -57,3 kJ
Vẽ sơ đồ biểu diễn biến thiên enthalpy của phản ứng
 Xem đáp án
Xem đáp án
Sơ đồ biểu diễn biến thiên enthalpy của phản ứng:
Có thể bạn quan tâm
- Trắc nghiệm Hóa học 10 Bài 13. Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học có đáp án (1819 lượt thi)
