50 Bài tập Cấu tạo nguyên tử cơ bản cực hay có lời giải
50 Bài tập Cấu tạo nguyên tử cơ bản cực hay có lời giải (P2)
-
370 lượt thi
-
25 câu hỏi
-
25 phút
Danh sách câu hỏi
Câu 1:
22/07/2024Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
 Xem đáp án
Xem đáp án
Đáp án C
Có số p = số e= = 17
Số hạt mang điện nhiều hơn số hạt không mang điện là 16 → n = 17.2 - 16 = 18
Vậy số khối của X là A= n + p = 18 + 17 = 35
Số hiệu nguyên tử của X là Z= p = 17
Vậy kí hiệu của X là .
Câu 2:
21/07/2024Tổng điện tích lớp vỏ của nguyên tử R có điện tích bằng -32.10-19C. Nguyên tố R là
 Xem đáp án
Xem đáp án
Đáp án B
R có số electron =
→ R có số hiệu nguyên tử Z = 20 → Ca
Câu 3:
03/07/2024Tổng số hạt trong nguyên tử một nguyên tố R là 36. Số hạt mang điện gấp đôi hạt không mang điện. R là
 Xem đáp án
Xem đáp án
Đáp án A
Giả sử số hiệu nguyên tử, số hạt nơtron trong nguyên tử của nguyên tố lần lượt là Z, N.
Ta có hpt:
→ R là Mg.
Câu 4:
21/07/2024Nguyên tử của nguyên tố X có tổng số hạt là 40. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 12 hạt. Nguyên tố X có số khối là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giả sử số hiệu nguyên tử, số nơtron trong nguyên tử của nguyên tố X lần lượt là Z, N.
Ta có hệ phương trình:
⇔
Vậy nguyên tố X có số khối là
A = Z + N = 13 + 14 = 27
Câu 5:
19/07/2024Tổng các hạt cơ bản trong một nguyên tử là 82 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Số khối của nguyên tử đó là
 Xem đáp án
Xem đáp án
Đáp án B
Giả sử số hiệu nguyên tử, số nơtron trong nguyên tử của nguyên tố X lần lượt là Z, N.
Ta có hpt:
→ Nguyên tử X có số khối: A = Z + N = 26 + 30 = 56
Câu 6:
23/07/2024Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 49, trong đó số hạt không mang điện bằng 53,125% số hạt mang điện. Điện tích hạt nhân của X là:
 Xem đáp án
Xem đáp án
Đáp án D
Giả sử số hiệu nguyên tử, số nơtron trong nguyên tử của nguyên tố X lần lượt là Z, N.
Ta có hpt:
→ Điện tích hạt nhân của X là 16+
Câu 7:
22/07/2024Nguyên tử của một nguyên tố có tổng số hạt proton, nơtron, electron là 122. Số hạt mang điện trong hạt nhân ít hơn số hạt không mang điện là 11 hạt. Số khối của nguyên tử trên là:
 Xem đáp án
Xem đáp án
Đáp án C
Giả sử số hiệu nguyên tử, số nơtron trong nguyên tử của nguyên tố X lần lượt là Z, N.
Ta có hpt:
→ Nguyên tử X có số khối: A = Z + N = 37 + 48 = 85
Câu 8:
21/07/2024Mệnh đề nào sau đây không đúng ?
(1) Số điện tích hạt nhân đặc trưng cho 1 nguyên tố.
(2) Chỉ có hạt nhân nguyên tử oxi mới có 8 proton.
(3) Chỉ có hạt nhân nguyên tử oxi mới có 8 nơtron.
(4) Chỉ có trong nguyên tử oxi mới có 8 electron.
 Xem đáp án
Xem đáp án
Đáp án D
(3) sai vì hạt nhân của nguyên tử cũng có 8 nơtron.
Có 3 mệnh đề đúng là (1), (2), (4)
Câu 9:
21/07/2024Điều khẳng định nào sau đây là sai?
 Xem đáp án
Xem đáp án
Đáp án A
Hạt nhân của hầu hết các nguyên tử được cấu tạo bởi proton và nơtron.
Câu 11:
11/07/2024Nguyên tố hóa học là những nguyên tử có cùng
 Xem đáp án
Xem đáp án
Chọn đáp án C
Nguyên tố hóa học là tập hợp những nguyên tử cùng loại, có cùng số proton trong hạt nhân.
Câu 12:
12/07/2024Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Đáp án C
Vì nguyên tử là hạt trung hòa về điện nên trong một nguyên tử số proton luôn bằng số electron
Câu 13:
18/07/2024Phát biểu nào dưới đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án C
A đúng. Nguyên tử gồm lớp vỏ electron mang điện tích âm và hạt nhân nguyên tử mang điện tích dương.
B đúng. mp = 1,6726. 10-27 kg; mn = 1,6748. 10-27 kg.
C sai vì trong một nguyên tử, nếu biết số proton và số khối thì ta mới có thể suy ra số nơtron.
D đúng vì trong một nguyên tử số proton = số electron.
Câu 14:
22/07/2024Phát biểu nào dưới đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án A
Số khối, kí hiệu A, bằng tổng số proton (Z) và tổng số nơtron (N).
A = Z + N
Câu 15:
08/07/2024Một nguyên tố hoá học có thể có nhiều nguyên tử có khối lượng khác nhau vì lí do nào dưới đây?
 Xem đáp án
Xem đáp án
Đáp án B
Vì hạt nhân của các nguyên tử có cùng số proton nhưng khác nhau về số nơtron, do đó khối lượng của chúng khác nhau.
Câu 16:
04/07/2024Số hiệu nguyên tử của các nguyên tố cho biết
 Xem đáp án
Xem đáp án
Đáp án D
Số hiệu nguyên tử = số đơn vị điện tích hạt nhân = số proton = số electron.
Câu 17:
11/11/2024Trong một nguyên tử
 Xem đáp án
Xem đáp án
Đáp án đúng là : D
-Trong một nguyên tử tổng số proton và số nơtron được gọi là số khối.
- Loại A vì số proton luôn bằng số electron, rất ít trường hợp bằng số nơtron.
- Loại B vì tổng điện tích các proton và electron = 0.
- Loại C vì số khối A là khối lượng gần đúng của nguyên tử do bỏ qua khối lượng của các hạt electron không đáng kể.
→ D đúng.A,B,C sai.
* Thành phần nguyên tử
- Mọi vật thể đều được tạo nên từ các chất và mọi chất đều được tạo nên từ các nguyên tử.
- Nguyên tử được tạo nên từ 3 loại hạt cơ bản là:
+ Hạt electron, kí hiệu là e
+ Hạt proton, kí hiệu là p
+ Hạt neutron, kí hiệu là n
- Khối lượng và điện tích các hạt cơ bản này được thể hiện trong Bảng 2.1.
Bảng 2.1. Khối lượng và điện tích của các hạt cấu tạo nên nguyên tử
|
Loại hạt |
Electron |
Proton |
Neutron |
|
Khối lượng (amu) |
0,00055 |
1 |
1 |
|
Điện tích (e0) |
-1 |
+1 |
0 |
- Trong một nguyên tử, số proton và số electron luôn bằng nhau.
- Trong tất cả các nguyên tố, chỉ có duy nhất một loại nguyên tử của hydrogen (H) được tạo nên bởi proton và electron (không có neutron).
Chú ý:
+ Đơn vị của khối lượng nguyên tử là amu (atomic mass unit)
1 amu = 1,6605.10-27 kg
+ Đơn vị của điện tích các hạt cơ bản là e0 (điện tích nguyên tố)
1 e0 = 1,602.10-19 C
2. Cấu trúc của nguyên tử
Nguyên tử bao gồm:
+ Lớp vỏ: được tạo nên bởi các hạt electron
+ Hạt nhân: được tạo nên bởi các hạt proton và hạt neutron
Ví dụ: Mô hình cấu tạo nguyên tử hydrogen và beryllium
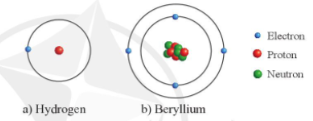
II. Khối lượng và kích thước của nguyên tử
Nguyên tử của các nguyên tố khác nhau có khối lượng và kích thước khác nhau
1. Khối lượng của nguyên tử
- Khối lượng của nguyên tử vô cùng nhỏ.
- Khối lượng nguyên tử thường được biểu thị theo đơn vị amu
- Nguyên tử có khối lượng nhỏ nhất là nguyên tử của nguyên tố hydrogen (H), có khối lượng là 1 amu
- Nguyên tử có khối lượng lớn nhất là nguyên tử của nguyên tố uranium (U), có khối lượng là 238 amu
- Do khối lượng của các electron (0,00055 amu) rất nhỏ so với khối lượng của proton (1 amu) hay neutron (1 amu) nên khối lượng nguyên tử tập trung chủ yếu ở hạt nhân nguyên tử. Một cách gần đúng, có thể coi khối lượng của nguyên tử bằng khối lượng của hạt nhân.
2. Kích thước của nguyên tử
- Kích thước của nguyên tử là vô cùng nhỏ
- Coi nguyên tử có dạng hình cầu, khi đó, đường kính của nó chỉ khoảng 10-10 m
- Nguyên tử có đường kính nhỏ nhất là helium (0,62), nguyên tử có đường kính lớn nhất là francium (7,0)
Chú ý: Angstrom là đơn vị đo độ dài, kí hiệu là ![]()
1 = 102 pm = 10-10 m
- Hạt nhân nguyên tử có kích thước rất nhỏ so với nguyên tử. Kích thước hạt nhân bằng khoảng 10-5 đến 10-4 lần kích thước nguyên tử. Như vậy, phần không gian rỗng chiếm chủ yếu trong nguyên tử.
Xem thêm các bài viết liên quan,chi tiết khác:
Lý thuyết Hóa học 10 Bài 2: Các thành phần của nguyên tử
Giải bài tập Hóa 10 Bài 2: Thành phần của nguyên tử
Câu 18:
17/07/2024Chọn mệnh đề đúng trong các mệnh đề sau?
 Xem đáp án
Xem đáp án
Đáp án A
A đúng. 11H có 1 proton → N = A - Z = 1 - 1 = 0 → không chứa nơtron.
Loại B vì nguyên tố 11H có hạt nhân nguyên tử không chứa nơtron.
Loại C vì 73X có tổng số hạt mang điện (= 6) nhiều hơn số hạt không mang điện (= 4) là 2.
Loại D vì nguyên tử 73X có 3 electron và 4 nơtron.
Câu 19:
03/07/2024Phát biểu nào sau đây là sai?
 Xem đáp án
Xem đáp án
Đáp án A
A sai vì nguyên tử trong hạt nhân chỉ có 1 proton và không có nơtron.
Câu 20:
18/07/2024Nguyên tử nguyên tố X có tổng số các hạt p, n, e là 58, trong hạt nhân số hạt p và n hơn kém nhau 1 đơn vị. Số hiệu nguyên tử của X là
 Xem đáp án
Xem đáp án
Đáp án A
Theo bài ra có:
P + N + E = 58 2P + N = 58 (vì P = E)
Lại có N - P = 1 (chú ý N luôn lớn hơn hoặc bằng P)
P = 19 Số hiệu nguyên tử của X là 19
Câu 21:
22/07/2024Nguyên tử của nguyên tố R có 56e và 81n. Kí hiệu nguyên tử nào sau đây là của nguyên tố R
 Xem đáp án
Xem đáp án
Đáp án A
Nguyên tử R có số hiệu nguyên tử Z = số e = 56.
Số khối A = Z + N = 56 + 81 = 137.
→ Kí hiệu:
Câu 22:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Trong nguyên tử số p = số e.
Tổng số hạt trong nguyên tử là 20 → 2p + n= 20
Số hạt không mang điện nhiều hơn số hạt mang điện dương là 2 đơn vị → n - p= 2
Giải hệ → n = 8, p = 6
Số khối của X là A= n + p = 8 + 6 = 14.
Câu 23:
15/07/2024Số proton và số nơtron có trong một ion lần lượt là
 Xem đáp án
Xem đáp án
Đáp án A
Trong 1 nguyên tử Fe: p = e = 26, n = 56 - 26 = 30
Trong ion : p = 26, n = 30, e = 24.
Bài thi liên quan
-
50 Bài tập Cấu tạo nguyên tử cơ bản cực hay có lời giải (P1)
-
25 câu hỏi
-
25 phút
-
