Giải Vật lí 12 Bài 9 (Kết nối tri thức): Định luật Boyle
Với giải bài tập Vật lí 12 Bài 9: Định luật Boyle sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Vật lí 12 Bài 9.
Giải Vật lí 12 Bài 9: Định luật Boyle
Khởi động trang 37 Vật lí 12: Khi thay đổi thể tích của một khối lượng khí xác định ở nhiệt độ không đổi thì áp suất khí thay đổi như thế nào?
Lời giải:
Với một lượng khí nhất định, ở nhiệt độ không đổi, áp suất và thể tích tỉ lệ nghịch với nhau. Tích số của áp suất và thể tích luôn không đổi.
I. Các thông số trạng thái của một lượng khí
Câu hỏi (trang 37)
Các thông số trạng thái của một lượng khí đều là đại lượng có thể đo hoặc xác định được bằng các dụng cụ đo lường.
Câu hỏi 1 trang 37 Vật lí 12: Người ta dùng các dụng cụ nào để đo, xác định các thông số trạng thái của lượng khí trong hộp kín ở Hình 9.1?
Lời giải:
Áp kế: Dùng để đo áp suất khí trong hộp kín.
Nhiệt kế: Dùng để đo nhiệt độ khí trong hộp kín.
Xylanh: Dùng để đo thể tích khí trong hộp kín.
Câu hỏi 2 trang 37 Vật lí 12: Nêu tên đơn vị của các đại lượng này trong hệ SI.
Lời giải:
|
Đại lượng |
Ký hiệu |
Đơn vị SI |
|
Áp suất |
p |
Pascal (Pa) |
|
Nhiệt độ |
T |
Kelvin (K) |
|
Thể tích |
V |
Mét khối (m3) |
Câu hỏi trang 37 Vật lí 12: Hãy so sánh các thông số trạng thái của không khí trong một quả bóng bay đã được bơm khi để trong bóng mát và khi để ngoài nắng (Hình 9.3).
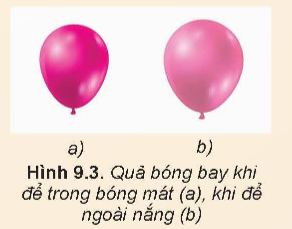
Lời giải:
|
Đại lượng |
Bóng mát |
Ngoài nắng |
|
Áp suất |
p₁ |
p₂ (P₂ > P₁) |
|
Nhiệt độ |
T₁ |
T₂ (T₂ > T₁) |
|
Thể tích |
V₁ |
V₂ (V₂ > V₁) |
II. Định luật Boyle
Hoạt động trang 38 Vật lí 12: Chuẩn bị: Bộ thí nghiệm về chất khí
- Xi lanh trong suốt có độ chia nhỏ nhất 0,5 cm3 (1).
- Pit-tông có ống nối khí trong xi lanh với áp kế (2).
- Áp kế có độ chia nhỏ nhất 0,05.105 Pa (3).
- Giá đỡ thí nghiệm (4).
- Thước đo (5).
Tiến hành:
- Bố trí thí nghiệm như Hình 9.4.

- Dịch chuyển từ từ pit-tông để làm thay đổi thể tích khí.
- Đọc và ghi kết quả thí nghiệm vào vở tương tự mẫu ở Bảng 9.1.
Bảng 9.1. Ví dụ về kết quả thí nghiệm khảo sát mối quan hệ của thể tích và áp suất trong quá trình đẳng nhiệt của một lượng khí xác định
| Lần thí nghiệm | V (cm3) | p (105 Pa) |
| 1 | 3,0 | 1,0 |
| 2 | 2,5 | 1,2 |
| 3 | 2,0 | 1,5 |
| 4 | 1,5 | 1,9 |
Từ kết quả thí nghiệm ở Bảng 9.1, thực hiện các yêu cầu sau:
1. Xác định giá trị của tích pV trong mỗi lần thí nghiệm.
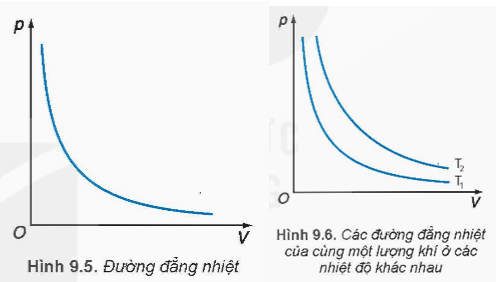
2. Vẽ đường biểu diễn sự phụ thuộc của áp suất p vào thể tích V trong hệ toạ độ (p,V).
3. Phát biểu mối quan hệ giữa p và V trong quá trình đẳng nhiệt.
Lời giải:
1.
p1V1 = 3,0.1,0 = 3,0
p2V2 = 2,5.1,2 = 3,0
p3V3 = 2,0.1,5 = 3,0
p4V4 = 1,5.1,9 = 2,85
2.
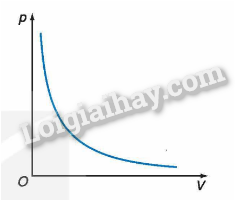
3. Trong quá trình đẳng nhiệt của một lượng khí nhất định, tích của áp suất và thể tích luôn không đổi.
Câu hỏi 1 trang 39 Vật lí 12: Nếu vẽ đường biểu diễn sự phụ thuộc của p vào thì đường biểu diễn sẽ có dạng như thế nào? Tại sao?
Lời giải:
Biểu diễn p và :
- Dạng đường biểu diễn: Đường thẳng.
- Lý do:
+ Theo định luật Boyle (Mariotte): pV = const
+ Biến đổi công thức:
+ Vẽ đồ thị:
Trục hoành:
Trục tung: p
Các điểm (, p₁) và (, p₂) nằm trên đường thẳng.
Câu hỏi 2 trang 39 Vật lí 12: Tìm ví dụ về quá trình đẳng nhiệt trong đời sống.
Lời giải:
Ví dụ về quá trình đẳng nhiệt:
- Bơm xe đạp: Khi ta ấn pit-tông, thể tích khí giảm, áp suất khí tăng. Quá trình này diễn ra ở nhiệt độ môi trường không đổi (gần như đẳng nhiệt).
- Bình xịt khử trùng: Khí bên trong bình được nén dưới áp suất cao. Khi ta ấn nút, van mở, khí thoát ra ngoài, thể tích khí tăng. Do có van điều tiết, áp suất khí giảm dần, nhưng nhiệt độ khí gần như không đổi (gần như đẳng nhiệt).
- Nén khí trong bình: Khi nén khí, thể tích khí giảm, áp suất khí tăng. Quá trình này có thể được thực hiện gần như đẳng nhiệt bằng cách sử dụng nước để làm mát bình khí.
Bài tập vận dụng (trang 40)
Vận dụng 1 trang 40 Vật lí 12: Một quả bóng chứa 0,04 m3 không khí ở áp suất 120 kPa. Tính áp suất của không khí trong bóng khi làm giảm thể tích bóng còn 0,025 m3 ở nhiệt độ không đổi.
Lời giải:
Ta có:
p₁V₁ = p₂V₂ =>
Vận dụng 2 trang 40 Vật lí 12: Một bọt khí nổi từ đáy giếng sâu 6 m lên mặt nước. Khi lên tới mặt nước, thể tích của bọt khí tăng lên bao nhiêu lần? Coi áp suất khí quyển là 1,013.105 Pa; khối lượng riêng của nước giếng là 1 003 kg/m3 và nhiệt độ của nước giếng không thay đổi theo độ sâu.
Lời giải:
Áp suất tại đáy giếng:
p₁ = p₀ + hρg = 1,013.105+6.1003.9,81 = 1,592.105 Pa
Áp dụng định luật Boyle:
p₁V₁ = p₂V₂ =>
Thể tích của bọt khí tăng lên 1,57 lần khi lên tới mặt nước.
Lý thuyết Vật lí 12 Bài 9: Định luật Boyle
I. Các thông số trạng thái của một lượng khí
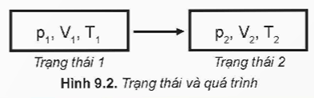
Trạng thái của một khối lượng khí nhất định được xác định bằng ba thông số trạng thái của khối khí: thể tích V, áp suất p và nhiệt độ tuyệt đối T.
Quá trình khối khí biến đổi từ trạng thái này sang trạng thái khác gọi là quá trình biến đổi trạng thái.
II. Định luật Boyle
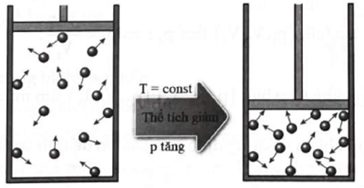
1. Quá trình đẳng nhiệt
Quá trình biến đổi trạng thái của một khối lượng khí xác định khi nhiệt độ giữ không đổi được gọi là quá trình đẳng nhiệt. Thí nghiệm về quá trình đẳng nhiệt sẽ giúp ta xác định được mối quan hệ giữa áp suất p và thể tích V của một khối lượng khí xác định trong quá trình này.
2. Thí nghiệm khảo sát quá trình đẳng nhiệt
Lập bảng kết quả:
|
p (kPa) |
V (cm3) |
|
PV (kPa.cm3) |
|
110 |
43,6 |
0,023 |
4796 |
|
120 |
40,0 |
0,025 |
4800 |
|
130 |
36,9 |
0,027 |
4797 |
|
140 |
34,3 |
0,029 |
4802 |
2. Định luật Boyle
Với khối luợng khí xác định, khi giữ nhiệt độ của khí không đổi thì áp suất p gây ra bởi khí tỉ lệ nghịch với thể tích V của nó.
pV = hằng số
Định luật Boyle được ứng dụng trong nhiều lĩnh vực như:
• Chế tạo các dụng cụ như bơm xe đạp, bình cứu hỏa, phao cứu sinh, ...
• Hóa lỏng khí để bảo quản và vận chuyển.
• Lặn biển.
Sơ đồ tư duy Định luật Boyle

Xem thêm các chương trình khác:
- Soạn văn 12 Kết nối tri thức (hay nhất)
- Văn mẫu 12 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 12 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn 12 - Kết nối tri thức
- Bố cục tác phẩm Ngữ văn 12 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn 12 – Kết nối tri thức
- Giải sgk Toán 12 – Kết nối tri thức
- Giải Chuyên đề học tập Toán 12 – Kết nối tri thức
- Lý thuyết Toán 12 – Kết nối tri thức
- Giải sbt Toán 12 – Kết nối tri thức
- Bài tập Tiếng Anh 12 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 12 - Global success
- Trọn bộ Từ vựng Tiếng Anh 12 Global success đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 12 Global success đầy đủ nhất
- Giải sbt Tiếng Anh 12 – Global Success
- Giải sgk Hóa học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Hóa 12 – Kết nối tri thức
- Lý thuyết Hóa 12 – Kết nối tri thức
- Giải sbt Hóa 12 – Kết nối tri thức
- Chuyên đề dạy thêm Hóa 12 cả 3 sách (chương trình mới 2025)
- Giải sgk Sinh học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Sinh học 12 – Kết nối tri thức
- Lý thuyết Sinh học 12 – Kết nối tri thức
- Giải sbt Sinh học 12 – Kết nối tri thức
- Giải sgk Lịch sử 12 – Kết nối tri thức
- Giải Chuyên đề học tập Lịch sử 12 – Kết nối tri thức
- Giải sbt Lịch sử 12 – Kết nối tri thức
- Giải sgk Địa lí 12 – Kết nối tri thức
- Giải Chuyên đề học tập Địa lí 12 – Kết nối tri thức
- Giải sbt Địa lí 12 – Kết nối tri thức
- Giải sgk Tin học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Tin học 12 – Kết nối tri thức
- Giải sbt Tin học 12 – Kết nối tri thức
- Lý thuyết Tin học 12 - Kết nối tri thức
- Giải sgk Công nghệ 12 – Kết nối tri thức
- Giải sgk Kinh tế pháp luật 12 – Kết nối tri thức
- Giải Chuyên đề học tập Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sbt Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng 12 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 12 – Kết nối tri thức