Giải Vật lí 12 Bài 11 (Kết nối tri thức): Phương trình trạng thái của khí lí tưởng
Với giải bài tập Vật lí 12 Bài 11: Phương trình trạng thái của khí lí tưởng sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Vật lí 12 Bài 11.
Giải Vật lí 12 Bài 11: Phương trình trạng thái của khí lí tưởng
Khởi động trang 45 Vật lí 12: Các định luật Boyle và Charles chỉ xác định mối liên hệ giữa hai cặp thông số "áp suất - thể tích" và "thể tích - nhiệt độ" của một khối lượng khí xác định. Vậy, làm thế nào để xác định được mối liên hệ của cả ba thông số trạng thái của một khối lượng khí xác định?
Lời giải:
Định luật Boyle và Charles chỉ xác định mối liên hệ giữa hai cặp thông số trạng thái (áp suất, thể tích và nhiệt độ) của một khối lượng khí xác định. Để xác định mối liên hệ của cả ba thông số, ta cần sử dụng phương trình trạng thái của khí lí tưởng:
pV = nRT
I. Phương trình trạng thái của khí lí tưởng
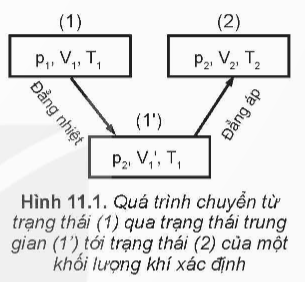
Hoạt động trang 45 Vật lí 12: Hãy dựa vào các định luật Boyle, Charles và Hình 11.1 về quá trình chuyến trạng thái của một khối lượng khí xác định để lập phương trình dưới đây về mối liên hệ giữa ba thông số trạng thái của một khối lượng khí xác định:
= hằng số
Độ lớn của hăng số trên phụ thuộc vào lượng khí ta xét.
Lời giải:
- Định luật Boyle:
p₁V₁ = p₂V₂ => (khi T = const)
- Định luật Charles:
(khi p = const)
- Hình 11.1:
Quá trình biến đổi trạng thái từ (p₁, V₁, T₁) đến (p₂, V₂, T₂).
Câu hỏi 1 trang 45 Vật lí 12: Hãy lập phương trình bằng một cách biến đổi trạng thái khác cách trong Hình 11.1 để chứng tỏ: Quá trình chuyển trạng thái không phụ thuộc cách chuyển trạng thái mà chỉ phụ thuộc trạng thái đầu và trạng thái cuối.
Lời giải:
Lập phương trình chứng tỏ quá trình chuyển trạng thái không phụ thuộc cách chuyển trạng thái:
- Cách biến đổi trạng thái khác trong Hình 11.1:
+ Chọn trạng thái trung gian (1') với áp suất p' và thể tích V₂.
+ Áp dụng định luật Boyle cho quá trình đẳng nhiệt (1) → (1'): p₁V₁ = p'V₂
+ Áp dụng định luật Charles cho quá trình đẳng áp (1') → (2): V₂/T₁ = V₂/T₂
Thay V₂ từ hai phương trình trên vào nhau:
So sánh với phương trình (11.1):
Ta thấy hai phương trình có dạng tương tự nhau, chỉ khác nhau ở ký hiệu áp suất (p' thay cho p₂).
Câu hỏi 2 trang 45 Vật lí 12: Tại sao không gọi phương trình (11.1) là phương trình trạng thái của chất khí mà lại gọi là phương trình trạng thái của khí lí tưởng?
Lời giải:
Lý do không gọi phương trình (11.1) là phương trình trạng thái của chất khí:
- Phương trình (11.1):
- Lý do không gọi phương trình (11.1) là phương trình trạng thái của chất khí:
+ Phương trình (11.1) chỉ áp dụng cho khí lí tưởng.
+ Khí lí tưởng là khí giả định, có các tính chất: Các phân tử khí có kích thước bằng 0. Lực tương tác giữa các phân tử khí bằng 0. Các phân tử khí chuyển động hỗn loạn, va chạm hoàn toàn đàn hồi.
+ Trên thực tế, không có khí nào hoàn toàn là khí lí tưởng.
+ Các khí thực đều có: Kích thước phân tử. Lực tương tác giữa các phân tử.
Do đó, phương trình (11.1) chỉ là phương trình trạng thái gần đúng của chất khí.
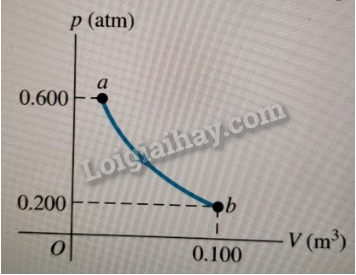
Hoạt động 1 trang 45 Vật lí 12: Hãy biểu diễn bằng đồ thị trong hệ toạ độ (p - V) các quá trình chuyển trạng thái vẽ ở Hình 11.1.
Lời giải:
Hoạt động 2 trang 45 Vật lí 12: Từ phương trình trạng thái của khí lí tưởng suy ra hệ thức liên hệ giữa áp suất và nhiệt độ tuyệt đối trong quá trình đẳng tích.
Lời giải:
pV = nRT
Quá trình đẳng tích: Thể tích khí không đổi (V = const)
II. Vận dụng
Hoạt động 1 trang 47 Vật lí 12: Bóng thám không. Bóng thám không được sử dụng để thu thập thông tin về môi trường không khí và thời tiết. Bóng thường được bơm khí hiếm nhẹ hơn không khí, nhờ đó có thể bay lên các tầng không khí khác nhau để thu thập thông tin về nhiệt độ, độ ẩm, áp suất, tốc độ gió,...
Người ta muốn chế tạo một bóng thám không có thể tăng bán kính lên tới 10 m khi bay ở tầng khí quyển có áp suất 0,3.105 Pa và nhiệt độ 200 K. Hỏi bán kính của bóng khi vừa bơm xong phải bằng bao nhiêu? Biết bóng được bơm ở áp suất 1,02.105 Pa và nhiệt độ 300 K.
Lời giải:
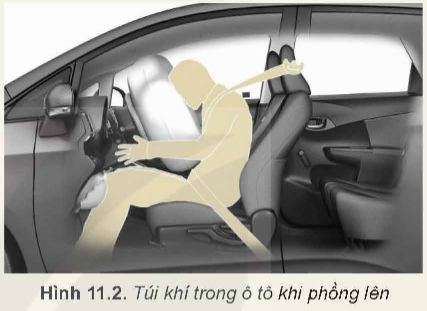
Hoạt động 2 trang 47 Vật lí 12: Túi khí. Trong ô tô, người ta thường đặt ở hệ thống tay lái một thiết bị nhằm bảo vệ người lái xe khi xe gặp tai nạn, gọi là "túi khí". Túi khí được chế tạo bằng vật liệu co giãn, chịu được áp suất lớn. Trong túi khí thường chứa chất NaN3 khi xe va chạm mạnh vào vật cản thì hệ thống cảm biến của xe sẽ kích thích chất rắn này làm nó phân huy tạo thành Na và khí N2. Khí N2 được tao thành có tác dung làm phồng túi lên, giúp người lái xe không bị va chạm trực tiếp vào hệ thống lái (Hình 11.2).
a) Viết phương trình phân hủy NaN3.
b) Tính lượng chất khí N2 được giải phóng khi xảy ra phản ứng phân hủy NaN3, biết trong túi chứa 100 g NaN3 và thể tích mol là 24,0 lít /mol.
c) Biết thể tích túi khí khi phồng lên có độ lớn tới 48 lít. Bỏ qua thể tích khí có trong túi trước khi phồng lên và thể tích của Na được tạo thành trong túi do phản ứng phân huỷ. Tính áp suất của khí N2 trong túi khí khi đã phòng lên, biết nhiệt độ là 30 °C.
Lời giải:
a) 2NaN3 → 2Na + 3N2
b)
c)
T = 30 + 273,15 = 303,15 K
pV = nRT
Lý thuyết Vật lí 12 Bài 11: Phương trình trạng thái của khí lí tưởng
I. Phương trình trạng thái của khí lí tưởng
1. Phương trình trạng thái của một lượng khí xác định
Phương trình trạng thái khí lý tưởng mô tả mối quan hệ giữa áp suất, thể tích, nhiệt độ và số mol của chất khí: hằng số.
2. Phương trình Claperon – Mendeleev
Phương trình: còn được gọi là phương trình Claperon - Mendeleev.
* Trong đó:
• n là số mol: với (m là khối lượng, M là khối lượng mol);
• R hằng số khí, hệ SI: R = 8,31 (J/kg.K); hệ hỗn hợp
II. Vận dụng
Mô hình khí lý tưởng được sử dụng rộng rãi trong nhiều lĩnh vực khác nhau, bao gồm:
Kỹ thuật: Mô hình này được sử dụng để thiết kế động cơ, máy nén khí, hệ thống lạnh,...
Hóa học: Tính toán các phản ứng hóa học, xác định thành phần của hỗn hợp khí,...
Vật lý: Được sử dụng để nghiên cứu các hiện tượng vật lý như sự khuếch tán, dẫn nhiệt,...
Dự báo thời tiết: Mô hình khí lý tưởng được sử dụng trong dự báo thời tiết
Hàng không: Tính toán hiệu suất của máy bay và thiết kế các bộ phận khí động học.
Sơ đồ tư duy Phương trình trạng thái của khí lí tưởng

Xem thêm các chương trình khác:
- Soạn văn 12 Kết nối tri thức (hay nhất)
- Văn mẫu 12 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 12 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn 12 - Kết nối tri thức
- Bố cục tác phẩm Ngữ văn 12 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn 12 – Kết nối tri thức
- Giải sgk Toán 12 – Kết nối tri thức
- Giải Chuyên đề học tập Toán 12 – Kết nối tri thức
- Lý thuyết Toán 12 – Kết nối tri thức
- Giải sbt Toán 12 – Kết nối tri thức
- Bài tập Tiếng Anh 12 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 12 - Global success
- Trọn bộ Từ vựng Tiếng Anh 12 Global success đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 12 Global success đầy đủ nhất
- Giải sbt Tiếng Anh 12 – Global Success
- Giải sgk Hóa học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Hóa 12 – Kết nối tri thức
- Lý thuyết Hóa 12 – Kết nối tri thức
- Giải sbt Hóa 12 – Kết nối tri thức
- Chuyên đề dạy thêm Hóa 12 cả 3 sách (chương trình mới 2025)
- Giải sgk Sinh học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Sinh học 12 – Kết nối tri thức
- Lý thuyết Sinh học 12 – Kết nối tri thức
- Giải sbt Sinh học 12 – Kết nối tri thức
- Giải sgk Lịch sử 12 – Kết nối tri thức
- Giải Chuyên đề học tập Lịch sử 12 – Kết nối tri thức
- Giải sbt Lịch sử 12 – Kết nối tri thức
- Giải sgk Địa lí 12 – Kết nối tri thức
- Giải Chuyên đề học tập Địa lí 12 – Kết nối tri thức
- Giải sbt Địa lí 12 – Kết nối tri thức
- Giải sgk Tin học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Tin học 12 – Kết nối tri thức
- Giải sbt Tin học 12 – Kết nối tri thức
- Lý thuyết Tin học 12 - Kết nối tri thức
- Giải sgk Công nghệ 12 – Kết nối tri thức
- Giải sgk Kinh tế pháp luật 12 – Kết nối tri thức
- Giải Chuyên đề học tập Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sbt Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng 12 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 12 – Kết nối tri thức
