Để xác định phần trăm khối lượng của hỗn hợp A gồm nhôm và magie
Với giải bài 6 trang 58 sgk Hóa học lớp 9 được biên soạn lời giải chi tiết sẽ giúp học sinh biết cách làm bài tập môn Hóa 9. Mời các bạn đón xem:
Giải Hóa 9 Bài 18: Nhôm
Video Giải Bài 6* trang 58 Hóa học lớp 9
Bài 6* trang 58 Hóa học lớp 9: Để xác định phần trăm khối lượng của hỗn hợp A gồm nhôm và magie, người ta thực hiện hai thí nghiệm sau:
– Thí nghiệm 1: Cho m gam hỗn hợp A tác dụng với dung dịch H2SO4 loãng dư, thu được 1568 ml khí ở điều kiện tiêu chuẩn.
– Thí nghiệm 2: Cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư thì sau phản ứng thấy còn lại 0,6 gam chất rắn.
Tính phần trăm khối lượng của mỗi chất trong hỗn hợp A.
Lời giải:
Ở thí nghiệm 2: Al tác dụng hết với NaOH, còn Mg không phản ứng nên khối lượng chất rắn còn lại là Mg nên mMg = 0,6 gam.
Gọi nAl = x mol
Phương trình phản ứng:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2 ↑ ( 1)
Mg + H2SO4 → MgSO4 + H2 ↑ (2)
Từ phương (1) và (2)
Theo đề bài ta có:
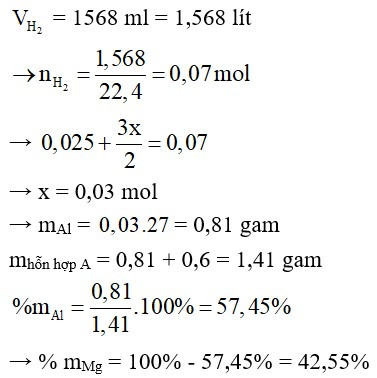
Xem thêm lời giải bài tập Hóa học lớp 9 hay, chi tiết khác:
Bài 1 trang 57 Hóa 9: Hãy điền vào bảng những tính chất tương ứng với những ứng dụng của nhôm ...
Bài 2 trang 58 Hóa 9: Thả một mảnh nhôm vào các ống nghiệm chứa các dung dịch...
Bài 3 trang 58 Hóa 9: Có nên dùng xô, chậu, nồi nhôm để đựng vôi, nước vôi tôi hoặc vữa xây dựng không...
Bài 4 trang 58 Hóa 9: Có dung dịch muối AlCl3 lẫn tạp chất là CuCl2...
Bài 5 trang 58 Hóa 9: Thành phần chính của đất sét là Al2O3.2SiO2.2H2O...
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 9 (hay nhất) | Để học tốt Ngữ văn 9 (sách mới)
- Soạn văn 9 (ngắn nhất)
- Văn mẫu 9 (sách mới) | Để học tốt Ngữ văn 9 Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 9 (sách mới) | Giải bài tập Toán 9 Tập 1, Tập 2
- Giải sbt Toán 9
- Lý thuyết Toán 9
- Các dạng bài tập Toán lớp 9
- Giáo án Toán lớp 9 mới nhất
- Bài tập Toán lớp 9 mới nhất
- Chuyên đề Toán lớp 9 mới nhất
- Giải sgk Tiếng Anh 9 (thí điểm)
- Giải sgk Tiếng Anh 9 (sách mới) | Để học tốt Tiếng Anh 9
- Giải sbt Tiếng Anh 9
- Giải sbt Tiếng Anh 9 (thí điểm)
- Giải sgk Sinh học 9 (sách mới) | Giải bài tập Sinh học 9
- Giải vở bài tập Sinh học 9
- Lý thuyết Sinh học 9
- Giải sbt Sinh học 9
- Giải sgk Vật Lí 9 (sách mới) | Giải bài tập Vật lí 9
- Giải sbt Vật Lí 9
- Lý thuyết Vật Lí 9
- Các dạng bài tập Vật lí lớp 9
- Giải vở bài tập Vật lí 9
- Giải sgk Địa Lí 9 (sách mới) | Giải bài tập Địa lí 9
- Lý thuyết Địa Lí 9
- Giải Tập bản đồ Địa Lí 9
- Giải sgk Tin học 9 (sách mới) | Giải bài tập Tin học 9
- Lý thuyết Tin học 9
- Lý thuyết Giáo dục công dân 9
- Giải vở bài tập Lịch sử 9
- Giải Tập bản đồ Lịch sử 9
- Lý thuyết Lịch sử 9
- Lý thuyết Công nghệ 9
