Câu hỏi:
11/07/2024 190
Cho enthalpy tạo thành tiêu chuẩn của các chất trong bảng sau.
Chất
C6H6 (l)
C2H5OH (l)
CH3COOH (l)
CO2 (g)
H2O (g)
ΔfHo298 (kJ/mol)
49,00
-277,63
-487,00
-393,50
-241,82
(a) Viết phương trình đốt cháy hoàn toàn C6H6, C2H5OH và CH3COOH với hệ số nguyên tối giản.
b) Chất nào trong các chất trên có biến thiên enthalpy của phản ứng lớn hơn ( ΔfHo298 âm hơn).
c) Từ kết quả tính toán hãy so sánh biến thiên enthalpy của phản ứng khi đốt cháy cùng khối lượng C6H6, C2H5OH và CH3COOH.
Cho enthalpy tạo thành tiêu chuẩn của các chất trong bảng sau.
|
Chất |
C6H6 (l) |
C2H5OH (l) |
CH3COOH (l) |
CO2 (g) |
H2O (g) |
|
ΔfHo298 (kJ/mol) |
49,00 |
-277,63 |
-487,00 |
-393,50 |
-241,82 |
(a) Viết phương trình đốt cháy hoàn toàn C6H6, C2H5OH và CH3COOH với hệ số nguyên tối giản.
b) Chất nào trong các chất trên có biến thiên enthalpy của phản ứng lớn hơn ( ΔfHo298 âm hơn).
c) Từ kết quả tính toán hãy so sánh biến thiên enthalpy của phản ứng khi đốt cháy cùng khối lượng C6H6, C2H5OH và CH3COOH.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
(a) Phương trình đốt cháy hoàn toàn các chất:
2C6H6(l) + 15O2(g) to→ 12CO2(g) + 6H2O(g) (1)
C2H5OH(l) + 3O2(g) to→ 2CO2(g) + 3H2O(g) (2)
CH3COOH(l) + 2O2 to→2CO2(g) + 3H2O(g) (3)
b) Biến thiên enthanpy của phản ứng:
C6H6(l) + 152 O2(g) to→ 6CO2(g) + 3H2O(g)
ΔrHo298= 6× ΔfHo298(CO2) + 3× ΔfHo298(H2O)- ΔfHo298(C6H6)
= 6 ×(-393,5) + 3×(-241,82) - 49,00 = -3 135,46 (kJ)
C2H5OH(l) + 3O2(g) to→2CO2(g) + 3H2O(g)
ΔrHo298= 2× ΔfHo298(CO2) + 3× ΔfHo298 (H2O)- ΔfHo298(C2H5OH)
= 2 ×(-393,5) + 3×(-241,82) – (-277,63) = -1 234,83 (kJ)
CH3COOH(l) + 2O2 to→2CO2(g) + 3H2O(g)
ΔrHo298= 2× ΔfHo298(CO2) + 3× ΔfHo298(H2O)- ΔfHo298( CH3COOH)
= 2 ×(-393,5) + 3×(-241,82) – (-487,00) = -783,64 (kJ)
c) Biết MC6H6=78; MC2H5OH=46; MCH3COOH=60.
Xét khi đốt cháy cùng khối lượng là 78 gam thì
C6H6 có ΔrHo298 =-3 135,46 kJ;
C2H5OH có ΔrHo298 = -2 093,84 kJ;
CH3COOH có ΔrHo298= -1 018,73 kJ.
Vậy khi đốt cháy cùng khối lượng thì biến thiên enthalpy của phản ứng đốt cháy các chất theo thứ tự giảm dần C6H6, C2H5OH, CH3COOH.
(a) Phương trình đốt cháy hoàn toàn các chất:
2C6H6(l) + 15O2(g) to→ 12CO2(g) + 6H2O(g) (1)
C2H5OH(l) + 3O2(g) to→ 2CO2(g) + 3H2O(g) (2)
CH3COOH(l) + 2O2 to→2CO2(g) + 3H2O(g) (3)
b) Biến thiên enthanpy của phản ứng:
C6H6(l) + 152 O2(g) to→ 6CO2(g) + 3H2O(g)
ΔrHo298= 6× ΔfHo298(CO2) + 3× ΔfHo298(H2O)- ΔfHo298(C6H6)
= 6 ×(-393,5) + 3×(-241,82) - 49,00 = -3 135,46 (kJ)
C2H5OH(l) + 3O2(g) to→2CO2(g) + 3H2O(g)
ΔrHo298= 2× ΔfHo298(CO2) + 3× ΔfHo298 (H2O)- ΔfHo298(C2H5OH)
= 2 ×(-393,5) + 3×(-241,82) – (-277,63) = -1 234,83 (kJ)
CH3COOH(l) + 2O2 to→2CO2(g) + 3H2O(g)
ΔrHo298= 2× ΔfHo298(CO2) + 3× ΔfHo298(H2O)- ΔfHo298( CH3COOH)
= 2 ×(-393,5) + 3×(-241,82) – (-487,00) = -783,64 (kJ)
c) Biết MC6H6=78; MC2H5OH=46; MCH3COOH=60.
Xét khi đốt cháy cùng khối lượng là 78 gam thì
C6H6 có ΔrHo298 =-3 135,46 kJ;
C2H5OH có ΔrHo298 = -2 093,84 kJ;
CH3COOH có ΔrHo298= -1 018,73 kJ.
Vậy khi đốt cháy cùng khối lượng thì biến thiên enthalpy của phản ứng đốt cháy các chất theo thứ tự giảm dần C6H6, C2H5OH, CH3COOH.
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Sơ đồ điều chế ethanol từ tinh bột:
Tinh bột +H2O,H+→ glucose enzyme→ ethanol
Lên men 162 gam tinh bột với hiệu suất các giai đoạn lần lượt là 80% và 90%. Tính thể tích ethanol 40° thu được. Biết khối lượng riêng của C2H5OH nguyên chất là 0,79 g/mL.
Sơ đồ điều chế ethanol từ tinh bột:
Tinh bột +H2O,H+→ glucose enzyme→ ethanol
Lên men 162 gam tinh bột với hiệu suất các giai đoạn lần lượt là 80% và 90%. Tính thể tích ethanol 40° thu được. Biết khối lượng riêng của C2H5OH nguyên chất là 0,79 g/mL.
Câu 2:
Trung hòa 100 mL dung dịch carbonxylic acid (X) nồng độ 0,1 M cần vừa đủ 16 gam dung dịch NaOH 5%, thu được 1,48 gam muối. Công thức cấu tạo của (X) là
A. HOOC-CH2-COOH.
B. HOOC-COOH.
C. CH3-COOH.
D. HOOC-CH2-CH2-COOH.
Trung hòa 100 mL dung dịch carbonxylic acid (X) nồng độ 0,1 M cần vừa đủ 16 gam dung dịch NaOH 5%, thu được 1,48 gam muối. Công thức cấu tạo của (X) là
A. HOOC-CH2-COOH.
B. HOOC-COOH.
C. CH3-COOH.
D. HOOC-CH2-CH2-COOH.
Câu 3:
Viết 4 phương trình hoá học thực hiện sơ đồ chuyển hoá sau đây:
(X) (1)→ (Y) (2)→ (Z) (3)→ (T) (4)→ (Y)
Cho biết (X), (Y), (Z) và (T) là các chất hữu cơ, trong đó (Y) có nồng độ từ 2% đến 5% thì được gọi là giấm ăn.
Viết 4 phương trình hoá học thực hiện sơ đồ chuyển hoá sau đây:
(X) (1)→ (Y) (2)→ (Z) (3)→ (T) (4)→ (Y)
Cho biết (X), (Y), (Z) và (T) là các chất hữu cơ, trong đó (Y) có nồng độ từ 2% đến 5% thì được gọi là giấm ăn.
Câu 4:
Sắp xếp theo trình tự tăng dần tính acid của các chất trong dãy sau:
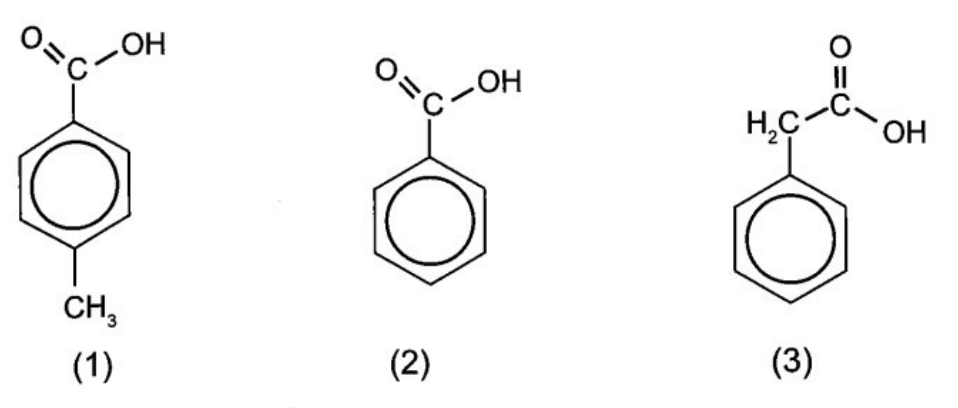
Sắp xếp theo trình tự tăng dần tính acid của các chất trong dãy sau:

Câu 5:
Cho sơ đồ phản ứng:
(X) +Cl2,500oC→ (Y) +NaOH,to→ (Z) CuO,to→ (T) +O2,to→ (Q) +CH3OH/HS2O4→ methyl acrylate
Biết (Y), (Z), (T), (Q) là các sản phẩm chính của phản ứng. Xác định tên gọi của các chất trong sơ đồ và viết phản ứng xảy ra.
Cho sơ đồ phản ứng:
(X) +Cl2,500oC→ (Y) +NaOH,to→ (Z) CuO,to→ (T) +O2,to→ (Q) +CH3OH/HS2O4→ methyl acrylate
Biết (Y), (Z), (T), (Q) là các sản phẩm chính của phản ứng. Xác định tên gọi của các chất trong sơ đồ và viết phản ứng xảy ra.
Câu 6:
Vị chua của trái cây là do các acid hữu cơ có trong đó gây nên. Trong quả táo có 2-hydroxybutane-1,4-dioic acid (malic acid), trong quả nho có 2,3-dihydroxybutanedioic acid (tartaric acid), trong quả chanh có 2-hydroxypropane-1,2,3-tricarboxylic acid (citric acid). Hãy viết công thức cấu tạo các acid đó.
Vị chua của trái cây là do các acid hữu cơ có trong đó gây nên. Trong quả táo có 2-hydroxybutane-1,4-dioic acid (malic acid), trong quả nho có 2,3-dihydroxybutanedioic acid (tartaric acid), trong quả chanh có 2-hydroxypropane-1,2,3-tricarboxylic acid (citric acid). Hãy viết công thức cấu tạo các acid đó.
Câu 7:
Giấm ăn được điều chế bằng cách lên men dung dịch ethanol loãng. Hãy tính khối lượng giấm ăn 5% thu được khi lên men 100 L ethanol 4°. Biết hiệu suất quá trình lên men là 80%, khối lượng riêng của ethanol nguyên chất là 0,79 g/mL.
Giấm ăn được điều chế bằng cách lên men dung dịch ethanol loãng. Hãy tính khối lượng giấm ăn 5% thu được khi lên men 100 L ethanol 4°. Biết hiệu suất quá trình lên men là 80%, khối lượng riêng của ethanol nguyên chất là 0,79 g/mL.
Câu 8:
Methyl salicylate trong thuốc giảm đau được điều chế bằng cách cho salicylic acid phản ứng với methanol có H2SO4 đặc làm xúc tác, đun nóng. Cho 0,1 mol methyl salicylate phản ứng với dung dịch NaOH dư, số mol NaOH đã tham gia phản ứng là
A. 0,1 mol.
B. 0,2 mol.
C. 0,3 mol.
D. 0,05 mol.
Methyl salicylate trong thuốc giảm đau được điều chế bằng cách cho salicylic acid phản ứng với methanol có H2SO4 đặc làm xúc tác, đun nóng. Cho 0,1 mol methyl salicylate phản ứng với dung dịch NaOH dư, số mol NaOH đã tham gia phản ứng là
A. 0,1 mol.
B. 0,2 mol.
C. 0,3 mol.
D. 0,05 mol.
Câu 9:
Hợp chất hữu cơ (X) có công thức phân tử là C4H6O2 nhưng chưa rõ công thức cấu tạo. Để tiến hành xác định công thức cấu tạo của chất, người ta đã thực nghiệm về tính chất của (X) thu được kết quả sau:
(X) làm quỳ tím chuyển màu đỏ;
- (X) làm mất màu nước bromine;
- Khi cho tác dụng với Na2CO3 tạo chất khí không màu.
(a) Tìm công thức cấu tạo có thể có của (X), gọi tên các đồng phân và cho biết cấu tạo nào có đồng phân hình học.
Hợp chất hữu cơ (X) có công thức phân tử là C4H6O2 nhưng chưa rõ công thức cấu tạo. Để tiến hành xác định công thức cấu tạo của chất, người ta đã thực nghiệm về tính chất của (X) thu được kết quả sau:
(X) làm quỳ tím chuyển màu đỏ;
- (X) làm mất màu nước bromine;
- Khi cho tác dụng với Na2CO3 tạo chất khí không màu.
(a) Tìm công thức cấu tạo có thể có của (X), gọi tên các đồng phân và cho biết cấu tạo nào có đồng phân hình học.
Câu 10:
Formic acid là một chất lỏng, mùi xốc mạnh và gây bỏng da, acid này được chưng cất lần đầu từ loài kiến lửa có tên là Formicarufa. Kiến khi cắn sẽ “tiêm” dung dịch chứa 50% thể tích formic acid vào da. Trung bình mỗi lần cắn, kiến có thể “tiêm” khoảng 6,0×10−3 cm3 dung dịch formic acid.
(a) Biết mỗi lần cắn, kiến “tiêm” 80% formic acid có trong cơ thể. Giả sử lượng formic acid trong các con kiến là bằng nhau. Hãy xác định thể tích formic acid tinh khiết có trong một con kiến.
(b) Để làm giảm lượng formic acid trong vết cắn, bác sĩ thường dùng thuốc có chứa thành phần là sodium hydrogencarbonate (NaHCO3). Hãy viết phương trình hoá học của phản ứng và tính khối lượng sodium hydrogencarbonate cần dùng để trung hoà hoàn toàn lượng formic acid từ vết kiến cắn (biết khối lượng riêng của formic acid là 1,22 g/cm3).
Formic acid là một chất lỏng, mùi xốc mạnh và gây bỏng da, acid này được chưng cất lần đầu từ loài kiến lửa có tên là Formicarufa. Kiến khi cắn sẽ “tiêm” dung dịch chứa 50% thể tích formic acid vào da. Trung bình mỗi lần cắn, kiến có thể “tiêm” khoảng 6,0×10−3 cm3 dung dịch formic acid.
(a) Biết mỗi lần cắn, kiến “tiêm” 80% formic acid có trong cơ thể. Giả sử lượng formic acid trong các con kiến là bằng nhau. Hãy xác định thể tích formic acid tinh khiết có trong một con kiến.
(b) Để làm giảm lượng formic acid trong vết cắn, bác sĩ thường dùng thuốc có chứa thành phần là sodium hydrogencarbonate (NaHCO3). Hãy viết phương trình hoá học của phản ứng và tính khối lượng sodium hydrogencarbonate cần dùng để trung hoà hoàn toàn lượng formic acid từ vết kiến cắn (biết khối lượng riêng của formic acid là 1,22 g/cm3).
Câu 11:
Tên gọi của CH3CH(CH3)CH2COOH là
A. 2-methylpropanoic acid.
B. 2-methylbutanoic acid,
C. 3-methylbutanoic acid.
D. 3-methylpropanoic acid
Tên gọi của CH3CH(CH3)CH2COOH là
A. 2-methylpropanoic acid.
B. 2-methylbutanoic acid,
C. 3-methylbutanoic acid.
D. 3-methylpropanoic acid
Câu 12:
Cho dung dịch acetic acid có nồng độ x% tác dụng vừa đủ với dung dịch NaOH 20% thu được dung dịch muối sodium acetate có nồng độ 10,25%. Giá trị của X là
A. 10%. B. 15%. C. 18,67%. D. 20%.
Cho dung dịch acetic acid có nồng độ x% tác dụng vừa đủ với dung dịch NaOH 20% thu được dung dịch muối sodium acetate có nồng độ 10,25%. Giá trị của X là
A. 10%. B. 15%. C. 18,67%. D. 20%.
Câu 13:
Rót 1 - 2 mL dung dịch chất (X) đậm đặc vào ống nghiệm đựng 1 - 2 mL dung dịch NaHCO3. Đưa que diêm đang cháy vào miệng ống nghiệm thì que diêm tắt. Chất (X) có thể là chất nào sau đây?
A. Ethanol.
B. Acetaldehyde.
C. Acetic acid.
D. Phenol.
Rót 1 - 2 mL dung dịch chất (X) đậm đặc vào ống nghiệm đựng 1 - 2 mL dung dịch NaHCO3. Đưa que diêm đang cháy vào miệng ống nghiệm thì que diêm tắt. Chất (X) có thể là chất nào sau đây?
A. Ethanol.
B. Acetaldehyde.
C. Acetic acid.
D. Phenol.
Câu 14:
Benzoic acid được sử dụng như một chất bào quản thực phẩm (kí hiệu là E-210) cho xúc xích, nước sốt cà chua, mù tạt, bơ thực vật,… vì có tác dụng ức chế sự phát triển của nấm mốc, nấm men và một số vi khuẩn. Công thức của benzoic acid là
A. CH3COOH.
B. C6H5COOH.
C. HOOC-COOH.
D. HCOOH.
Benzoic acid được sử dụng như một chất bào quản thực phẩm (kí hiệu là E-210) cho xúc xích, nước sốt cà chua, mù tạt, bơ thực vật,… vì có tác dụng ức chế sự phát triển của nấm mốc, nấm men và một số vi khuẩn. Công thức của benzoic acid là
A. CH3COOH.
B. C6H5COOH.
C. HOOC-COOH.
D. HCOOH.
Câu 15:
Cho các chất sau: (1) C3H8, (2) C2H5OH, (3) CH3CHO, (4) CH3COOH. Thứ tự các chất theo chiều tăng dần nhiệt độ sôi từ trái sang phải là
A. (1), (2), (3), (4). B. (4), (3), (2), (1).
C. (1), (2), (4), (3). D. (1), (3), (2), (4).
Cho các chất sau: (1) C3H8, (2) C2H5OH, (3) CH3CHO, (4) CH3COOH. Thứ tự các chất theo chiều tăng dần nhiệt độ sôi từ trái sang phải là
A. (1), (2), (3), (4). B. (4), (3), (2), (1).
C. (1), (2), (4), (3). D. (1), (3), (2), (4).


