Câu hỏi:
20/07/2024 3,434Cho các phát biểu sau
(1) Phản ứng tỏa nhiệt là phản ứng hóa học trong đó có sự giải phóng nhiệt năng ra môi trường.
(2) Phản ứng thu nhiệt là phản ứng hóa học trong đó có sự hấp thụ nhiệt năng từ môi trường.
(3) Phản ứng tỏa nhiệt là phản ứng hóa học trong đó có sự hấp thụ nhiệt năng từ môi trường.
(4) Phản ứng thu nhiệt là phản ứng hóa học trong đó có sự giải phóng nhiệt năng ra môi trường.
Các phát biểu đúng là
A. (1) và (2);
B. (1) và (4);
C. (2) và (3);
D. (3) và (4).
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: A
Các phát biểu đúng là
(1) Phản ứng tỏa nhiệt là phản ứng hóa học trong đó có sự giải phóng nhiệt năng ra môi trường.
(2) Phản ứng thu nhiệt là phản ứng hóa học trong đó có sự hấp thụ nhiệt năng từ môi trường.
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Cho biết phản ứng tạo thành 2 mol HCl (g) ở điều kiện chuẩn tỏa ra 184,62 kJ:
H2 (g) + Cl2 (g)⟶ 2HCl (g) (*)
Những phát biểu nào dưới đây đúng?
(1) Enthalpy tạo thành chuẩn của HCl (g) là − 184,62 kJ/mol.
(2) Biến thiên enthalpy chuẩn của phản ứng (*) là − 184,62 kJ.
(3) Enthalpy tạo thành chuẩn của HCl (g) là – 92,31 kJ/mol.
(4) Biến thiên enthalpy chuẩn của phản ứng (*) là 184,62 kJ.
Câu 2:
Cho phản ứng: N2 (g) + 3H2 (g) ⟶ 2NH3 (g)
Ở điều kiện chuẩn, cứ 1 mol N2 phản ứng hết sẽ tỏa ra 91,8 kJ. Enthalpy tạo thành chuẩn của NH3 là
Câu 3:
Cho các phản ứng dưới đây:
(1) CO (g) +  O2 (g) ⟶ CO2 (g)
O2 (g) ⟶ CO2 (g)  = − 283 kJ
= − 283 kJ
(2) C (s) + H2O (g)  CO (g) + H2 (g)
CO (g) + H2 (g)  = + 131,25 kJ
= + 131,25 kJ
(3) H2 (g) + F2 (g) ⟶ 2HF (g)  = − 546 kJ
= − 546 kJ
(4) H2 (g) + Cl2 (g)⟶ 2HCl (g)  = − 184,62 kJ
= − 184,62 kJ
Phản ứng xảy ra thuận lợi nhất là
Câu 4:
Cho 2 phương trình nhiệt hóa học sau:
C (s) + H2O (g)  CO (g) + H2 (g)
CO (g) + H2 (g)  = + 131,25 kJ (1)
= + 131,25 kJ (1)
CuSO4 (aq) + Zn (s)  ZnSO4 (aq) + Cu (s)
ZnSO4 (aq) + Cu (s)  = −231,04 kJ (2)
= −231,04 kJ (2)
Khẳng định đúng là
Câu 5:
Cho  (Fe2O3, s) = − 825,5 kJ/mol. Biết 1 J = 0,239 cal. Enthalpy tạo thành chuẩn theo đơn vị (kcal) của Fe2O3 (s) là
(Fe2O3, s) = − 825,5 kJ/mol. Biết 1 J = 0,239 cal. Enthalpy tạo thành chuẩn theo đơn vị (kcal) của Fe2O3 (s) là
Câu 6:
Phản ứng nào trong các phản ứng dưới đây là phản ứng thu nhiệt?
Câu 8:
Phương trình nhiệt hóa học giữa nitrogen và oxygen như sau:
N2 (g) + O2 (g) ⟶ 2NO (g)  = +180 kJ
= +180 kJ
Kết luận nào sau đây đúng?
Câu 10:
Enthalpy tạo thành của một chất (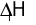 ) là nhiệt kèm theo phản ứng tạo thành
) là nhiệt kèm theo phản ứng tạo thành
Câu 11:
Biến thiên enthalpy của một phản ứng được ghi ở sơ đồ dưới đây. Kết luận nào sau đây là đúng?
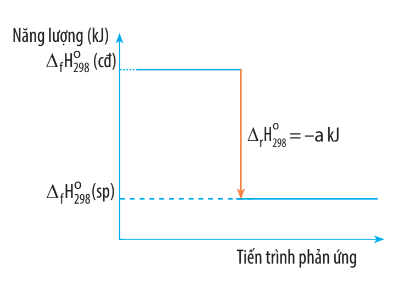
Câu 12:
Cho phản ứng: Na (s) +  Cl2 (g) ⟶NaCl (s) có
Cl2 (g) ⟶NaCl (s) có  (NaCl, s) = − 411,1 kJ/mol.
(NaCl, s) = − 411,1 kJ/mol.
Nếu chỉ thu được 0,5 mol NaCl (s) ở điều kiện chuẩn thì lượng nhiệt tỏa ra là
Câu 13:
Cho phản ứng sau:
S (s) + O2 (g)  SO2 (g)
SO2 (g)  (SO2, g) = – 296,8 kJ/mol
(SO2, g) = – 296,8 kJ/mol
Khẳng định sai là


