Trắc nghiệm Một số axit quan trọng (có đáp án)
Trắc nghiệm Hóa học 9 Bài 4: Một số axit quan trọng
-
554 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
23/07/2024Chất nào dưới đây không dùng để phân biệt dung dịch Na2SO4 và dung dịch H2SO4 loãng?
 Xem đáp án
Xem đáp án
Đáp án D
Chất không dùng để phân biệt dung dịch Na2SO4 và dung dịch H2SO4 loãng là Cu.
Vì Cu không phản ứng với dung dịch Na2SO4 và dung dịch H2SO4 loãng.
Câu 2:
23/07/2024Để an toàn khi pha loãng H2SO4 đặc cần thực hiện theo cách:
 Xem đáp án
Xem đáp án
Đáp án C
Để an toàn khi pha loãng H2SO4 đặc cần thực hiện theo cách: rót từ từ axit vào nước và khuấy đều bằng đũa thủy tinh.
Câu 3:
23/07/2024Để hòa tan vừa hết 6,72 gam sắt phải dùng bao nhiêu ml hỗn hợp dung dịch HCl 0,2M và H2SO4 0,5M?
 Xem đáp án
Xem đáp án
Đáp án D
Số mol của Fe là:
nFe = 0,12 mol
Gọi thể tích dung dịch hỗn hợp axit cần dùng là V (lít)
Số mol của HCl là:
nHCl = 0,2V (mol)
Số mol của H2SO4 là:
nH2SO4nH2SO4= 0,5V (mol)
Phương trình phản ứng:
Fe+2HCl→FeCl2+H20,1V 0,2V (mol)Fe+H2SO4→FeSO4+H20,5V 0,5V (mol)Fe+2HCl→FeCl2+H20,1V
Suy ra số mol của Fe là:
nFe = 0,1V + 0,5V = 0,6V = 0,12 mol
Suy ra V = 0,2 lít = 200 ml.
Câu 4:
21/07/2024Kim loại nào sau đây không tác dụng với dung dịch axit H2SO4 loãng?
 Xem đáp án
Xem đáp án
Đáp án D
K, Mg, Zn đều tác dụng với dung dịch axit H2SO4 loãng.
Ag đứng sau H trong dãy hoạt động hóa học nên không tác dụng với dung dịch axit H2SO4 loãng.
Câu 5:
22/07/2024Ứng dụng của axit clohidric được dùng để
 Xem đáp án
Xem đáp án
Đáp án D
Ứng dụng của axit clohidric được dùng để
+ Điều chế các muối clorua
+ Làm sạch bề mặt kim loại trước khi hàn
+ Chế biến thực phẩm, dược phẩm.
Câu 6:
16/07/2024Cho 8,1 gam kẽm oxit tác dụng vừa đủ với dung dịch axit HCl, sau phản ứng thu được m gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Số mol của ZnO là:
nZnO = 8,181 = 0,1 mol
Phương trình phản ứng:
ZnO+2HCl→ZnCl2+H2O0,1 0,1 (mol)
Theo phương trình phản ứng ta có
nZnCl2 = 0,1 mol
Vậy khối lượng của ZnCl2 cần tìm là:
m = 0,1.136 = 13,6 gam.
Câu 7:
13/07/2024Chất nào sau đây khi tác dụng với H2SO4 loãng sinh ra dung dịch có màu xanh lam?
 Xem đáp án
Xem đáp án
Đáp án D
CuO khi tác dụng với H2SO4 loãng sinh ra dung dịch có màu xanh lam (CuSO4)
Phương trình phản ứng:
CuO + H2SO4 → CuSO4 + H2O
Câu 8:
23/07/2024Cho 1,08 gam nhôm tác dụng với axit clohidric dư, sau phản ứng thu được V lít khí H2 ở đktc. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án B
Số mol của nhôm là:
nAl = 1,0827= 0,04 mol
Phương trình phản ứng:
2Al+6HCl→2AlCl3+3H20,04 0,06(mol)
Theo phương trình phản ứng ta có:
nH2 = 0,06 mol
Vậy thể tích khí H2 thu được ở đktc là:
V = 0,06.22,4 = 1,344 lít.
Câu 9:
23/07/2024Chất nào sau đây tác dụng với dung dịch HCl loãng sinh ra chất khí cháy được trong không khí?
 Xem đáp án
Xem đáp án
Đáp án C
Zn tác dụng với dung dịch HCl loãng sinh ra chất khí cháy được trong không khí (chất khí đó là H2)
Phương trình phản ứng:
Zn + 2HCl → ZnCl2 + H2
Câu 10:
16/07/2024Oxit tác dụng được với axit clohiđric là
 Xem đáp án
Xem đáp án
Đáp án D
Phương trình phản ứng:
BaO + 2HCl → BaCl2 + H2O
Câu 11:
22/07/2024Hòa tan hết 16,8 gam kim loại A hóa trị II trong dung dịch axit HCl, sau phản ứng thu được 6,72 lít khí H2 ở đktc. Kim loại A là
 Xem đáp án
Xem đáp án
Đáp án A
Số mol khí H2 là:
nH2=6,7222,4 = 0,3 mol
Phương trình phản ứng:
A+2HCl→ACl2+H20,3 0,3(mol)
Theo phương trình phản ứng ta có:
nA = 0,3 mol
⇒MA = 16,80,3= 56 g/mol
Vậy A là kim loại sắt (Fe).
Câu 12:
21/07/2024Ứng dụng của axit sunfuric là
 Xem đáp án
Xem đáp án
Đáp án D
Ứng dụng của axit sunfuric là: Chế biến dầu mỏ, sản xuất muối, axit, chất tẩy rửa. Ngoài ra còn có các ứng dụng khác như: luyện kim, phẩm nhuộm, phân bón, tơ sợi, chất dẻo, …
Câu 13:
21/07/2024Tính chất nào không phải là tính chất hóa học của axit clohidric?
 Xem đáp án
Xem đáp án
Đáp án D
- Tính chất hóa học của axit clohidric là:
+ Làm đổi màu quỳ tím thành đỏ
+ Tác dụng với nhiều kim loại (Mg, Al, Zn, …)
+ Tác dụng với bazơ
+ Tác dụng với oxit bazơ
+ Tác dụng với một số muối
Câu 14:
23/07/2024Trung hòa 100ml dung dịch H2SO4 2M bằng dung dịch NaOH 80%. Tính khối lượng dung dịch NaOH cần dùng.
 Xem đáp án
Xem đáp án
Đáp án C
Số mol H2SO4 là:
nH2SO4 = 2.0,1 = 0,2 mol
Phương trình phản ứng:
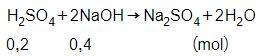
Theo phương trình phản ứng ta có số mol của NaOH là:
nNaOH = 0,4 mol
Khối lượng NaOH cần dùng:
mNaOH = 0,4.40 = 16 gam
Khối lượng dung dịch NaOH 80% là:
mdd=mNaOH.100%C%=16.100%80%⇒mdd=20 gam
Câu 15:
19/07/2024Nhỏ từ từ dung dịch BaCl2 vào dung dịch K2SO4 ta thấy xuất hiện
 Xem đáp án
Xem đáp án
Đáp án B
Nhỏ từ từ dung dịch BaCl2 vào dung dịch K2SO4 quan sát thấy xuất hiện kết tủa màu trắng (BaSO4).
Phương trình phản ứng:
BaCl2 + K2SO4 → BaSO4 ↓ + 2KCl
