Giải SGK Khoa học tự nhiên 8 KNTT Bài 7: Tốc độ phản ứng và chất xúc tác
Giải SGK Khoa học tự nhiên 8 KNTT Bài 7: Tốc độ phản ứng và chất xúc tác có đáp án
-
164 lượt thi
-
10 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
22/07/2024Có những phản ứng xảy ra rất nhanh, quan sát được ngay như phản ứng nổ, cháy, … và có những phản ứng xảy ra chậm, sau một khoảng thời gian mới quan sát được như phản ứng tạo gỉ sắt, tinh bột lên men rượu, … Vậy dùng đại lượng nào để đặc trưng cho sự nhanh, chậm của một phản ứng? Yếu tố nào ảnh hưởng đến sự nhanh, chậm này?
 Xem đáp án
Xem đáp án
- Tốc độ phản ứng là đại lượng đặc trưng cho sự nhanh chậm của phản ứng hoá học.
- Một số yếu tố ảnh hưởng đến tốc độ phản ứng là: nồng độ, nhiệt độ, diện tích bề mặt tiếp xúc, chất xúc tác…
Câu 2:
14/07/2024So sánh tốc độ của một số phản ứng
Phản ứng sắt bị gỉ, đốt cháy cồn được minh hoạ ở các Hình 7.1 và 7.2.

Quan sát các Hình 7.1 và 7.2, thảo luận nhóm và trả lời câu hỏi:
Phản ứng sắt bị gỉ xảy ra nhanh hơn hay chậm hơn phản ứng đốt cháy cồn?
 Xem đáp án
Xem đáp án
Phản ứng sắt bị gỉ xảy ra chậm hơn so với phản ứng đốt cháy cồn.
Câu 3:
16/07/2024Một học sinh thực hiện thí nghiệm và ghi lại hiện tượng như sau:
Cho cùng một lượng hydrochloric acid vào hai ống nghiệm đựng cùng một lượng đá vôi ở dạng bột (ống nghiệm (1)) và dạng viên (ống nghiệm (2)). Quan sát hiện tượng thấy rằng ở ống nghiệm (1) bọt khí xuất hiện nhiều hơn và đá vôi tan hết trước.
Phản ứng giữa hydrochloric acid với đá vôi dạng bột xảy ra nhanh hơn hay chậm hơn so với phản ứng giữa hydrochloric acid với đá vôi dạng viên?
 Xem đáp án
Xem đáp án
Phản ứng giữa hydrochloric acid với đá vôi dạng bột xảy ra nhanh hơn so với phản ứng giữa hydrochloric acid với đá vôi dạng viên.
Câu 4:
15/07/2024Ảnh hưởng của nồng độ đến tốc độ phản ứng
Chuẩn bị: dung dịch HCl 0,1 M, dung dịch HCl 1 M, 2 đinh sắt giống nhau (khoảng 0,2 g); ống nghiệm.
Tiến hành:
- Cho vào ống nghiệm (1) khoảng 5 mL dung dịch HCl 0,1 M; ống nghiệm (2) khoảng 5 mL dung dịch HCl 1 M.
- Nhẹ nhàng đưa lần lượt 2 đinh sắt vào 2 ống nghiệm và quan sát sự thoát khí.
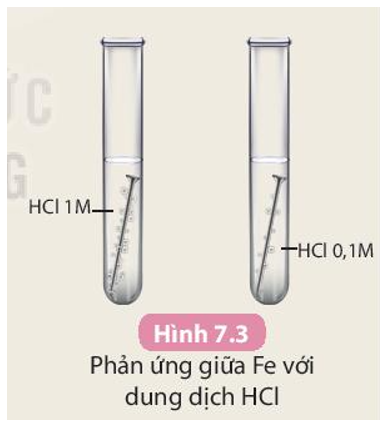
Trả lời câu hỏi:
- Phản ứng ở ống nghiệm nào xảy ra nhanh hơn?
- Nồng độ ảnh hưởng đến tốc độ phản ứng như thế nào?
 Xem đáp án
Xem đáp án
- Phản ứng ở ống nghiệm (2) (tức ống nghiệm chứa HCl 1 M) xảy ra nhanh hơn.
- Khi tăng nồng độ chất tham gia phản ứng thì tốc độ phản ứng tăng.
Câu 5:
23/07/2024Chuẩn bị: viên C sủi, nước lạnh, nước nóng; cốc thuỷ tinh.
Tiến hành:
Lấy hai cốc nước, một cốc nước lạnh và một cốc nước nóng, cho đồng thời vào mỗi cốc một viên C sủi.

Quan sát hiện tượng và trả lời câu hỏi:
- Phản ứng ở cốc nào xảy ra nhanh hơn?
- Nhiệt độ ảnh hưởng đến tốc độ phản ứng như thế nào?
 Xem đáp án
Xem đáp án
- Phản ứng ở cốc nước nóng xảy ra nhanh hơn.
- Khi tăng nhiệt độ của chất tham gia phản ứng, tốc độ phản ứng tăng lên.
Câu 6:
13/07/2024Chuẩn bị: dung dịch HCl 0,1 M, đá vôi (dạng viên), đá vôi (dạng bột hoặc đập nhỏ từ đá vôi dạng viên); ống nghiệm.
Tiến hành:
- Cân một lượng đá vôi (dạng bột) và đá vôi (dạng viên) bằng nhau (khoảng 1 gam) cho vào 2 ống nghiệm (1) và (2).
- Cho vào mỗi ống nghiệm khoảng 3 mL dung dịch HCl 0,1 M, quan sát sự thoát khí.
Trả lời câu hỏi:
- Phản ứng ở ống nghiệm nào xảy ra nhanh hơn? Giải thích.
- Kích thước hạt ảnh hưởng đến tốc độ phản ứng như thế nào?
 Xem đáp án
Xem đáp án
- Phản ứng ở ống nghiệm (1) chứa đá vôi dạng bột xảy ra nhanh hơn. Do đá vôi dạng bột có diện tích tiếp xúc lớn hơn đá vôi dạng viên.
- Kích thước hạt càng nhỏ, tốc độ phản ứng càng lớn.
Câu 7:
13/07/2024Chuẩn bị: nước oxy già (y tế) H2O2 3%, manganese dioxide (MnO2, dạng bột); ống nghiệm.
Tiến hành:
- Cho khoảng 3 mL dung dịch H2O2 3% vào hai ống nghiệm (1) và ống nghiệm (2).
- Cho một ít bột manganese dioxide vào ống nghiệm (2) và quan sát sự thoát khí.
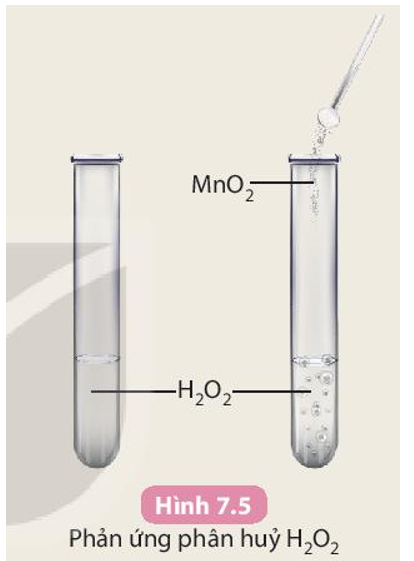
Trả lời câu hỏi:
Phản ứng ở ống nghiệm nào xảy ra nhanh hơn?
 Xem đáp án
Xem đáp án
Phản ứng ở ống nghiệm (2) xảy ra nhanh hơn do khí thoát ra nhanh và mạnh hơn.
Câu 8:
18/07/2024Than cháy trong bình khí oxygen nhanh hơn cháy trong không khí. Yếu tố nào ảnh hưởng đến tốc độ của phản ứng đốt cháy than?
 Xem đáp án
Xem đáp án
Than cháy trong bình khí oxygen nhanh hơn cháy trong không khí. Yếu tố nồng độ đã ảnh hưởng đến phản ứng đốt cháy than.
Câu 9:
18/07/2024Khi “bảo quản thực phẩm trong tủ lạnh để giữ thực phẩm tươi lâu hơn” là đã tác động vào yếu tố gì để làm chậm tốc độ phản ứng?
 Xem đáp án
Xem đáp án
Khi “bảo quản thực phẩm trong tủ lạnh để giữ thực phẩm tươi lâu hơn” là đã tác động vào yếu tố nhiệt độ để làm chậm tốc độ phản ứng.
Câu 10:
21/07/2024Trong quá trình sản xuất sulfuric acid có giai đoạn tổng hợp sulfur trioxide (SO3). Phản ứng xảy ra như sau:
2SO2 + O2 → 2SO3.
Khi có mặt vanadium(V) oxide thì phản ứng xảy ra nhanh hơn.
a) Vanadium(V) oxide đóng vai trò gì trong phản ứng tổng hợp sulfur trioxide?
b) Sau phản ứng, khối lượng của vanadium(V) oxide có thay đổi không? Giải thích.
 Xem đáp án
Xem đáp án
a) Vanadium(V) oxide đóng vai trò là chất xúc tác trong phản ứng tổng hợp sulfur trioxide.
b) Sau phản ứng, khối lượng của vanadium(V) oxide không thay đổi. Do chất xúc tác là chất làm tăng tốc độ phản ứng nhưng sau phản ứng vẫn giữ nguyên về khối lượng và tính chất hoá học.
Có thể bạn quan tâm
Các bài thi hot trong chương
- Trắc nghiệm KHTN 8 KNTT Bài 4: Dung dịch và nồng độ (398 lượt thi)
- Trắc nghiệm KHTN 8 KNTT Bài 6: Tính theo phương trình hoá học (377 lượt thi)
- Trắc nghiệm KHTN 8 KNTT Bài 3: Mol và tỉ khối chất khí (339 lượt thi)
- Trắc nghiệm KHTN 8 KNTT Bài 2: Phản ứng hoá học (227 lượt thi)
- Trắc nghiệm KHTN 8 KNTT Bài 5: Định luật bảo toàn khối lượng và phương trình hóa học (204 lượt thi)
