Giải SBT Hóa 10 Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học có đáp án
Giải SBT Hóa 10 Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học có đáp án
-
343 lượt thi
-
26 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 1:
23/07/2024Nối mỗi nội dung ở cột A với nội dung ở cột B sao cho phù hợp:
|
Cột A |
Cột B |
|
a) Trong phản ứng thu nhiệt, dấu của ∆H dương vì b) Trong phản ứng tỏa nhiệt có sự c) Trong phản ứng tỏa nhiệt, ∆H có dấu âm vì d) Trong phản ứng thu nhiệt có sự |
1. giải phóng năng lượng.
2. hấp thụ năng lượng. 3. năng lượng của hệ chất phản ứng lớn hơn năng lượng của hệ chất sản phẩm. 4. năng lượng của hệ chất phản ứng nhỏ hơn năng lượng của hệ chất sản phẩm. |
 Xem đáp án
Xem đáp án
- a ghép với 4:
Trong phản ứng thu nhiệt, dấu của ∆H dương vì năng lượng của hệ chất phản ứng nhỏ hơn năng lượng của hệ chất sản phẩm.
- b ghép với 1:
Trong phản ứng tỏa nhiệt có sự giải phóng năng lượng.
- c ghép với 3:
Trong phản ứng tỏa nhiệt, ∆H có dấu âm vì năng lượng của hệ chất phản ứng lớn hơn năng lượng của hệ chất sản phẩm.
- d ghép với 2:
Trong phản ứng thu nhiệt có sự giải phóng năng lượng.
Câu 2:
22/07/2024Đường sucrose (C12H22O11) là một đường đôi. Trong môi trường acid ở dạ dày và nhiệt độ cơ thể, sucrose bị thủy phân thành đường glucose và fructose, sau đó bị oxi hóa bởi oxygen tạo thành CO2 và H2O. Sơ đồ thay đổi năng lượng hóa học của phản ứng được cho như hình dưới đây:
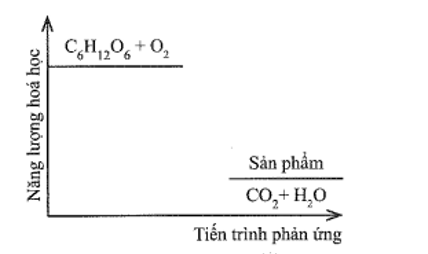
a) Dựa theo đồ thị, hãy cho biết phản ứng trong đó là tỏa nhiệt hay thu nhiệt. Vì sao?
 Xem đáp án
Xem đáp án
a) Phản ứng này là tỏa nhiệt vì có biến thiên enthalpy âm (năng lượng của hệ chất phản ứng lớn hơn năng lượng của hệ chất sản phẩm).
Câu 3:
14/07/2024b) Viết phương trình hoá học của phản ứng thuỷ phân đường sucrose. Phản ứng trong sơ đồ có phải là phản ứng oxi hoá - khử không? Nếu có, hãy chỉ ra chất oxi hoá và chất khử trong phản ứng và cân bằng phương trình hoá học của phản ứng theo phương pháp thăng bằng electron.
 Xem đáp án
Xem đáp án
b) Phản ứng thuỷ phân đường sucrose trong môi trường acid và đun nóng:
C12H22O11 + H2O acid,to→ C6H12O6 (glucose) + C6H12O6 (fructose)
Phản ứng trong sơ đồ là phản ứng oxi hóa – khử; trong đó oxygen là chất oxi hóa; đường glucose và fructose là chất khử.
Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron:
0C6H12O6+ 0O2→ +4CO2+ H2−2O
Các quá trình:
1×1×|0C→+4C +4e0O2+4e→2−2O
Phương trình hóa học:
C6H12O6(g) + 6O2(g) → 6CO2(g) + 6H2O(l)
Câu 4:
18/07/2024c) Khi 1 mol đường sucrose bị đốt cháy hoàn toàn với một lượng vừa đủ oxygen ở điều kiện chuẩn toả ra một lượng nhiệt là 5 645 kJ. Xác định biến thiên enthalpy chuẩn của phản ứng oxi hoá sucrose.
 Xem đáp án
Xem đáp án
c) Phản ứng đốt cháy đường sucrose:
C12H22O11(s) + 12O2(g) → 12CO2(g) + 11H2O(l)
Biến thiên enthalpy chuẩn của phản ứng là: ΔrH0298=−5 645kJ.
Câu 5:
15/07/2024d) Nếu 5,00 gam đường sucrose được đốt cháy hoàn toàn ở cùng điều kiện như trên thì biến thiên enthalpy quá trình bằng bao nhiêu?
 Xem đáp án
Xem đáp án
d) Nếu 5,00 gam đường sucrose được đốt cháy hoàn toàn ở cùng điều kiện như trên thì biến thiên enthalpy quá trình bằng:
5342×(−5645)=−82,5(kJ)
Câu 6:
16/07/2024e) Vì sao để duy trì một cơ thể khoẻ mạnh, cần một chế độ dinh dưỡng đầy đủ và luyện tập thể dục thể thao hợp lí?
 Xem đáp án
Xem đáp án
e) Cơ thể cần năng lượng để hoạt động nên phải có chế độ dinh dưỡng đầy đủ.
Luyện tập thể dục thể thao hợp lý là một phần quan trọng của lối sống lành mạnh. Tập thể dục thể thao giúp hạn chế các vấn đề sức khỏe, giúp cơ thể khỏe mạnh, cung cấp năng lượng, giúp giảm căng thẳng. Bên cạnh đó, còn có thể giúp bạn duy trì một trọng lượng cơ thể hợp lý và kiểm soát sự thèm ăn của bạn.
Câu 7:
23/07/2024Biến thiên enthalpy chuẩn của quá trình “H2O(s) → H2O(l)” là 6,020 kJ.
a) Quá trình tan chảy của nước đá là quá trình thu nhiệt hay toả nhiệt? Vì sao?
 Xem đáp án
Xem đáp án
a) Quá trình tan chảy của nước đá là quá trình thu nhiệt vì có biến thiên enthalpy dương.
Câu 8:
15/07/2024b) Vì sao khi cho viên nước đá vào một cốc nước lỏng ấm, viên đá lại tan chảy dần?
 Xem đáp án
Xem đáp án
b) Khi cho viên nước đá vào một cốc nước lỏng ấm, viên đá tan chảy dần vì nó lấy nhiệt từ nước lỏng (là môi trường xung quanh).
Câu 9:
19/07/2024c) Vì sao cốc nước lỏng bị lạnh dần trong quá trình viên nước đá tan chảy?
 Xem đáp án
Xem đáp án
c) Nước lỏng nhường nhiệt cho viên nước đá, sự mất nhiệt làm cho nước lỏng lạnh đi.
Câu 10:
23/07/2024d) Biết rằng để làm cho nhiệt độ của 1 mol nước lỏng thay đổi 1 °C cần một nhiệt lượng là 75,4 J. Giả sử mỗi viên nước đá tương ứng với 1 mol nước, số viên nước đá tối thiểu cần tan chảy để có thể làm lạnh 500 gam nước lỏng ở 20 °C xuống 0 °C là
A. 1.
B. 7.
C. 14.
D. 15.
E. 126.
 Xem đáp án
Xem đáp án
d) Nhiệt lượng mà 500 gam nước lỏng từ 20 oC giảm xuống 0 oC tỏa ra là:
50018×75,4×|0−20|=41888,9 (J)=41,8889(kJ)
Phần nhiệt lượng tỏa ra này được viên nước đá hấp thụ để tan chảy. Số viên nước đá tối thiểu cần là:
41,88896,02≈7 viên.
Câu 11:
17/07/2024e) Để làm lạnh 120 gam nước lỏng ở 45 °C xuống 0°C, một bạn học sinh đã dùng 150 gam nước đá. Lượng nước đá này là vừa đủ, thiếu hay dư?
(Trong phần d, e, giả thiết chỉ có sự trao đổi nhiệt giữa nước và nước đá.)
 Xem đáp án
Xem đáp án
e) Nhiệt lượng tỏa ra khi nhiệt độ của 120 gam nước lỏng từ 45 oC giảm xuống 0 oC là:
12018×75,4×|0−45|=22620 (J)=22,62(kJ)
Lượng nước đá cần dùng là:
22,626,02×18=67,63(g)
Vậy dùng 150 gam nước đá là dư.
Câu 12:
22/07/2024Phản ứng của 1 mol enthanol lỏng với oxygen xảy ra theo phương trình:
C2H5OH(l) + O2(g) → CO2(g) + H2O(l) (1)
a) Những nhận định nào sau đây là đúng?
(1) Đây là phản ứng tỏa nhiệt vì nó tạo ra khí CO2 và nước lỏng.
(2) Đây là phải là phản ứng oxi hóa – khử với tổng số hệ số cân bằng trong phương trình phản ứng là 9.
(3) Biến thiên enthalpy chuẩn của phản ứng sẽ thay đổi nếu nước tạo ra ở thể khí.
(4) Sản phẩm của phản ứng chiếm một thể tích lớn hơn so với chất phản ứng.
A. (1), (2).
B. (1), (2), (3).
C. (1), (3), (4).
D. (3), (4).
E. (1).
G. (2), (3).
 Xem đáp án
Xem đáp án
a) Đáp án đúng là: G
C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l) (1)
Phát biểu (1) sai vì để xét phản ứng tỏa nhiệt hay thu nhiệt cần dựa vào năng lượng hóa học của phản ứng.
Phát biểu (2) đúng, tổng hệ số cân bằng của phản ứng là 1 + 3 + 2 + 3 = 9.
Phát biểu (3) đúng.
Phát biểu (4) sai, sản phẩm của phản ứng chiếm một số mol lớn hơn so với chất phản ứng.
Câu 13:
21/07/2024b) Biến thiên enthalpy chuẩn kèm theo quá trình khi 1 mol ethanol lỏng cháy hoàn toàn trong oxygen là ΔrH0298=−1,367×103 kJ, xác định enthalpy hình thành chuẩn của C2H5OH (lỏng).
(Những số liệu cần thiết được cho trong Phụ lục 3, SGK Hóa học 10, Cánh Diều).
 Xem đáp án
Xem đáp án
b) C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l) ΔrH0298=−1367,0kJ.
ΔrH0298=3×ΔfH0298(H2O(l))+2×ΔfH0298(CO2(g))−3×ΔfH0298(O2(g))−ΔfH0298(C2H5OH(l))
Vậy ΔfH0298(C2H5OH(l))=3×(−285,8)+2×(−393,5)−3×0−(−1367)=−277,4(kJ mol−1)
Câu 14:
21/07/2024Sulfur dioxide là một chất có nhiều ứng dụng trong công nghiệp (dùng để sản xuất sulfuric acid, tẩy trắng bột giấy trong công nghiệp giấy, tẩy trắng dung dịch đường trong sản xuất đường tinh luyện, …) và giúp ngăn cản sự phát triển của một số loại vi khuẩn và nấm gây hư hại cho thực phẩm. Ở áp suất 1 bar và nhiệt độ 25oC, phản ứng giữa 1 mol sulfur với oxygen xảy ra theo phương trình “S(s) + O2(g) → SO2(g)” và tỏa ra một lượng nhiệt là 296,9 kJ.
Những phát biểu nào sau đây là đúng?
A. Biến thiên enthalpy chuẩn của phản ứng là 296,9 kJ.
B. Enthalpy tạo thành chuẩn của sulfur dioxide bằng -296,9 kJ mol-1.
C. Sulfur dioxide vừa có thể là chất khử vừa có thể là chất oxi hóa, tùy thuộc vào phản ứng mà nó tham gia.
D. 0,5 mol sulfur tác dụng hết với oxygen giải phóng 148,45 kJ năng lượng dưới dạng nhiệt.
E. 32 gam sulfur cháy hoàn toàn tỏa ra một lượng nhiệt là 2,969 × 105 J.
 Xem đáp án
Xem đáp án
Đáp án đúng là: B, C, D, E
A sai vì: Biến thiên enthalpy chuẩn của phản ứng là -296,9 kJ.
Câu 15:
13/07/2024Phản ứng luyện gang trong lò cao có phương trình như sau:
Fe2O3(s) + CO(g) → Fe(s) + CO2(g) (1)
a) Cân bằng phương trình hóa học của phản ứng (1) và tính biến thiên enthalpy chuẩn của phản ứng với các hệ số cân bằng tương ứng.
 Xem đáp án
Xem đáp án
a) +3Fe2O3(s) + +2CO(g) → 0Fe(s) + +4CO2(g)
2×3×|+3Fe+3e→0Fe+2C→+4C+2e
Phương trình hóa học: Fe2O3(s) + 3CO(g) → 2Fe(s) + 3CO2(g)
Biến thiên enthalpy chuẩn của phản ứng:
ΔrH0298=3×ΔfH0298(CO2(g))+2×ΔfH0298(Fe(s))−3×ΔfH0298(CO(g))−ΔfH0298(Fe2O3(s))=3×(−393,5)+2×0−3×(−110,5)−(−824,2)=−24,8(kJ).
Câu 16:
23/07/2024b) Từ 1 mol Fe2O3 và 1 mol CO, giả sử chỉ xảy ra phản ứng (1) với hiệu suất 100% thì giải phóng một lượng nhiệt là
 Xem đáp án
Xem đáp án
b) Đáp án đúng là: A
Fe2O3(s) + 3CO(g) → 2Fe(s) + 3CO2(g)
Theo phương trình hóa học ta có CO hết, Fe2O3 dư, tính toán theo mol CO.
Từ 1 mol Fe2O3 và 1 mol CO, giả sử chỉ xảy ra phản ứng (1) với hiệu suất 100% thì giải phóng một lượng nhiệt là
24,83=8,27(kJ).
Câu 17:
23/07/2024Ở điều kiện chuẩn, 2 mol nhôm tác dụng vừa đủ với khí chlorine tạo ra muối aluminium chloride và giải phóng một lượng nhiệt 1 390,81 kJ.
a) Viết và cân bằng phương trình hóa học của phản ứng. Đây có phải là phản ứng oxi hóa – khử không? Vì sao?
 Xem đáp án
Xem đáp án
a) Phương trình hóa học của phản ứng:
2Al(s) + 3Cl2(g) → 2AlCl3(g)
Đây là phản ứng oxi hóa – khử vì có sự thay đổi số oxi hóa của các nguyên tử trong phản ứng.
20Al(s) + 30Cl2(g) → 2+3Al−1Cl3(g)
Câu 18:
13/07/2024b) Biến thiên enthalpy chuẩn của phản ứng bằng bao nhiêu? Phản ứng trên thu nhiệt hay tỏa nhiệt?
 Xem đáp án
Xem đáp án
b) Biến thiên enthalpy chuẩn của phản ứng: ΔrH0298=−1390,81kJ<0
Phản ứng trên tỏa nhiệt.
Câu 19:
21/07/2024c) Tính lượng nhiệt được giải phóng khi 10 gam AlCl3 được tạo thành.
 Xem đáp án
Xem đáp án
c) Cứ 1 mol AlCl3 tạo thành giải phóng:
1390,812=695,405kJ
Lượng nhiệt được giải phóng khi 10 gam AlCl3 được tạo thành là:
10133,5×695,405=52,09(kJ).Câu 20:
22/07/2024d) Nếu muốn tạo ra được 1,0 kJ nhiệt lượng cần bao nhiêu gam Al phản ứng?
 Xem đáp án
Xem đáp án
d) Cứ 1 mol Al phản ứng giải phóng:
1390,812=695,405kJ
Nếu muốn tạo ra được 1,0 kJ nhiệt lượng cần khối lượng Al phản ứng là:
1695,405×27=0,03888(gam).
Câu 21:
15/07/2024Trong ngành công nghệ lọc hóa dầu, các ankan thường được loại bỏ hydrogen trong các phản ứng dehydro hóa để tạo ra những sản phẩm hydrocarbon không no có nhiều ứng dụng trong công nghiệp. Hãy tính biến thiên enthalpy chuẩn của các phản ứng sau dựa vào năng lượng liên kết. (Giá trị một số năng lượng liên kết được cho trong Phụ lục 2, SGK Hóa học 10, Cánh Diều)
Cho biết công thức cấu tạo của 1,3,5 – cyclohexatriene như sau:
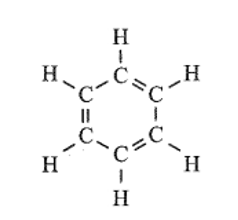
Các phản ứng trên có thuận lợi về phương diện nhiệt hay không? Phản ứng theo chiều ngược lại có biến thiên enthalpy bằng bao nhiêu?
a) H3C – CH2 – CH2 – CH3 → CH2 = CH – CH = CH2 + 2H2
 Xem đáp án
Xem đáp án
a) H3C – CH2 – CH2 – CH3 → CH2 = CH – CH = CH2 + 2H2
ΔrH0298=(10EC−H+3EC−C)−(6EC−H+2EC=C+EC−C)−2EH−H=10×414+3×347−(6×414+2×611+347)−2×436=256(kJ).
Câu 22:
23/07/2024b) 6CH4 → C6H6 (1,3,5 – cyclohexatriene) + 9H2
 Xem đáp án
Xem đáp án
b) 6CH4 → C6H6 + 9H2
ΔrH0298=6×4EC−H−(6EC−H+3EC=C+3EC−C)−9EH−H=24×414−(6×414+3×611+3×347)−9×436=654(kJ).
Các phản ứng này không thuận lợi về phương diện nhiệt.
Phản ứng theo chiều ngược lại thuận lợi về phương diện nhiệt:
CH2 = CH – CH = CH2 + 2H2 → H3C – CH2 – CH2 – CH3 ΔrH0298=−256(kJ)
C6H6 + 9H2 → 6CH4 ΔrH0298=−654(kJ)
Câu 23:
19/07/2024Bằng cách tính biến thiên enthalpy chuẩn của quá trình sau dựa vào năng lượng liên kết, hãy chỉ ra ở điều kiện chuẩn, H3C – CH2 – OH hay H3C – O – CH3 bền hơn.
H3C – CH2 – OH (g) → H3C – O – CH3 (g)
 Xem đáp án
Xem đáp án
CH3CH2OH có 1 liên kết C – C; 5 liên kết C – H; 1 liên kết C – O và 1 liên kết O – H.
CH3OCH3 có 6 liên kết C – H và 2 liên kết C – O.
Quá trình đã cho có biến thiên enthalpy chuẩn là:
ΔrH0298=Eb(CH3CH2OH)−Eb(CH3OCH3)=(347+5×414+360+464)−(6×414+2×360)=37(kJ)
ΔrH0298>0 chứng tỏ ở điều kiện chuẩn CH3CH2OH bền hơn CH3OCH3.
Câu 24:
23/07/2024Xét các phản ứng thế trong dãy halogen ở điều kiện chuẩn:
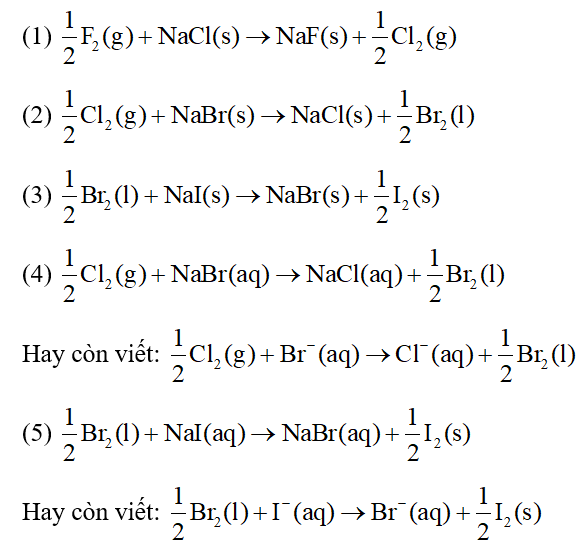
a) Từ các giá trị của enthapyl hình thành chuẩn, hãy tính biến thiên enthalpy chuẩn của các phản ứng thế trên.

(Các giá trị khác được cho trong Phụ lục 3, SGK Hóa học 10, Cánh Diều).
 Xem đáp án
Xem đáp án
a)
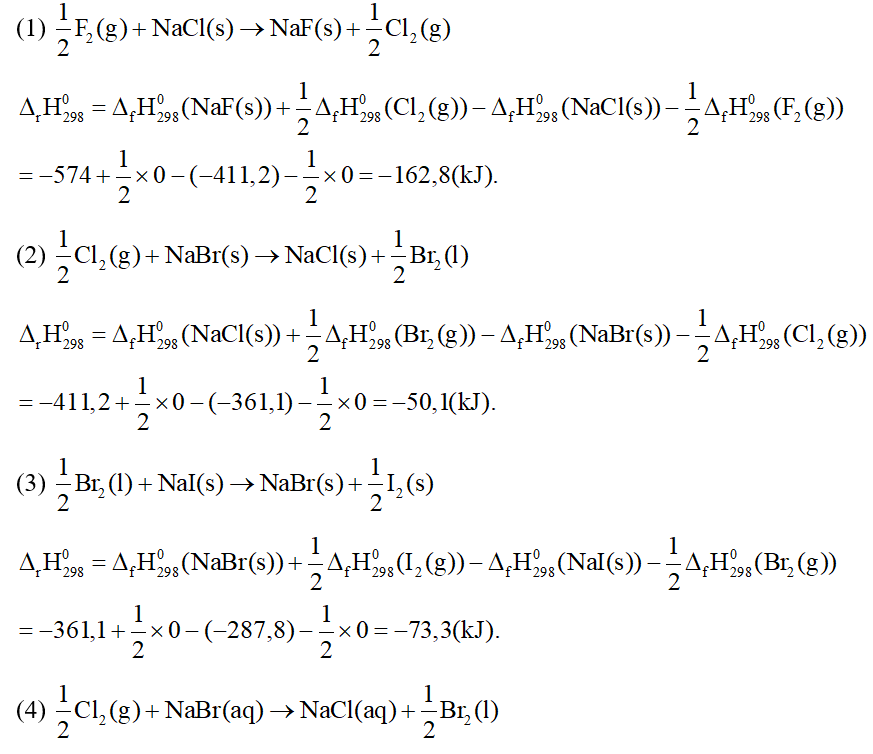
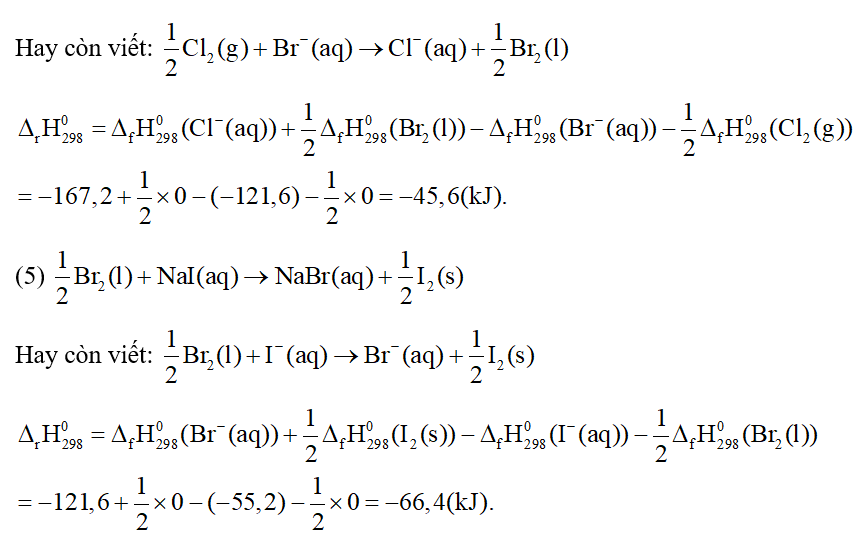
Câu 25:
19/07/2024b) Nhận xét sự thuận lợi về phương diện nhiệt của các phản ứng thế trong dãy halogen. Kết quả này có phù hợp với quy luật biến đổi tính phi kim của dãy halogen trong bảng tuần hoàn các nguyên tố hóa học không?
 Xem đáp án
Xem đáp án
b) Kết quả này có phù hợp với quy luật biến đổi tính phi kim của dãy halogen trong bảng tuần hoàn các nguyên tố hóa học.
Cụ thể, các giá trị biến thiên enthalpy chuẩn đều âm thể hiện quá trình diễn ra thuận lợi về phương diện nhiệt; quy luật tính chất oxi hóa của X: halogen có tính oxi hóa mạnh đẩy được halogen có tính oxi hóa yếu hơn ra khỏi muối của nó.
Câu 26:
17/07/2024Phân tử hemoglobin (Hb) trong máu nhận O2 ở phổi để chuyển thành HbO2. Chất này theo máu tới các bộ phận cơ thể, tại đó HbO2 lại chuyển thành Hb và O2 (để cung cấp O2 cho các hoạt động sinh hóa cần thiết trong cơ thể). Nếu trong không khí có lẫn carbon monoxide (CO), cơ thể nhanh chóng bị ngộ độc. Cho các số liệu thực nghiệm sau:
Hb + O2 → HbO2 ΔrH0298=−33,05 kJ (1)
Hb + CO → HbCO ΔrH0298=−47,28 kJ (2)
HbO2 + CO → HbCO + O2 ΔrH0298=−14,23 kJ (3)
HbCO + O2 → HbO2 + CO ΔrH0298=14,23 kJ (4)
Liên hệ giữa mức độ thuận lợi của phản ứng (qua ΔrH0298) với những vấn đề thực nghiệm nêu trên.
 Xem đáp án
Xem đáp án
Vì các phản ứng (2) và (3) lần lượt có ΔrH0298 âm hơn phản ứng (1) và (4) nên sự hình thành HbCO thuận lợi hơn sự tạo thành HbO2. Do vậy không có sự nhả O2 và giải phóng Hb như trường hợp không có CO. Điều này giải thích sự ngộ độc CO trong máu.
