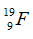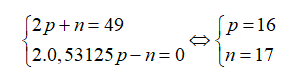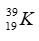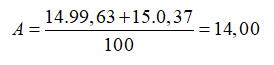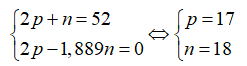Đề thi giữa kì 1 Hóa học 10 có đáp án (Bài số 1)
Đề thi giữa kì 1 Hóa 10 có đáp án (Bài số 1 - Đề 3)
-
759 lượt thi
-
30 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 2:
02/07/2024Hạt nhân của hầu hết các nguyên tử do các loại hạt sau cấu tạo nên
 Xem đáp án
Xem đáp án
Chọn C
Câu 3:
21/07/2024Một nguyên tử được đặc trưng cơ bản bằng
 Xem đáp án
Xem đáp án
Chọn đáp án D
Số đơn vị điện tích hạt nhân Z và số khối A đặc trưng cho hạt nhân và cũng đặc trưng cho nguyên tử vì khi biết Z và A sẽ biết được số proton, số notron và số electron.
Câu 4:
20/07/2024Nguyên tử có số e là 13 thì cấu hình lớp ngoài cùng là
 Xem đáp án
Xem đáp án
Chọn D
Cấu hình electron của nguyên tử đó là:
→ Cấu hình electron lớp ngoài cùng là:
Câu 5:
02/07/2024Trong nguyên tử X các e được phân bố trên 3 lớp, lớp thứ 3 có 8e. Điện tích hạt nhân của nguyên tử X là
 Xem đáp án
Xem đáp án
Chọn C
Cấu hình electron của X là:
Số hiệu nguyên tử X = số electron = 18.
Điện tích hạt nhân X là 18+.
Câu 7:
12/07/2024Có bao nhiêu electron trong ion ?
 Xem đáp án
Xem đáp án
Chọn A
Crom có p = e = 24 hạt, có e = 21 (do đã nhường 3 e).
Câu 10:
09/07/2024Cho số hiệu nguyên tử của cacbon, nitơ, oxi và flo lần lượt là 6, 7, 8, 9 và số khối của chúng lần lượt là 12, 14, 16, 19. Xét kí hiệu nào sau đây viết sai?
 Xem đáp án
Xem đáp án
Chọn D
Kí hiệu đúng là
Câu 11:
18/07/2024Kí hiệu nào trong số các kí hiệu của các phân lớp sau là sai?
 Xem đáp án
Xem đáp án
Chọn A
Không có phân lớp 2d.
Câu 12:
19/07/2024A có điện tích hạt nhân là 25. Vậy A là?
 Xem đáp án
Xem đáp án
Chọn A
Trật tự phân mức năng lượng:
Electron cuối cùng được điền vào phân lớp d theo trật tự phân mức năng lượng. Vậy A là nguyên tố d.
Câu 14:
14/07/2024Cho 2 kí hiệu nguyên tử: và chọn câu trả lời đúng
 Xem đáp án
Xem đáp án
Chọn D
A sai vì điện tích của hạt nhân A là 11+, điện tích của hạt nhân B là 12+.
B sai vì A có 11 electron và B có 12 electron.
C sai vì A và B có số proton khác nhau nên không là đồng vị của nhau.
Câu 16:
22/07/2024Nguyên tử của nguyên tố A có tổng số electron trong các phân lớp p là 7. Nguyên tử của nguyên tố B có tổng số hạt mang điện nhiều hơn tổng số hạt mang điện của A là 8. Số đơn vị điện tích hạt nhân của A và B là
 Xem đáp án
Xem đáp án
Chọn A
Cấu hình electron của A là
→ Số đơn vị điện tích hạt nhân của A là 13.
Số hạt mang điện trong A là 13.2 = 26 → Số hạt mang điện trong B là 26 + 8 = 34.
→ Số đơn vị điện tích hạt nhân của B là 34 : 2 = 17.
Câu 17:
20/07/2024Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 49, trong đó số hạt không mang điện bằng 0,53125 số hạt mang điện. Điện tích hạt nhân của X là
 Xem đáp án
Xem đáp án
Chọn D
Gọi số hạt proton, nơtron và electron trong X lần lượt là p, n và e.
Theo bài ra ta có:
Điện tích hạt nhân nguyên tử X là 16+.
Câu 18:
18/07/2024Trong nguyên tử một nguyên tố A có tổng số các loại hạt là 58. Biết số hạt proton ít hơn số hạt nơtron là 1 hạt. Kí hiệu của A là
 Xem đáp án
Xem đáp án
Chọn B
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố A là 58:
p + e + n = 58 hay 2p + n = 58 (do p = e) (1)
Số hạt p ít hơn số hạt n là 1 hạt:
n- p =1 (2)
Giải (1), (2) ta có p = e = 19, n = 20
Vậy A có số hiệu nguyên tử = số p = 19; Số khối của A là 19 + 20 = 39.
→ Kí hiệu nguyên tử A là:
Câu 19:
06/07/2024Các đồng vị được phân biệt bởi yếu tố nào sau đây?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Các đồng vị được phân biệt bởi số nơtron.
Đồng vị là những nguyên tố hóa học có cùng số proton nhưng khác nhau về số nơtron.
Câu 21:
12/07/2024Dựa vào thứ tự mức năng lượng, xét xem sự xắp xếp các phân lớp nào sau đây sai?
 Xem đáp án
Xem đáp án
Chọn A
Mức năng lượng ở phân lớp 3d > 4s.
Câu 22:
02/07/2024Tổng số hạt cơ bản trong một nguyên tử là
 Xem đáp án
Xem đáp án
Chọn C
Tổng số hạt cơ bản trong Cr = p + n + e = A + e = 52 + 24 = 76.
Câu 23:
20/07/2024Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị có % về số nguyên tử tương ứng là (99,63%) và (0,37%). Nguyên tử khối trung bình của nitơ là
 Xem đáp án
Xem đáp án
Chọn B
Câu 25:
16/07/2024Tổng số hạt n, p, e trong một nguyên tử X là 52, trong đó số hạt mang điện bằng 1,889 lần số hạt không mang điện. Kết luận nào không đúng?
 Xem đáp án
Xem đáp án
Chọn D
Theo bài ra ta có hệ phương trình:
Cấu hình electron của X là → X có 7e lớp ngoài cùng nên là phi kim.
Số khối của X là: 18 + 17 = 35.
Điện tích hạt nhân X là 17+.
Câu 27:
02/07/2024Một nguyên tố hoá học có thể có nhiều nguyên tử có khối lượng khác nhau vì lí do nào dưới đây?
 Xem đáp án
Xem đáp án
Chọn B
Câu 28:
20/07/2024Cho hai nguyên tố A và B có số hiệu nguyên tử lần lượt là 11 và 13. Cấu hình electron của A và B lần lượt là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Cấu hình electron của A là: 1s21s22p63s1
Cấu hình electron của B là: 1s22s22p63s23p1
Lưu ý: Cách viết cấu hình electron:
Bước 1: Xác định số electron của nguyên tử.
Bước 2: Điền các electron của nguyên tử vào các phân lớp theo sơ đồ năng lượng (đầy phân lớp trong mới điền ra phân lớp ngoài).
Sơ đồ mức năng lượng: 1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p….
Bước 3: Khi bắt đầu có phân lớp 3d xuất hiện thì ta phải sắp xếp lại (không điền lại) các phân lớp thành từng lớp theo thứ tự tăng dần. Ta được cấu hình electron.
Bài thi liên quan
-
Đề thi giữa kì 1 Hóa 10 có đáp án (Bài số 1 - Đề 1)
-
30 câu hỏi
-
45 phút
-
-
Đề thi giữa kì 1 Hóa 10 có đáp án (Bài số 1 - Đề 2)
-
30 câu hỏi
-
45 phút
-
-
Đề thi giữa kì 1 Hóa 10 có đáp án (Bài số 1 - Đề 4)
-
30 câu hỏi
-
45 phút
-
Có thể bạn quan tâm
- Đề thi giữa kì 1 Hóa 10 cực hay có đáp án (Bài kiểm tra số 2) (307 lượt thi)
- Đề thi Học kì 1 Hóa 10 có đáp án (328 lượt thi)
- Đề kiểm tra 15 phút Hóa học 10 Học kì 1 có đáp án (Bài số 1) (2600 lượt thi)
- Đề thi giữa kì 1 Hóa học 10 có đáp án (Bài số 1) (758 lượt thi)
- Đề kiểm tra 15 phút Hóa 10 Học kì 1 có đáp án (Bài số 2 - Đề 1) (620 lượt thi)
- Đề thi giữa kì 1 Hóa học 10 có đáp án (Bài số 2) (735 lượt thi)
- Đề thi Hóa 10 Học kì 1 (557 lượt thi)
- Đề thi Hóa học 10 Giữa học kì 1 biên soạn (449 lượt thi)
- Đề thi Hóa học 10 Giữa học kì 1 năm 2020 - 2021 có đáp án (505 lượt thi)
Các bài thi hot trong chương
- Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (3252 lượt thi)
- Đề kiểm tra 15p Hóa 10 Học kì 2 (Bài số 2) (1277 lượt thi)
- Đề thi giữa kì 2 Hóa 10 (Bài số 1) (868 lượt thi)
- Đề thi Học kì 2 Hóa 10 cực hay có đáp án (830 lượt thi)
- Đề thi giữa kì 2 Hóa 10 (Bài số 2) (688 lượt thi)
- Đề kiểm tra 15 phút - Trắc nghiệm + Tự luận (677 lượt thi)
- Đề thi Hóa 10 Học kì 2 (Bài kiểm tra học kì) (656 lượt thi)
- Đề kiểm tra 15p Hóa 10 Học kì 2 (Bài số 1) (611 lượt thi)
- Đề thi giữa kì 2 Hóa 10 cực hay có đáp án (397 lượt thi)