Đề thi cuối kì 2 Hóa 12 có đáp án
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 6)
-
3193 lượt thi
-
48 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
16/07/2024D. NH3
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
H2S + Pb(NO3)2→ PbS (↓ đen) + 2HNO3
Câu 2:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Công thức hoá học của thuốc muối là NaHCO3.
Câu 3:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Thép không phải hợp kim của nhôm; thép là hợp kim của sắt.
Câu 4:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
B sai, Al bị thụ động hoá trong HNO3đặc, nguội.
Câu 5:
16/07/2024Fe + HNO3(loãng) → (X) + (Y) + H2O
(X) và (Y) lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
X là Fe(NO3)3, Y là NO
Fe + 4HNO3→ Fe(NO3)3+ NO + 2H2O
Câu 6:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
A sai, Ag dẫn điện tốt nhất
Câu 7:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Trong công nghiệp sản xuất gang, chất khử CO được dùng để khử oxit sắt.
Câu 8:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Kim loại Na và Ca có tính khử mạnh hơn Cr
Câu 9:
16/07/2024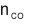 : nNaOH = 1:2 thì dung dịch sau phản ứng chứa chất nào?
: nNaOH = 1:2 thì dung dịch sau phản ứng chứa chất nào? Xem đáp án
Xem đáp án
Đáp án đúng là: C
CO2+ 2NaOH → Na2CO3+ H2O
Câu 10:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Bảo toàn nguyên tố Al:
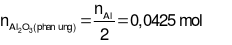
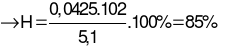
Câu 11:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Gọi công thức hoá học chung của hai muối là MCO3
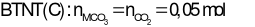
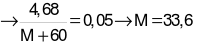
Vậy hai kim loại là Mg và Ca.
Câu 12:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Khi hầm xương, muốn nước xương thu được giàu canxi và photpho ta nên ninh xương với một ít quả chua (me, khế,…) vì trong các quả chua có chứa axit, Ca3(PO4)2trong xương sẽ kết hợp với axit tạo thành muối tan Ca(H2PO4)2.
Câu 13:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Cr + 2HCl → CrCl2+ H2
Theo phương trình: nHCl= 2nCr= 0,24 mol
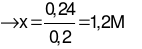
Câu 14:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
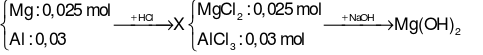
Bảo toàn nguyên tố Mg: 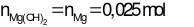

Câu 15:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
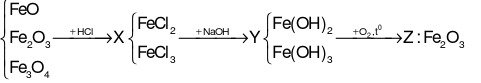
Câu 16:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Bảo toàn electron và bảo toàn N có:
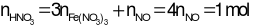
Câu 17:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Đặt công thức hoá học của muối sunfat của kim loại R là RSO4
Ta có hàm lượng % của kim loại R trong muối sunfat là 20%
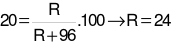
Vậy R là Mg
Câu 18:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D

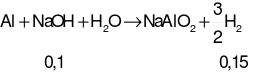
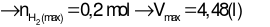
Câu 19:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Fe2O3+ 6HNO3→ 2Fe(NO3)3+ 3H2O
Câu 20:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Gọi 8a, 2a, a lần lượt là số mol của Fe, FeCO3, Fe3O4trong X
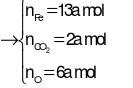
→ mX= 912a gam
→ nCu= 2,85a mol
Bảo toàn e: 13a.2 +2,85a.2 = 6a.2 + (0,1185 – 2a).2
→ a = 0,01
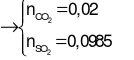
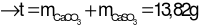
Câu 21:
16/07/2024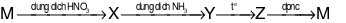 . Cho biết M là kim loại. Trong các nhận định sau:
. Cho biết M là kim loại. Trong các nhận định sau: (a) M, X, Y và Z đều tác dụng với dung dịch NaOH.
(b) M có tính khử yếu hơn magie.
(c) X vừa có tính oxi hóa, vừa có tính khử.
(d) Y có trong thành phần chính của đá saphia.
Số nhận định đúnglà
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
X là M(NO3)n
Y là M(OH)n
Z là M2On
M được điều chế bằng điện phân nóng chảy oxit nên M là Al
Các nhận định đúng là: (a), (b).
Câu 22:
16/07/2024Mẫu thử Thuốc thử | X | Y | Z | T |
Dung dịch Ba(OH)2 | Kết tủa màu trắng, sau đó tan hết | Khí mùi khai và kết tủa màu trắng | Có khí mùi khai | Có kết tủa màu nâu đỏ |
X, Y, Z, Tlần lượt là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
X là AlCl3, Y là (NH4)2SO4, Z là NH4NO3, T là FeCl3
Câu 23:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
B sai, CrO3là oxit axit
Câu 24:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Sự thiếu hụt nguyên tố canxi gây ra bệnh loãng xương.
Phần tự chọn: Dành cho Ban Khoa học Xã hội
Câu 25:
18/07/2024Câu 1:Để đánh giá độ nhiễm bẩn không khí của một nhà máy, người ta tiến hành như sau: lấy không khí rồi dẫn qua dung dịch Pb(NO3)2dư thì thu được chất kết tủa màu đen. Hiện tượng đó chứng tỏ trong không khí đã có:
D. NH3
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
H2S + Pb(NO3)2→ PbS (↓ đen) + 2HNO3
Câu 26:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Thép không phải hợp kim của nhôm, thép là hợp kim của sắt.
Câu 27:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
B sai, Al bị thụ động hoá trong HNO3đặc, nguội
Câu 28:
18/07/2024Câu 5:Ta có phương trình phản ứng hóa học sau:
Fe + HNO3(loãng) → (X) + (Y) + H2O
(X) và (Y) lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
X là Fe(NO3)3, Y là NO
Fe + 4HNO3→ Fe(NO3)3+ NO + 2H2O
Câu 29:
23/07/2024Câu 7:Nguyên tắc chung của quá trình sản xuất gang trong công nghiệp là khử oxit sắt ở nhiệt độ cao bằng chất khử
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Trong công nghiệp sản xuất gang, chất khử CO được dùng để khử oxit sắt
Câu 30:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Bảo toàn nguyên tố Al: 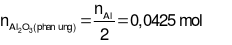
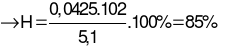
Câu 31:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Gọi công thức hoá học chung của hai muối là MCO3
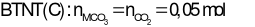
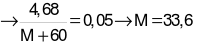
Vậy hai kim loại là Mg và Ca
Câu 32:
22/07/2024Câu 12:Trong xương động vật, nguyên tố canxi và photpho tồn tại chủ yếu dưới dạng Ca3(PO4)2. Nếu muốn nước xương thu được có nhiều canxi và photpho ta nên làm gì?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Khi hầm xương, muốn nước xương thu được giàu canxi và photpho ta nên ninh xương với một ít quả chua (me, khế,…) vì trong các quả chua có chứa axit, Ca3(PO4)2trong xương sẽ kết hợp với axit tạo thành muối tan Ca(H2PO4)2
Câu 33:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
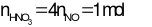
Câu 34:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Bảo toàn e: 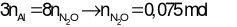
→ V = 1,68 lít = 1680 ml
Câu 35:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Công thức hoá học của kali cromat là K2CrO4
Câu 36:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Cho hỗn hợp kim loại tác dụng với KOH chỉ có Al phản ứng.
Bảo toàn e: 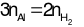
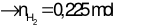
Câu 37:
16/07/2024Phèn chua em đánh nước nào cũng trong"
Ngoài công dụng dùng để đánh trong nước, phèn chua còn được sử dụng như một chất phụ gia để tăng thêm độ trắng, giòn, dai cho thức ăn, làm thuốc trị bệnh, dùng để tẩy trắng trong kỹ nghệ nhuộm, thuộc da… Công thức hoá học của phèn chua là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Công thức hoá học của phèn chua là K2SO4.Al2(SO4)3.24H2O.
Câu 38:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Cu không tác dụng được với dung dịch HCl.
Câu 39:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Ta có thể dùng thuốc thử là dung dịch KOH, to
Xuất hiện khí không màu, mùi khai là NH4Cl; không hiện tượng là KCl.
NH4Cl + KOH → KCl + NH3↑ + H2O
Câu 40:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Sự thiếu hụt nguyên tố canxi gây ra bệnh loãng xương.
Câu 41:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là:
nFe= 0,015 mol

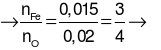 công thức hoá học của oxit sắt là Fe3O4
công thức hoá học của oxit sắt là Fe3O4
PHẦN TỰ LUẬN (4 điểm)
Thời gian làm bài: 20 phút (Không kể thời gian phát đề)
Câu 42:
20/07/2024(0.5 điểm):
Hỗn hợp Tecmit có thể dùng để hàn đường ray. Thành phần của hỗn hợp này gồm những chất nào? Xem đáp án
Xem đáp án
Hướng dẫn giải
Hỗn hợp tecmit gồm Al và oxit sắt.
Câu 43:
16/07/2024(0.5 điểm):
Điện phân (điện cực trơ, màng ngăn xốp) dung dịch gồm CuSO4và NaCl (tỉ lệ mol tương ứng 1:3) với cường độ dòng điện 1,34A. Sau thời gian t giờ, thu được dung dịch Y (chứa hai chất tan) có khối lượng giảm 10,375 gam so với dung dịch ban đầu. Cho bột Al dư vào Y, thu được 1,68 lít khí H2(đktc). Biết các phản ứng xảy ra hoàn toàn, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước. Tính giá trị của t. Xem đáp án
Xem đáp án
Hướng dẫn giải
Dung dịch Y chứa hai chất tan gồm Na2SO4và NaOH
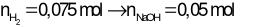
Đặt 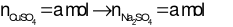
Bảo toàn Na → nNaCl= 2a + 0,05 mol
Theo đề → 2a + 0,05 = 3a → a = 0,05
Catot: 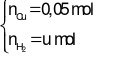
Anot: 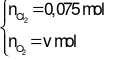
Bảo toàn e: 2u + 0,05.2 = 4v + 0,075.2
Khối lượng dung dịch giảm: mgiảm= 0,05.64 + 2u + 0,075.71 + 32v = 10,375
→ u = 0,125 mol và v = 0,05 mol
→ ne= 2u + 0,05.2 = 0,35
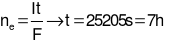
Câu 44:
20/07/2024(0.5 điểm):
Điền vào chỗ trống: “Trong phòng thí nghiệm, bạn Nam bỏ một ít dung dịch K2CrO4vào ống nghiệm. Dung dịch có màu ....(1)...., sau đó, bạn nhỏ vào vài giọt axit H2SO4, dung dịch chuyển sang màu ....(2).....” Xem đáp án
Xem đáp án
Hướng dẫn giải
(1) vàng
(2) da cam
Câu 45:
16/07/2024(0.5 điểm):
Cho các kim loại sau: Na, Ag, Cr, Li, Fe, Zn, Ala/ Kim loại nào tan được trong nước ở điều kiện thường?
b/ Kim loại nào thụ động trong dung dịch axit sunfuric đặc, nguội?
 Xem đáp án
Xem đáp án
Hướng dẫn giải
a. Các kim loại tan được trong nước ở điều kiện thường: Na, Li.
b. Kim loại thụ động trong dung dịch axit H2SO4đặc, nguội: Cr, Fe, Al.
Câu 46:
21/07/2024(0.5 điểm):
Viết phản ứng minh họa khi cho từ từ đến dư dung dịch KOH vào dung dịch AlCl3. Xem đáp án
Xem đáp án
Hướng dẫn giải
3KOH + AlCl3→ 3KCl + Al(OH)3↓
KOH dư+ Al(OH)3→ KAlO2+ 2H2O
Câu 47:
16/07/2024(0.5 điểm):
Cho 100ml dung dịch FeSO40,5 M Phản ứng với NaOH dư. Sau Phản ứng lọc lấy kết tủa rồi đem nung trong không khí đến khi khối luợng không đổi. Tính khối lượng chất rắn thu được sau khi nung. Xem đáp án
Xem đáp án
Hướng dẫn giải
Ta có sơ đồ:

Bảo toàn e: 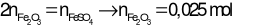

Câu 48:
20/07/2024(1.0 điểm):
Đọc bài viết sau và trả lời các câu hỏi bên dưới:THẠCH NHŨ
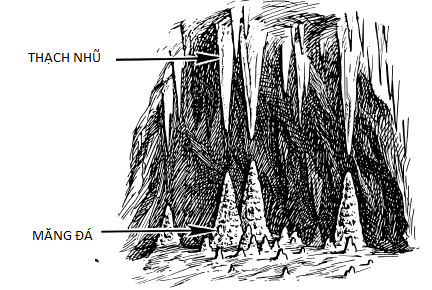 Thạch nhũ hay nhũ đá được hình thành do cặn của nước nhỏ giọt đọng lại trải qua hàng trăm, nghìn năm. Nó là khoáng vật hang độngthứ sinh treo trên trần hay tường của các hang động.
Thạch nhũ hay nhũ đá được hình thành do cặn của nước nhỏ giọt đọng lại trải qua hàng trăm, nghìn năm. Nó là khoáng vật hang độngthứ sinh treo trên trần hay tường của các hang động.
Thạch nhũ được tạo thành từ CaCO3và các khoáng chất khác kết tụ từ dung dịch nước khoáng. Đá vôilà đá chứa canxi cacbonat, nó có thể bị hoà tan trong nước có chứa khí cacbonictạo thành dung dịch Ca(HCO3)2. Phương trình phản ứng như sau:
CaCO3(r) + H2O(l) + CO2(kh) → Ca(HCO3)2(dd)
Dung dịch này chảy qua kẽ đá cho đến khi gặp vách đá hay trần đá và nhỏ giọt xuống. Khi dung dịch tiếp xúc với không khí, phản ứng hoá học tạo thành thạch nhũ như sau:
Ca(HCO3)2(dd) → CaCO3(r) + H2O(l) + CO2(dd)
Thạch nhũ "lớn" lên với tốc độ trung bình 0,13 mm một năm.
Mọi thạch nhũ đều bắt đầu với một giọt nước chứa đầy khoáng chất. Khi giọt nước này rơi xuống, nó để lại phía sau một vòng mỏng chứa canxi cacbonat. Mỗi giọt tiếp theo được hình thành và rơi xuống đều ngưng tụ một vòng canxi cacbonat khác. Cuối cùng, các vòng này tạo thành thạch nhũ. Cùng các giọt nước này rơi xuống từ đầu của thạch nhũ ngưng tụ nhiều canxi cacbonat hơn trên nền phía dưới, cuối cùng tạo thành măng đáthuôn tròn hay hình nón. Không giống như nhũ đá, các măng đá không bao giờ rỗng. Khi có đủ thời gian, các dạng hình thành này có thể gặp nhau và hợp nhất để tạo thành các cột đá.
 Xem đáp án
Xem đáp án
a. Thành phần hoá học của thạch nhũ là CaCO3
b. Phản ứng tạo thành thạch nhũ: Ca(HCO3)2(dd) → CaCO3(r) + H2O(l) + CO2(dd)
c. Thạch nhũ lớn lên với tốc độ trung bình 0,13mm một năm
→ thạch nhũ có chiều dài 1m cần trung bình 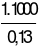 = 7692,308 năm
= 7692,308 năm
-----HẾT-----
Bài thi liên quan
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 1)
-
40 câu hỏi
-
50 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 2)
-
40 câu hỏi
-
50 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 3)
-
30 câu hỏi
-
50 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 4)
-
30 câu hỏi
-
50 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 5)
-
30 câu hỏi
-
40 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 7)
-
40 câu hỏi
-
50 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 8)
-
30 câu hỏi
-
50 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 9)
-
36 câu hỏi
-
50 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 10)
-
30 câu hỏi
-
50 phút
-
-
Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 11)
-
30 câu hỏi
-
50 phút
-
Có thể bạn quan tâm
- Đề thi Hóa Học 12 giữa kì 2 có đáp án (2827 lượt thi)
- 30 Câu trắc nghiệm bài thi giữa kì 2 có đáp án (307 lượt thi)
- 40 câu trắc nghiệm bài thi học kì 2 có đáp án (301 lượt thi)
- Top 12 Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Bài số 1) (2209 lượt thi)
- Top 9 Đề thi giữa kì 2 Hóa 12 có đáp án (Bài số 1) (1653 lượt thi)
- Top 8 Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Bài số 2) (1246 lượt thi)
- Top 9 Đề thi giữa kì 2 Hóa 12 có đáp án (Bài số 2) (3626 lượt thi)
- Top 9 Đề thi Hóa học 12 Học kì 2 có đáp án (1826 lượt thi)
- Đề thi cuối kì 2 Hóa 12 có đáp án (3192 lượt thi)
Các bài thi hot trong chương
- Top 4 Đề kiểm tra 15 phút Hóa 12 Học kì 1 có đáp án (Lần 1) (1138 lượt thi)
- Top 4 Đề thi Hóa học 12 Học kì 1 có đáp án (965 lượt thi)
- Top 4 Đề thi giữa kì 1 Hóa 12 có đáp án (Lần 1) (812 lượt thi)
- Top 4 Đề thi giữa kì 1 Hóa 12 có đáp án (Lần 2) (810 lượt thi)
- Top 4 Đề thi Hóa học 12 Học kì 1 chọn lọc, có đáp án (743 lượt thi)
- Đề kiểm tra 1 tiết Hóa học 12 có đáp án (Bài kiểm tra số 1) (368 lượt thi)
- Đề kiểm tra 1 tiết Hóa học 12 có đáp án (Bài kiểm tra số 2) (328 lượt thi)
- 40 Câu trắc nghiệm bài thi giữa kì 2 có đáp án (304 lượt thi)
