Chuyên đề Hóa 10 Bài 1: Liên kết hóa học có đáp án
Chuyên đề Hóa 10 Bài 1: Liên kết hóa học có đáp án
-
1365 lượt thi
-
24 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
23/07/2024Hình học phân tử (hình dạng phân tử) của một chất rất quan trọng trong việc xác định cách thức phân tử chất đó tương tác và phản ứng với các phân tử khác. Hình học phân tử cũng ảnh hưởng đến nhiệt độ sôi và nhiệt độ nóng chảy của chất. Nhiều đặc tính của chất được giải thích từ dữ liệu hình học phân tử của nó.
Yếu tố nào quyết định hình học phân tử các chất?

 Xem đáp án
Xem đáp án
Hình học một số phân tử chỉ phụ thuộc vào tổng số các cặp electron hóa trị (liên kết và chưa liên kết) của nguyên tử trung tâm.
Câu 2:
23/07/2024Viết công thức Lewis của nguyên tử oxygen và nguyên tử magnesium.
 Xem đáp án
Xem đáp án
- Công thức Lewis của nguyên tử oxygen:

- Công thức Lewis của nguyên tử magnesium:
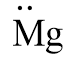
Câu 3:
23/07/2024Viết công thức electron của phân tử methane (CH4).
 Xem đáp án
Xem đáp án
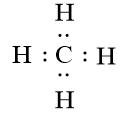
Câu 4:
23/07/2024Khi dùng chlorine để khử trùng hồ bơi, chlorine sẽ phản ứng với urea trong nước tiểu và mồ hôi người tắm, tạo hợp chất nitrogen trichloride (NCl3), gây ra nhiều tác động xấu đến sức khỏe như đỏ mắt, hen suyễn, …
Viết công thức Lewis của nitrogen trichloride.
 Xem đáp án
Xem đáp án
Bước 1: Tổng số electron hóa trị của phân tử NCl3 là:
5 + 7.3 = 26
Bước 2: Sơ đồ khung biểu diễn liên kết của phân tử NCl3:
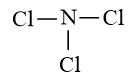
Bước 3: Số electron hóa trị chưa tham gia liên kết trong sơ đồ là:
26 – 2.3 = 20
Hoàn thiện octet cho các nguyên tử có độ âm điện lớn hơn trong sơ đồ (Cl có độ âm điện lớn hơn.
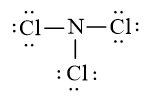
Số electron hóa trị còn lại: 20 – 6.3 = 2
Nguyên tử trung tâm N chưa đạt octet, dùng 2 electron còn lại tạo octet cho N.
Công thức Lewis của nitrogen trichloride (NCl3) là:
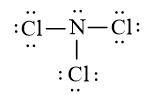
Câu 5:
21/07/2024Hãy tính tổng số electron hóa trị của phân tử BF3.
 Xem đáp án
Xem đáp án
B có 3 electron hóa trị, F có 7 electron hóa trị. Trong phân tử BF3 có 1 nguyên tử B và 3 nguyên tử F
⇒ Tổng số electron hóa trị là: 1.3 + 3.7 = 24 electron
Câu 6:
21/07/2024Xác định nguyên tử trung tâm trong BF3. Lập sơ đồ khung của phân tử BF3.
 Xem đáp án
Xem đáp án
B có độ âm điện nhỏ hơn F nên B là nguyên tử trung tâm.
Sơ đồ khung của phân tử BF3:
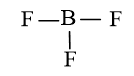
Câu 7:
19/07/2024Thực hiện Bước 3 cho phân tử BF3 và cho biết có cần tiếp tục bước 4?
 Xem đáp án
Xem đáp án
Bước 3: Số electron hóa trị chưa tham gia liên kết trong sơ đồ là:
24 – 2 × 3 = 18 electron
Hoàn thiện octet cho nguyên tử có độ âm điện lớn hơn trong sơ đồ:
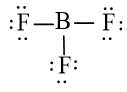
Số electron hóa trị còn lại: 18 – 18 = 0
Vì nguyên tử B chưa đạt octet nên vẫn cần thực hiện bước 4.
Bước 4: Nguyên tử B chưa được octet nên ta chuyển 1 cặp electron chưa liên kết của F tạo cặp electron chung
Vậy công thức Lewis của BF3
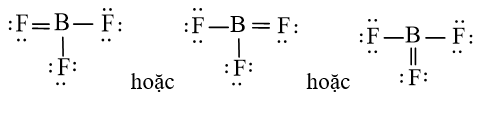
Câu 8:
19/07/2024Viết công thức Lewis của phân tử CCl4.
 Xem đáp án
Xem đáp án
Bước 1: C có 4 electron hóa trị, Cl có 7 electron hóa trị. Trong phân tử CCl4 có 1 nguyên tử C và 4 nguyên tử Cl.
⇒ Tổng số electron hóa trị của phân tử CCl4 là: 1.4 + 4.7 = 32 electron
Bước 2: Sơ đồ khung biểu diễn liên kết của phân tử CCl4
C có độ âm điện nhỏ hơn nên C là nguyên tử trung tâm.
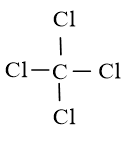
Bước 3: Số electron hóa trị chưa tham gia liên kết trong sơ đồ là: 32 – 2 × 4 = 24 electron
Hoàn thiện octet cho nguyên tử có độ âm điện lớn hơn trong sơ đồ:
Sử dụng 24 electron này để tạo octet cho Cl trước (vì Cl có độ âm điện cao hơn)
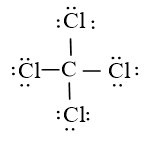
Bước 4: Nguyên tử C đã được octet. Vậy công thức Lewis của CCl4 là
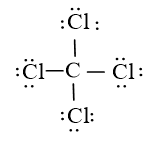
Câu 9:
15/07/2024Theo công thức Lewis của nước, phân tử nước có bao nhiêu cặp electron riêng ở nguyên tử trung tâm?
 Xem đáp án
Xem đáp án
Công thức Lewis của H2O là
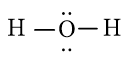
Phân tử nước có 2 cặp electron chung và 2 cặp electron riêng ở nguyên tử trung tâm (nguyên tử O).
Câu 10:
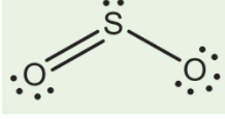
22/07/2024Xác định giá trị n, m trong công thức VSEPR của phân tử SO2. Cho biết công thức Lewis của SO2 là
 Xem đáp án
Xem đáp án
Dựa vào công thức Lewis của SO2 ta thấy:
+ n là số nguyên tử O liên kết với nguyên tử trung tâm S ⇒ n = 2.
+ m là số cặp electron riêng của nguyên tử trung tâm ⇒ m = 1.
Câu 11:
23/07/2024 Xem đáp án
Xem đáp án
- Từ công thức Lewis của H2O
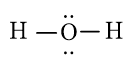
⇒ Công thức VSEPR của H2O là: AX2E2
- Từ công thức Lewis của NH3
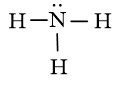
⇒ Công thức VSEPR của NH3 là: AX3E1
- Từ công thức Lewis của SO2
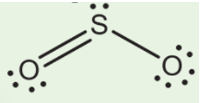
⇒ Công thức VSEPR của SO2 là AX2E1.
Câu 12:
22/07/2024Sử dụng mô hình VSEPR để dự đoán hình học của phân tử CS2.
 Xem đáp án
Xem đáp án
Công thức Lewis của CS2
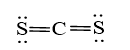
⇒ Công thức VSEPR của CS2 là: AX2
Xung quanh nguyên tử C có hai cặp electron chung (hai liên kết đôi), để giảm tối ta lực đẩy 2 cặp electron này phải chiếm 2 khu vực điện tích âm sao cho lực đẩy giữa chúng là nhỏ nhất
→ Phân tử CS2 có dạng đường thẳng theo mô hình VSEPR, góc hóa trị liên kết là 180o
Câu 13:
22/07/2024Vì sao góc liên kết HCH trong phân tử methane không thể là 90o?
 Xem đáp án
Xem đáp án
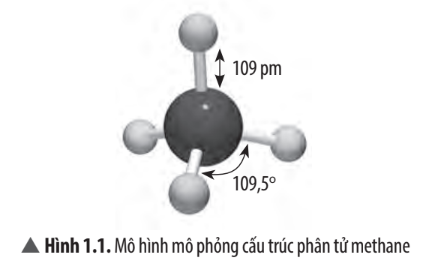
Vì xung quanh nguyên tử C có 4 cặp electron chung. Để giảm tối đa lực đẩy giữa 4 cặp electron chung, 4 cặp electron này phải chiếm 4 khu vực điện tích âm sao cho lực đẩy giữa chúng là nhỏ nhất nên phân tử có dạng tứ diện, góc liên kết = 109,5o
Câu 14:
13/07/2024Em có nhận xét gì về hình dạng, kích thước, năng lượng và hướng của các orbital nguyên tử lai hóa?
 Xem đáp án
Xem đáp án
Câu 15:
13/07/2024Nếu tổng số các AO tham gia lai hóa là 3 sẽ tạo ra bao nhiêu AO lai hóa?
 Xem đáp án
Xem đáp án
Câu 16:
21/07/2024Nguyên tử carbon trong phân tử CO2 ở trạng thái lai hóa nào? Giải thích liên kết hóa học tạo thành trong phân tử CO2 theo thuyết lai hóa.
 Xem đáp án
Xem đáp án
Công thức Lewis của CO2
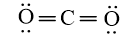
Công thức VSEPR của CO2 có dạng AX2
Từ công thức Lewis của CO2 ta xác định được phân tử này có dạng đường thẳng theo mô hình VSEPR.
Cấu hình electron của C (Z = 6) là 1s22s22p2.
1 AO 2s tổ hợp với 1 AO 2p, tạo 2 AO lai hóa sp
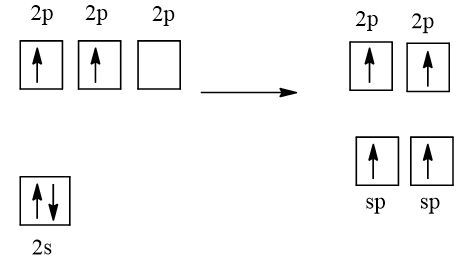
2 AO lai hóa này xen phủ trục với 2 AO 2p chứa electron độc thân của 2 nguyên tử O tạo thành liên kết σ.
Hai AO 2p không lai hóa của nguyên tử C có chứa electron độc thân xen phủ bên với 2AO 2p chứa electron độc thân còn lại của 2 nguyên tử O, tạo nên 2 liên kết π.
Câu 17:
21/07/2024Theo mô hình VSEPR, phân tử formaldehyde có dạng tam giác phẳng. Xác định trạng thái lai hóa của nguyên tử trung tâm carbon. Cho biết formaldehyde có công thức như hình sau đây:
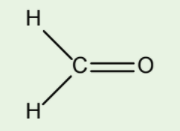
 Xem đáp án
Xem đáp án
Cấu hình electron của C (Z = 6) là 1s22s22p2.
1 AO 2s tổ hợp với 2 AO 2p tạo 3 AO lai hóa sp2.
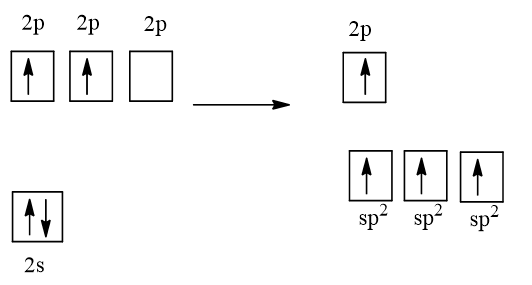
Vậy nguyên tử C trong phân tử formaldehyde lai hóa sp2
Câu 18:
20/07/2024Tương tự như công thức VSEPR, có thể dự đoán nhanh trạng thái lai hóa của nguyên tử A (nguyên tố s, p) trong một phân tử bất kì như sau:
- Xác định số nguyên tử liên kết trực tiếp với A.
- Xác định số cặp electron hóa trị riêng của A.
- Nếu tổng hai giá trị là 2; 3 hoặc 4 thì trạng thái lai hóa của A lần lượt là sp; sp2 hoặc sp3
Dự đoán trạng thái lai hóa của nguyên tử C, S và N trong các phân tử CO2, SO2 và NH3
 Xem đáp án
Xem đáp án
Trong phân tử CO2
- Số nguyên tử liên kết với C là 2.
- Số cặp electron hóa trị riêng của C là 0
- Tổng hai giá trị là 2 ⇒ Trạng thái lai hóa của C là sp.
Trong phân tử SO2
- Số nguyên tử liên kết với S là 2.
- Số cặp electron hóa trị riêng của S là 1
- Tổng hai giá trị là 3 ⇒ Trạng thái lai hóa của S là sp2.
Trong phân tử NH3
- Số nguyên tử liên kết với N là 3.
- Số cặp electron hóa trị riêng của N là 1
- Tổng hai giá trị là 4 ⇒ Trạng thái lai hóa của N là sp3.
Câu 19:
15/07/2024Phân tử chứa nguyên tử lai hóa sp3 có cấu trúc phẳng không? Giải thích và cho ví dụ.
 Xem đáp án
Xem đáp án
Phân tử chứa nguyên tử lai hóa sp3 không thể có cấu trúc phẳng. Vì khi 1 AO ns tổ hợp với 3 AO np tạo ra 4 AO lai hóa sp3. 4 AO sp3 này chiếm 4 khu vực điện tích âm sao cho lực đẩy giữa chúng là nhỏ nhất nên phân tử có dạng tứ diện, góc tạo bởi hai trục của hai AO là 109,5o.
Ví dụ phân tử CH4
Từ công thức Lewis của CH4 ta xác định được phân tử này có dạng tứ diện theo mô hình VSEPR.
Cấu hình electron của C (Z = 6) là 1s22s22p2
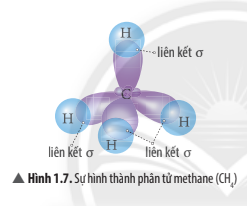
1 AO 2s tổ hợp với 3 AO 2p tạo 4 AO lai hóa sp3
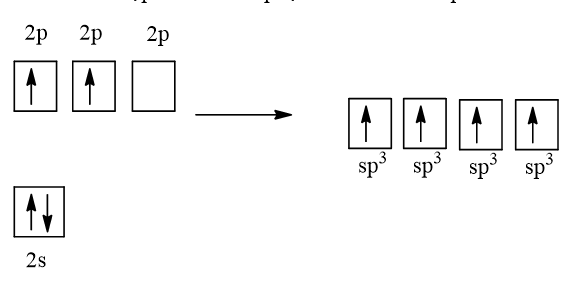
4 AO lai hóa sp3 của nguyên tử C xen phủ với 4 AO s của nguyên tử H tạo thành 4 liên kết σ hướng về 4 đỉnh của một tứ diện đều.
Câu 20:
13/07/2024Biết nguyên tử oxygen trong phân tử H2O ở trạng thái lai hóa sp3. Trình bày sự hình thành liên kết hóa học trong phân tử H2O
 Xem đáp án
Xem đáp án
Cấu hình electron của O (Z = 8) là 1s22s22p4
1 AO 2s tổ hợp với 3 AO 2p tạo 4 AO lai hóa sp3
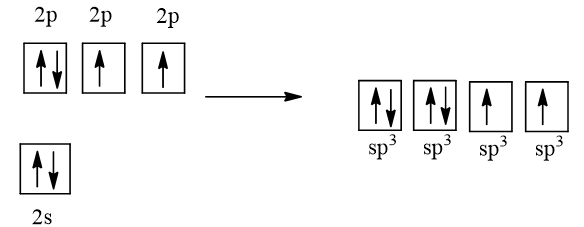
2 AO lai hóa sp3 chứa electron độc thân của nguyên tử O xen phủ với 2 AO s của nguyên tử H tạo thành 2 liên kết σ.
Câu 21:
23/07/2024Viết công thức Lewis của các phân tử sau:
a) HCN b) SO3
 Xem đáp án
Xem đáp án
a) Viết công thức Lewis của HCN
Bước 1: C có 4 electron hóa trị, H có 1 electron hóa trị, N có 5 electron hóa trị.
⇒ Tổng số electron hóa trị là: 4 + 1 + 5 = 10 electron.
Bước 2: Sơ đồ khung biểu diễn liên kết của phân tử HCN
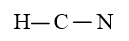
Bước 3: Số electron hóa trị chưa tham gia liên kết trong sơ đồ là: 10 – 2 × 2 = 6 electron
Hoàn thiện octet cho nguyên tử có độ âm điện lớn hơn trong sơ đồ:
Sử dụng 6 electron này để tạo octet cho N trước
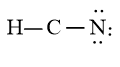
Bước 4: Đã sử dụng hết 6 electron để tạo octet cho N. Tuy nhiên C chưa đủ octet nên ta chuyển 2 cặp electron của nguyên tử N tạo thành cặp electron dùng chung giữa C và N. Nguyên tử H đã đủ octet
Vậy công thức Lewis của HCN là:
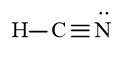
b) Viết công thức Lewis của SO3
Bước 1: S có 6 electron hóa trị, O có 6 electron hóa trị. Trong phân tử SO3, có 1 nguyên tử S và 3 nguyên tử O
⇒ Tổng số electron hóa trị là: 1.6 + 3.6 = 24 electron
Bước 2: Sơ đồ khung biểu diễn liên kết của phân tử SO3
S có độ âm điện nhỏ hơn nên S là nguyên tử trung tâm.
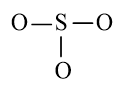
Bước 3: Số electron hóa trị chưa tham gia liên kết trong sơ đồ là: 24 – 2 × 3 = 18 electron
Hoàn thiện octet cho nguyên tử có độ âm điện lớn hơn trong sơ đồ:
Sử dụng 18 electron này để tạo octet cho O trước (vì O có độ âm điện cao hơn)
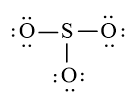
Bước 4: Đã sử dụng hết 18 electron để tạo octet cho O. Tuy nhiên S chưa đủ octet nên ta chuyển 1 cặp electron của nguyên tử O tạo thành cặp electron dùng chung.
Vậy công thức Lewis của SO3 là:

Câu 22:
22/07/2024Viết công thức VSEPR và dự đoán hình học của các phân tử sau:
a) HCN b) SO3 c) PH3
 Xem đáp án
Xem đáp án
a) Công thức Lewis của HCN là:
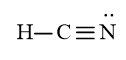
⇒ Công thức VSEPR của HCN là AX2
⇒ HCN có dạng đường thẳng
b) Từ công thức Lewis của SO3
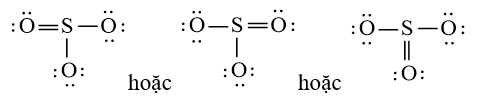
⇒ Công thức VSEPR của SO3 là: AX3
⇒ SO3 có dạng tam giác phẳng.
c) Công thức Lewis của PH3 là
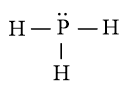
⇒ Công thức VSEPR của PH3 là: AX3E1
⇒ Để giảm tối đa lực đẩy giữa 4 cặp electron hóa trị (gồm 3 cặp electron chung và 1 cặp electron riêng), 4 cặp electron này phải chiếm 4 khu vực điện tích âm sao cho lực đẩy giữa chúng là nhỏ nhất. Tuy nhiên cặp electron riêng đẩy mạnh hơn làm góc liên kết giảm, nên nhỏ hơn 109,5o
Câu 23:
22/07/2024Trình bày sự tạo thành liên kết hóa học trong các phân tử sau dựa vào sự lai hóa của các nguyên tử trung tâm:
a) C2H2 b) C2H4 c) NH3
 Xem đáp án
Xem đáp án
a) Công thức Lewis của C2H2 là:
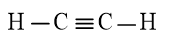
Cấu hình electron của nguyên tử C là: 1s22s22p2
1 AO 2s tổ hợp với 1 AO 2p, tạo 2 AO lai hóa sp
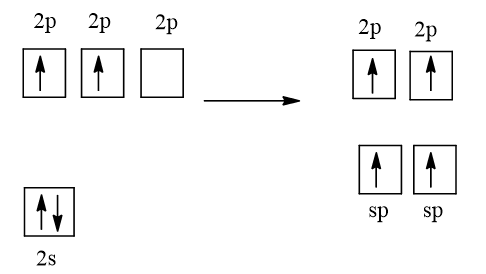
Mỗi nguyên tử C ở trạng thái lai hóa sp. Mỗi nguyên tử C dùng 1 AO lai hóa sp để xen phủ với nhau tạo ra liên kết σC-C. Mỗi nguyên tử C dùng AO lai hóa sp còn lại để xen phủ với AO 1s của một nguyên tử H tạo ra liên kết σC-H. Mỗi nguyên tử C còn lại 2 AO 2p song song từng đôi một. Chúng xen phủ bên với nhau tạo ra 2 liên kết πC-C. Như vậy trong phân tử C2H2 có 3 liên kết σ và 2 liên kết π.
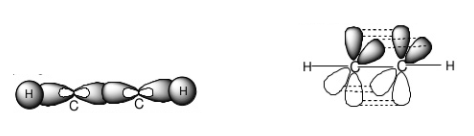
b) Công thức Lewis của C2H4 là:
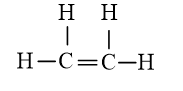
Cấu hình electron của nguyên tử C là: 1s22s22p2
1 AO 2s tổ hợp với 2 AO 2p tạo 3 AO lai hóa sp2.
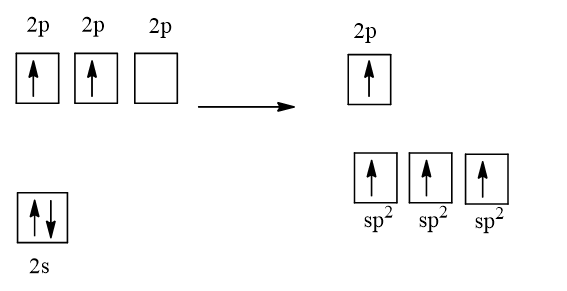
Trong phân tử C2H4 mỗi nguyên tử C có sự lai hóa sp2. Mỗi nguyên tử C dùng 1 AO lai hóa để xen phủ với nhau tạo ra liên kết σC-C. Mỗi nguyên tử C dùng AO lai hóa còn lại để xen phủ với AO 1s của một nguyên tử H tạo ra liên kết σC-H. Mỗi nguyên tử C còn 1 AO p không tham gia lai hóa sẽ xen phủ bên với nhau tạo liên kết πC-C. Như vậy trong phân tử C2H4 có 5 liên kết σ và 1 liên kết π.
c) Công thức Lewis của NH3 là:
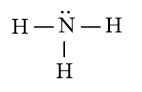
⇒ Công thức VSEPR của NH3 là: AX3E1
Từ công thức VSEPR dự đoán được trạng thái lai hóa của nguyên tử N trong phân tử NH3 là sp3.
Cấu hình electron của N là: 1s22s22p3
1 AO 2s tổ hợp với 3 AO 2p tạo 4 AO lai hóa sp3
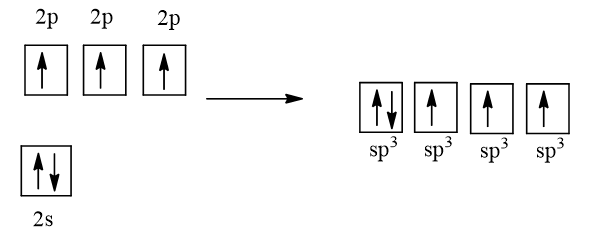
Ba AO lai hóa sp3 (chứa electron độc thân) của nguyên tử N xen phủ với AO 1s của 3 nguyên tử H, tạo va liên kết σ, hướng về ba đỉnh của hình tứ diện. Nguyên tử N còn 1 AO lai hóa sp3 chứa một cặp electron chưa liên kết nằm hướng về đỉnh còn lại của tứ diện. Tuy nhiên cặp electron chưa liên kết này đẩy mạnh hơn nên làm góc liên kết giảm, nên nhỏ hơn 109,5o
Câu 24:
21/07/2024Dự đoán trạng thái lai hóa của nguyên tử trung tâm trong các phân tử sau:
a) PCl3 b) CS2 c) SO2
 Xem đáp án
Xem đáp án
Lưu ý: Có thể dự đoán nhanh trạng thái lai hóa của nguyên tử A (nguyên tố s, p) trong một phân tử bất kì như sau:
- Xác định số nguyên tử liên kết trực tiếp với A.
- Xác định số cặp electron hóa trị riêng của A.
- Nếu tổng hai giá trị là 2; 3 hoặc 4 thì trạng thái lai hóa của A lần lượt là sp; sp2 hoặc sp3
a) Trong phân tử PCl3
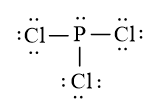
- Số nguyên tử liên kết với P là 3.
- Số cặp electron hóa trị riêng của P là 1
- Tổng hai giá trị là 4 ⇒ Trạng thái lai hóa của C là sp3.
b) Trong phân tử CS2
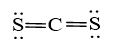
- Số nguyên tử liên kết với C là 2.
- Số cặp electron hóa trị riêng của C là 0
- Tổng hai giá trị là 2 ⇒ Trạng thái lai hóa của C là sp.
c) Trong phân tử SO2
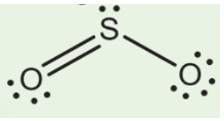
- Số nguyên tử liên kết với S là 2.
- Số cặp electron hóa trị riêng của S là 1
- Tổng hai giá trị là 3 ⇒ Trạng thái lai hóa của S là sp2.
