Câu hỏi:
22/07/2024 107
Những electron như thế nào được gọi là:
a) Electron hóa trị
b) Electron chung
c) Electron hóa trị riêng
Những electron như thế nào được gọi là:
a) Electron hóa trị
b) Electron chung
c) Electron hóa trị riêng
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
a) Electron hóa trị là những electron ở các orbital của lớp ngoài cùng và phân lớp sát ngoài cùng chưa bão hòa, có thể tham gia vào việc hình thành liên kết hóa học.
b) Electron chung là những electron hóa trị mà tham gia vào việc hình thành liên kết hóa học.
c) Electron hóa trị riêng là những electron hóa trị nhưng không tham gia vào việc hình thành liên kết hóa học.
Ví dụ:
- Nguyên tử Cl có có cấu hình electron là 1s22s22p63s23p5
⇒ Nguyên tử Cl có 7 electron hóa trị
- Phân tử Cl2 có liên kết giữa hai nguyên tử Cl được thực hiện nhờ 1 đôi electron góp chung; các electron còn lại được gọi là electron hóa trị riêng. 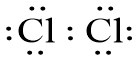
a) Electron hóa trị là những electron ở các orbital của lớp ngoài cùng và phân lớp sát ngoài cùng chưa bão hòa, có thể tham gia vào việc hình thành liên kết hóa học.
b) Electron chung là những electron hóa trị mà tham gia vào việc hình thành liên kết hóa học.
c) Electron hóa trị riêng là những electron hóa trị nhưng không tham gia vào việc hình thành liên kết hóa học.
Ví dụ:
- Nguyên tử Cl có có cấu hình electron là 1s22s22p63s23p5
⇒ Nguyên tử Cl có 7 electron hóa trị
- Phân tử Cl2 có liên kết giữa hai nguyên tử Cl được thực hiện nhờ 1 đôi electron góp chung; các electron còn lại được gọi là electron hóa trị riêng.
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 2:
Trình bày sự hình thành lai hóa sp3 của nguyên tử C trong CH4 và hình thành các liên kết trong phân tử này.
Trình bày sự hình thành lai hóa sp3 của nguyên tử C trong CH4 và hình thành các liên kết trong phân tử này.
Câu 5:
Xác định công thức Lewis của nitric acid HNO3. Cho biết nguyên tử H liên kết với O mà không phải với N.
Xác định công thức Lewis của nitric acid HNO3. Cho biết nguyên tử H liên kết với O mà không phải với N.
Câu 7:
Viết công thức Lewis và xác định dạng hình học của CS2. Xác định dạng lai hóa của nguyên tử trung tâm C trong phân tử này.
Viết công thức Lewis và xác định dạng hình học của CS2. Xác định dạng lai hóa của nguyên tử trung tâm C trong phân tử này.
Câu 8:
Dựa theo công thức Lewis của CHCl3 xác định được dạng lai hóa của nguyên tử trung tâm C trong phân tử này là
A. sp B. sp2 C. sp3
Dựa theo công thức Lewis của CHCl3 xác định được dạng lai hóa của nguyên tử trung tâm C trong phân tử này là
A. sp B. sp2 C. sp3
Câu 9:
Viết công thức Lewis của H2O. Dự đoán dạng hình học phân tử và dạng lai hóa của nguyên tử trung tâm.
Viết công thức Lewis của H2O. Dự đoán dạng hình học phân tử và dạng lai hóa của nguyên tử trung tâm.
Câu 11:
Theo em, dạng hình học nào sau đây của hai phân tử carbon dioxide và nước là đúng?
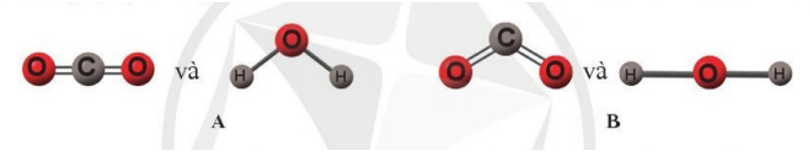
Theo em, dạng hình học nào sau đây của hai phân tử carbon dioxide và nước là đúng?
Câu 12:
Phân tử acetone có dạng tam giác phẳng theo mô hình VSEPR. Xác định dạng lai hóa của nguyên tử trung tâm X. Biết công thức của acetone là
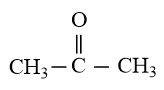
Phân tử acetone có dạng tam giác phẳng theo mô hình VSEPR. Xác định dạng lai hóa của nguyên tử trung tâm X. Biết công thức của acetone là
Câu 13:
Giải thích vì sao khi xung quanh nguyên tử trung tâm có 3 đám mây electron hóa trị E thì 3 đám mây này có xu hướng nằm ở 3 đỉnh của một tam giác phẳng.
Giải thích vì sao khi xung quanh nguyên tử trung tâm có 3 đám mây electron hóa trị E thì 3 đám mây này có xu hướng nằm ở 3 đỉnh của một tam giác phẳng.
Câu 14:
Nguyên tử C trong CO2 có dạng lai hóa gì? Trình bày sự hình thành dạng lai hóa đó.
Nguyên tử C trong CO2 có dạng lai hóa gì? Trình bày sự hình thành dạng lai hóa đó.


