Câu hỏi:
22/07/2024 148
Nêu ứng dụng trong đời sống, sản xuất của một số muối sulfate mà em biết.
Nêu ứng dụng trong đời sống, sản xuất của một số muối sulfate mà em biết.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Muối sulfate có nhiều ứng dụng trong đời sống và sản xuất.
- Calcium sulfate (CaSO4) được dùng trong sản xuất vật liệu xây dựng; làm chất phụ gia để làm đông các sản phẩm như đậu hũ, đậu non…
- Barium sulfate (BaSO4) được sử dụng như một loại bột màu làm phụ gia pha màu cho công nghiệp sơn, cho thuỷ tinh, cho gốm sứ cách điện và cao su chất lượng cao…
- Magnesium sulfate (MgSO4) được sử dụng sản xuất muối tắm; làm giảm dịu cơ bắp khi sưng tấy cho con người; bổ sung magnesium cho tôm, cá, động vật thuỷ sinh khác, …
- Ammonium sulfate (NH4)2SO4 là thành phần của thuốc trừ sâu hoà tan, thuốc diệt nấm, phân bón, sử dụng kết hợp với chlorine để tạo monochloramine để khử trùng nước uống…
Muối sulfate có nhiều ứng dụng trong đời sống và sản xuất.
- Calcium sulfate (CaSO4) được dùng trong sản xuất vật liệu xây dựng; làm chất phụ gia để làm đông các sản phẩm như đậu hũ, đậu non…
- Barium sulfate (BaSO4) được sử dụng như một loại bột màu làm phụ gia pha màu cho công nghiệp sơn, cho thuỷ tinh, cho gốm sứ cách điện và cao su chất lượng cao…
- Magnesium sulfate (MgSO4) được sử dụng sản xuất muối tắm; làm giảm dịu cơ bắp khi sưng tấy cho con người; bổ sung magnesium cho tôm, cá, động vật thuỷ sinh khác, …
- Ammonium sulfate (NH4)2SO4 là thành phần của thuốc trừ sâu hoà tan, thuốc diệt nấm, phân bón, sử dụng kết hợp với chlorine để tạo monochloramine để khử trùng nước uống…
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Viết phương trình hoá học khi cho dung dịch H2SO4 đặc tác dụng với KBr, C. Cho biết sản phẩm khử duy nhất là SO2.
Viết phương trình hoá học khi cho dung dịch H2SO4 đặc tác dụng với KBr, C. Cho biết sản phẩm khử duy nhất là SO2.
Câu 2:
Dung dịch sulfuric acid đặc được dùng làm khô khí nào trong số các khí sau: CO, H2, CO2, SO2, O2 và NH3. Giải thích.
Dung dịch sulfuric acid đặc được dùng làm khô khí nào trong số các khí sau: CO, H2, CO2, SO2, O2 và NH3. Giải thích.
Câu 3:
Có 4 mẫu sau: dung dịch NaOH, dung dịch HCl, dung dịch H2SO4 và H2O được kí hiệu bằng các chữ cái A, B, C và D (không theo trình tự trên). Kết quả của những thí nghiệm nhận biết những mẫu này được ghi trong bảng sau
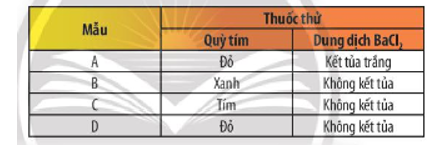
Hãy cho biết A, B, C và D là kí hiệu của những chất nào. Giải thích và viết phương trình hoá học của các phản ứng xảy ra.
Có 4 mẫu sau: dung dịch NaOH, dung dịch HCl, dung dịch H2SO4 và H2O được kí hiệu bằng các chữ cái A, B, C và D (không theo trình tự trên). Kết quả của những thí nghiệm nhận biết những mẫu này được ghi trong bảng sau

Hãy cho biết A, B, C và D là kí hiệu của những chất nào. Giải thích và viết phương trình hoá học của các phản ứng xảy ra.
Câu 4:
Hãy cho biết giai đoạn nào trong quá trình sản xuất H2SO4 có nguy cơ cao gây ô nhiễm môi trường. Giải thích.
Hãy cho biết giai đoạn nào trong quá trình sản xuất H2SO4 có nguy cơ cao gây ô nhiễm môi trường. Giải thích.
Câu 5:
Hãy giải thích vì sao ở giai đoạn tạo ra SO3, người ta chọn điều kiện phản ứng ở nhiệt độ cao (450 oC – 500 oC).
Hãy giải thích vì sao ở giai đoạn tạo ra SO3, người ta chọn điều kiện phản ứng ở nhiệt độ cao (450 oC – 500 oC).
Câu 6:
Cho các dung dịch không màu của mỗi chất sau: K2CO3, Na2SO4, Ba(NO3)2. Hãy trình bày cách phân biệt các dung dịch đã cho bằng phương pháp hoá học. Viết phương trình hoá học của các phản ứng xảy ra.
Cho các dung dịch không màu của mỗi chất sau: K2CO3, Na2SO4, Ba(NO3)2. Hãy trình bày cách phân biệt các dung dịch đã cho bằng phương pháp hoá học. Viết phương trình hoá học của các phản ứng xảy ra.
Câu 7:
Tính chất nào sau đây không phải là tính chất của dung dịch sulfuric acid đặc?
A. Tính háo nước.
B. Tính oxi hoá.
C. Tính acid.
D. Tính khử.
Tính chất nào sau đây không phải là tính chất của dung dịch sulfuric acid đặc?
A. Tính háo nước.
B. Tính oxi hoá.
C. Tính acid.
D. Tính khử.
Câu 8:
Quan sát Hình 7.6, trình bày cách nhận biết ion SO42-. Nêu hiện tượng xảy ra, viết phương trình hoá học.

Quan sát Hình 7.6, trình bày cách nhận biết ion SO42-. Nêu hiện tượng xảy ra, viết phương trình hoá học.

Câu 9:
Để nhận biết anion có trong dung dịch K2SO4, không thể dùng thuốc thử nào sau đây?
A. Ba(OH)2.
B. BaCl2.
C. Ba(NO3)2.
D. MgCl2.
Để nhận biết anion có trong dung dịch K2SO4, không thể dùng thuốc thử nào sau đây?
A. Ba(OH)2.
B. BaCl2.
C. Ba(NO3)2.
D. MgCl2.
Câu 10:
Quan sát Hình 7.5, mô tả cách pha loãng sulfuric acid. Giải thích.
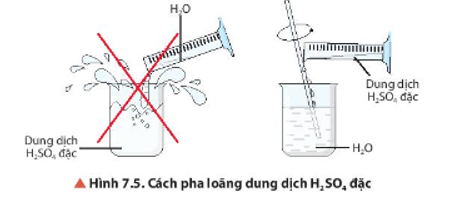
Quan sát Hình 7.5, mô tả cách pha loãng sulfuric acid. Giải thích.

Câu 12:
Quan sát Hình 7.1, nhận xét màu, trạng thái của sulfuric acid ở điều kiện thường và cho biết tại sao sulfuric acid lại không bay hơi.
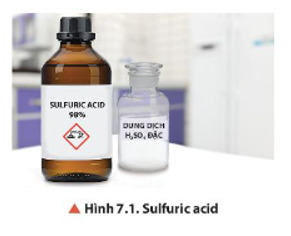
Quan sát Hình 7.1, nhận xét màu, trạng thái của sulfuric acid ở điều kiện thường và cho biết tại sao sulfuric acid lại không bay hơi.

Câu 13:
Viết quá trình oxi hoá và quá trình khử trong phản ứng của dung dịch H2SO4 đặc với Cu ở Thí nghiệm 1.
Viết quá trình oxi hoá và quá trình khử trong phản ứng của dung dịch H2SO4 đặc với Cu ở Thí nghiệm 1.
Câu 14:
Quan sát Hình 7.3, nêu hiện tượng, viết phương trình hoá học xảy ra (nếu có).

Quan sát Hình 7.3, nêu hiện tượng, viết phương trình hoá học xảy ra (nếu có).