Câu hỏi:
23/07/2024 618
Đốt cháy hết 0,54 gam Al trong không khí thu được aluminium oxide theo sơ đồ phản ứng:
Al + O2 → Al2O3
Lập phương trình hoá học của phản ứng rồi tính:
a) Khối lượng aluminium oxide tạo ra.
Đốt cháy hết 0,54 gam Al trong không khí thu được aluminium oxide theo sơ đồ phản ứng:
Al + O2 → Al2O3
Lập phương trình hoá học của phản ứng rồi tính:
a) Khối lượng aluminium oxide tạo ra.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Phương trình hoá học: 4Al + 3O2 → 2Al2O3.
Số mol Al tham gia phản ứng:
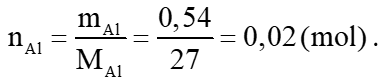
a) Từ phương trình hoá học ta có:
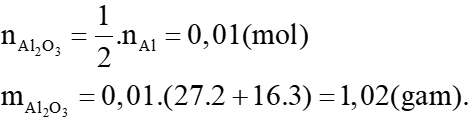
Phương trình hoá học: 4Al + 3O2 → 2Al2O3.
Số mol Al tham gia phản ứng:
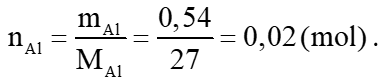
a) Từ phương trình hoá học ta có:
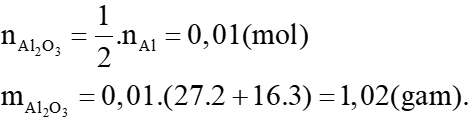
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Trong công nghiệp, nhôm được sản xuất từ aluminium oxide (Al2O3) theo phương trình hoá học sau:
2Al2O3 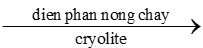 4Al + 3O2↑
4Al + 3O2↑
a) Tính hiệu suất phản ứng khi điện phân 102 kg Al2O3, biết khối lượng nhôm thu được sau phản ứng là 51,3 kg.
Trong công nghiệp, nhôm được sản xuất từ aluminium oxide (Al2O3) theo phương trình hoá học sau:
2Al2O3 ![]() 4Al + 3O2↑
4Al + 3O2↑
a) Tính hiệu suất phản ứng khi điện phân 102 kg Al2O3, biết khối lượng nhôm thu được sau phản ứng là 51,3 kg.
Câu 2:
b*) Biết khối lượng nhôm thu được sau điện phân là 54 kg và hiệu suất phản ứng là 92%, tính khối lượng Al2O3 đã dùng.
b*) Biết khối lượng nhôm thu được sau điện phân là 54 kg và hiệu suất phản ứng là 92%, tính khối lượng Al2O3 đã dùng.
Câu 3:
Đốt cháy 1 mol khí hydrogen trong 0,4 mol khí oxygen đến khi phản ứng xảy ra hoàn toàn. Cho biết chất nào còn dư sau phản ứng.
Đốt cháy 1 mol khí hydrogen trong 0,4 mol khí oxygen đến khi phản ứng xảy ra hoàn toàn. Cho biết chất nào còn dư sau phản ứng.
Câu 7:
Trong công nghiệp, người ta sản xuất nhôm từ aluminium oxide (Al2O3). Làm thế nào tính được khối lượng nguyên liệu cần dùng để sản xuất nhôm hoặc tính khối lượng nhôm tạo ra nếu biết khối lượng nguyên liệu đã dùng?
Trong công nghiệp, người ta sản xuất nhôm từ aluminium oxide (Al2O3). Làm thế nào tính được khối lượng nguyên liệu cần dùng để sản xuất nhôm hoặc tính khối lượng nhôm tạo ra nếu biết khối lượng nguyên liệu đã dùng?


