Câu hỏi:
22/07/2024 375
Cho 4,2 gam Fe phản ứng hoàn toàn với lượng dư dung dịch HNO3, thể tích khí NO (đkc) bay ra là (coi NO là sản phẩm khử duy nhất)
Cho 4,2 gam Fe phản ứng hoàn toàn với lượng dư dung dịch HNO3, thể tích khí NO (đkc) bay ra là (coi NO là sản phẩm khử duy nhất)
A. 1,8593 lít.
A. 1,8593 lít.
B. 3,3600 lít.
C. 3,7185 lít .
C. 3,7185 lít .
D. 5,6360 lít.
D. 5,6360 lít.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Theo phương trình hoá học:
Vậy VNO = 0,075.24,79 = 1,8593 (lít).
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Theo phương trình hoá học:
Vậy VNO = 0,075.24,79 = 1,8593 (lít).
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Xác định biến thiên enthalpy chuẩn của phản ứng:
C2H2(g) + 2H2(g) ® C2H6(g)
Biết năng lượng liên kết (ở điều kiện chuẩn): Eb (H–H) = 436 kJ/mol; Eb (C–H) = 418 kJ/mol; Eb (CºC) = 837 kJ/mol.
Xác định biến thiên enthalpy chuẩn của phản ứng:
C2H2(g) + 2H2(g) ® C2H6(g)
Biết năng lượng liên kết (ở điều kiện chuẩn): Eb (H–H) = 436 kJ/mol; Eb (C–H) = 418 kJ/mol; Eb (CºC) = 837 kJ/mol.
Câu 3:
Trên thế giới, zinc (kẽm) được sản xuất chủ yếu từ quặng zinc blende có thành phần chính là ZnS. Ở giai đoạn đầu của quá trình sản xuất, quặng zinc blende được nung trong không khí để thực hiện phản ứng:
ZnS + O2 ZnO + SO2
Tổng hệ số cân bằng (là các số nguyên, tối giản) của chất tham gia trong phản ứng là
Trên thế giới, zinc (kẽm) được sản xuất chủ yếu từ quặng zinc blende có thành phần chính là ZnS. Ở giai đoạn đầu của quá trình sản xuất, quặng zinc blende được nung trong không khí để thực hiện phản ứng:
ZnS + O2 ZnO + SO2
Tổng hệ số cân bằng (là các số nguyên, tối giản) của chất tham gia trong phản ứng là
Câu 4:
Phosgene (COCl2) là một hợp chất hữu cơ, nó còn được gọi với tên là chất độc quang khí. Phosgene được điều chế bằng cách cho hỗn hợp CO và Cl2 đi qua than hoạt tính.
Biết ở điều kiện chuẩn: Eb(Cl-Cl) = 243 kJ/mol; Eb(C-Cl) = 339 kJ/mol; Eb(C=O) = 745 kJ/mol; Eb(C≡O) = 1075 kJ/mol. Tính biến thiên enthalpy chuẩn của phản ứng tạo thành phosgene từ CO và Cl2.
Phosgene (COCl2) là một hợp chất hữu cơ, nó còn được gọi với tên là chất độc quang khí. Phosgene được điều chế bằng cách cho hỗn hợp CO và Cl2 đi qua than hoạt tính.
Biết ở điều kiện chuẩn: Eb(Cl-Cl) = 243 kJ/mol; Eb(C-Cl) = 339 kJ/mol; Eb(C=O) = 745 kJ/mol; Eb(C≡O) = 1075 kJ/mol. Tính biến thiên enthalpy chuẩn của phản ứng tạo thành phosgene từ CO và Cl2.
Câu 6:
Cho phản ứng sau:
SO2(g) + O2(g) ® SO3(l)
Biến thiên enthalpy chuẩn của phản ứng tính theo nhiệt tạo thành là
Cho phản ứng sau:
SO2(g) + O2(g) ® SO3(l)
Biến thiên enthalpy chuẩn của phản ứng tính theo nhiệt tạo thành là
Câu 7:
Cho các hợp chất sau: NH3; NH4Cl; NaNO3; HNO3; N2O5. Số hợp chất trong đó nitrogen có số oxi hoá -3 là
Cho các hợp chất sau: NH3; NH4Cl; NaNO3; HNO3; N2O5. Số hợp chất trong đó nitrogen có số oxi hoá -3 là
Câu 8:
Phương trình nhiệt học của phản ứng nhiệt phân hoàn toàn 1 mol Cu(OH)2 ở điều kiện chuẩn, tạo thành 1 mol CuO và 1 mol H2O, thu vào nhiệt lượng 9,0 kJ là
Câu 9:
Cho các phát biểu sau:
(a). Trong phòng thí nghiệm, có thể nhận biết một phản ứng thu nhiệt hoặc toả nhiệt bằng cách đo nhiệt độ của phản ứng bằng một nhiệt kế.
(b). Nhiệt độ của hệ phản ứng sẽ tăng lên nếu phản ứng thu nhiệt.
(c). Nhiệt độ của hệ phản ứng sẽ tăng lên nếu phản ứng toả nhiệt.
(d). Nhiệt độ của hệ phản ứng sẽ giảm đi nếu phản ứng toả nhiệt.
(e). Nhiệt độ của hệ phản ứng sẽ giảm đi nếu phản ứng thu nhiệt.
Số phát biểu không đúng là
Cho các phát biểu sau:
(a). Trong phòng thí nghiệm, có thể nhận biết một phản ứng thu nhiệt hoặc toả nhiệt bằng cách đo nhiệt độ của phản ứng bằng một nhiệt kế.
(b). Nhiệt độ của hệ phản ứng sẽ tăng lên nếu phản ứng thu nhiệt.
(c). Nhiệt độ của hệ phản ứng sẽ tăng lên nếu phản ứng toả nhiệt.
(d). Nhiệt độ của hệ phản ứng sẽ giảm đi nếu phản ứng toả nhiệt.
(e). Nhiệt độ của hệ phản ứng sẽ giảm đi nếu phản ứng thu nhiệt.
Số phát biểu không đúng là
Câu 10:
Biến thiên enthalpy chuẩn của một phản ứng được mô tả ở sơ đồ dưới đây:
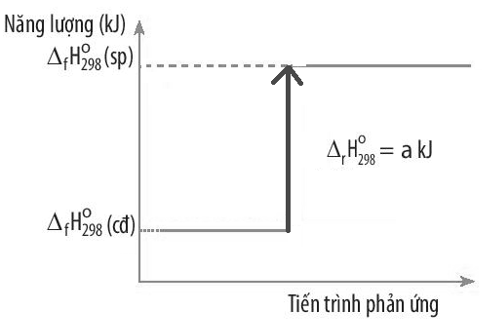
Kết luận nào sau đây đúng?
Biến thiên enthalpy chuẩn của một phản ứng được mô tả ở sơ đồ dưới đây:

Kết luận nào sau đây đúng?
Câu 11:
Cho phản ứng sau:
C(s) + O2(g) → CO2(g)
Nhiệt tạo thành chuẩn của CO2(g) là
Cho phản ứng sau:
C(s) + O2(g) → CO2(g)
Nhiệt tạo thành chuẩn của CO2(g) là
Câu 12:
b) Hợp chất CO2(g) bền hơn hay kém bền hơn về mặt năng lượng so với các đơn chất bền C(graphite) và O2(g).
b) Hợp chất CO2(g) bền hơn hay kém bền hơn về mặt năng lượng so với các đơn chất bền C(graphite) và O2(g).
Câu 13:
Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất, kí hiệu là
Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất, kí hiệu là
Câu 14:
Cho các phản ứng sau:
(1) H2(g) + Cl2(g) ® 2HCl (g)
(2) CH4(g) + H2O(l) → CO(g) + 3H2(g)
Phát biểu đúng là
Cho các phản ứng sau:
(1) H2(g) + Cl2(g) ® 2HCl (g)
(2) CH4(g) + H2O(l) → CO(g) + 3H2(g)
Phát biểu đúng là
Câu 15:
Biết rằng ở điều kiện chuẩn, 1 mol ethanol cháy tỏa ra một nhiệt lượng là 1,37 × 103 kJ. Nếu đốt cháy hoàn toàn 15,1 gam ethanol, năng được được giải phóng ra dưới dạng nhiệt bởi phản ứng là
A. 0,450 kJ.
B. 2,25 × 103 kJ.
C. 4,50 × 102 kJ.
D. 1,37 × 103 kJ.
ethanol, năng được được giải phóng ra dưới dạng nhiệt bởi phản ứng là
Biết rằng ở điều kiện chuẩn, 1 mol ethanol cháy tỏa ra một nhiệt lượng là 1,37 × 103 kJ. Nếu đốt cháy hoàn toàn 15,1 gam ethanol, năng được được giải phóng ra dưới dạng nhiệt bởi phản ứng là
A. 0,450 kJ.
B. 2,25 × 103 kJ.
C. 4,50 × 102 kJ.
D. 1,37 × 103 kJ.
ethanol, năng được được giải phóng ra dưới dạng nhiệt bởi phản ứng là


