Nguyên tắc sắp xếp các nguyên tố trong bảng
Với lí thuyết trang 91,92,93,94 vbt Hóa học lớp 9 được biên soạn lời giải chi tiết sẽ giúp học sinh biết cách làm bài tập môn Hóa 9. Mời các bạn đón xem:
Giải VBT Hóa 9 Bài 31: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Lí thuyết trang 91,92,93,94 VBT Hóa học lớp 9
I. NGUYÊN TẮC SẮP XẾP CÁC NGUYÊN TỐ TRONG BẢNG TUẦN HOÀN
Sắp xếp các nguyên tố theo chiều tăng dần của điện tích hạt nhân nguyên tử.
II. CẤU TẠO BẢNG TUẦN HOÀN
1. Ô nguyên tố
Ô nguyên tố cho biết: Số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố, nguyên tử khối của nguyên tố đó.
Thí dụ:
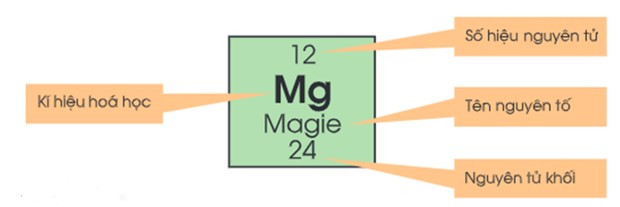
Số hiệu nguyên tử có số trị bằng số đơn vị điện tích hạt nhân và bằng số electron trong nguyên tử.
2. Chu kì: là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron và được xếp theo chiều điện tích hạt nhân tăng dần.
- Số thứ tự chu kì bằng số lớp electron. Thí dụ:
- Chu kì 2: Gồm 8 nguyên tố từ Li đến Ne, có 2 lớp electron trong nguyên tử. Điện tích hạt nhân tăng dần từ Li là 2+ đến Ne là 10+
- Chu kì 3: Gồm 8 nguyên tố từ Na đến Ar, có 3 lớp electron trong nguyên tử. Điện tích hạt nhân tăng dần từ Na là 11+ đến Ar là 18+
3. Nhóm
- Nhóm gồm các nguyên tố mà nguyên tử của chúng có số electron lớp ngoài cùng bằng nhau, do đó có tính chất tương tự nhau.
- Số thứ tự của các nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử trong nhóm đó. Thí dụ:
Nhóm IA: - Gồm các nguyên tố kim loại hoạt động mạnh. Nguyên tử của chúng đều có 1 electron ở lớp ngoài cùng.
- Điện tích hạt nhân tăng từ Li (3+) đến Fr (87+)
Nhóm VIIA: - Gồm các nguyên tố phi kim hoạt động mạnh. Nguyên tử của chúng đều có 7 electron ở lớp ngoài cùng.
- Điện tích hạt nhân tăng từ F (9+) đến At (85+)
III. SỰ BIỂN ĐỔI TÍNH CHẤT CỦA CÁC NGUYÊN TỐ TRONG BẢNG TUẦN HOÀN
1. Trong một chu kì
Số e lớp ngoài cùng của nguyên tử tăng dần từ 1 đến 8 electron.
Tính kim loại của các nguyên tố giảm dần, đồng thời tính phi kim của các nguyên tố tăng dần.
Thí dụ:
*) Chu kì 2 gồm 8 nguyên tố:
- Số e lớp ngoài cùng của nguyên tử các nguyên tố tăng dần từ 1 đến 8
- Tính kim loại giảm dần, đồng thời tính phi kim tăng dần. Đầu chu kì là kim loại mạnh cuối chu kì là phi kim mạnh.
*) Chu kì 3 gồm 8 nguyên tố:
- Số e lớp ngoài cùng của nguyên tử các nguyên tố tăng dần từ 1 đến 8
- Tính kim loại giảm dần, đồng thời tính phi kim tăng dần. Đầu chu kì là kim loại mạnh cuối chu kì là phi kim mạnh.
2. Trong một nhóm
Trong một nhóm, khi đi từ trên xuống dưới theo chiều tăng của điện tích hạt nhân:
Số lớp electron trong nguyên tử tăng dần, tính kim loại của các nguyên tố tăng dần, đồng thời tính phi kim của các nguyên tố giảm dần.
Thí dụ:
*) Nhóm IA gồm 6 nguyên tố từ Li đến Fr
- Số lớp electron tăng dần từ 2 đến 7. Số electron lớp ngoài cùng của nguyên tử đều bằng 1.
- Tính kim loại của các nguyên tố tăng dần. Đầu nhóm là kim loại hoạt động mạnh cuối nhóm là kim loại hoạt động rất mạnh
*) Nhóm VIIA gồm 5 nguyên tố từ F đến At
- Số lớp electron tăng dần từ 2 đến 6. Số electron lớp ngoài cùng của nguyên tử đều bằng 7.
- Tính phi kim của các nguyên tố giảm dần. Đầu nhóm là phi kim hoạt động mạnh cuối nhóm là phi kim hoạt động hóa học yếu hơn.
IV. Ý NGHĨA CỦA BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Biết vị trí của nguyên tố ta có thể suy đoán cấu tạo nguyên tử và tính chất của nguyên tố.
Thí dụ: Nguyên tố A có số hiệu nguyên tử là 17, chu kì 3, nhóm VIIA. Hãy cho biết cấu tạo nguyên tử, tính chất của nguyên tố A và so sánh với các nguyên tố lân cận.
Trả lời: Nguyên tố A có số hiệu nguyên tử là 17, suy ra diện tích hạt nhân của nguyên tử A là 17+, nguyên tử A có 17 electron.
- A ở chu kì 3, suy ra nguyên tử A có 3 lớp electron; nhóm VIIA suy ra lớp ngoài cùng có 7e.
Vì ở gần cuối chu kì 3 nên A là một phi kim mạnh, tính phi kim của A yếu hơn của nguyên tố phía trên nó trong cùng nhóm (là F có số hiệu nguyên tử là 9), mạnh hơn của nguyên tố trước nó trong cùng chu kì (là S có số hiệu là 16) và mạnh hơn của nguyên tố đứng dưới nó trong cùng nhóm (là Br có số hiệu nguyên tử là 35)
Nhận xét: Biết vị trí của nguyên tố trong bảng tuần hoàn có thể suy đoán cấu tạo nguyên tử và tính chất cơ bản của nguyên tố, so sánh tính kim loại hay phi kim của nguyên tố này với những nguyên tố lân cận.
2. Biết cấu tạo nguyên tử của nguyên tố có thể suy đoán vị trí và tính chất nguyên tố đó.
Thí dụ: Nguyên tố X có điện tích hạt nhân là 16+, 3 lớp electron, lớp ngoài cùng có 6 electron.
Hãy cho biết vị trí của X trong bảng tuần hoàn và tính chất cơ bản của nó.
Trả lời:
- Vì nguyên tử X có điện tích hạt nhân là 16+, 3 lớp electron và lớp ngoài cùng có 6 electron, suy ra nguyên tố X ở ô 16, chu kì 3, nhóm VIA.
- Nguyên tố X là phi kim vì X đứng gần đầu nhóm VIA, gần cuối chu kì 3.
Nhận xét: Biết cấu tạo nguyên tử của nguyên tố có thể suy đoán vị trí nguyên tố trong bảng tuần hoàn và tính chất hóa học cơ bản của nó
Xem thêm lời giải vở bài tập Hóa học lớp 9 hay, chi tiết khác:
Bài 1 trang 94 VBT Hóa 9: Dựa vào bảng tuần hoàn, hãy cho biết cấu tạo nguyên tử...
Bài 2 trang 94 VBT Hóa 9: Biết X có cấu tạo nguyên tử như sau...
Bài 3 trang 94 VBT Hóa 9: Các nguyên tố trong nhóm I đều là những kim loại mạnh...
Bài 4 trang 94 VBT Hóa 9: Các nguyên tố nhóm VII đều là những phi kim mạnh...
Bài 5 trang 94 VBT Hóa 9: Hãy cho biết cách sắp xếp nào sau đây đúng theo chiều...
Bài 6 trang 94 VBT Hóa 9: Hãy sắp xếp các nguyên tố sau theo chiều tính phi kim...
Bài 7* trang 95 VBT Hóa 9: Hãy xác định công thức của hợp chất khí A...
Bài 1 trang 95 VBT Hóa 9: Hãy viết tên, kí hiệu các nguyên tố nhóm I...
Bài 2 trang 95 VBT Hóa 9: Viết tên, kí hiệu các nguyên tố chu kì 2, 3...
Bài 3 trang 95 VBT Hóa 9: Viết công thức oxit cao nhất của các nguyên tố R...
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 9 (hay nhất) | Để học tốt Ngữ văn 9 (sách mới)
- Soạn văn 9 (ngắn nhất)
- Văn mẫu 9 (sách mới) | Để học tốt Ngữ văn 9 Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 9 (sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 9 (sách mới) | Giải bài tập Toán 9 Tập 1, Tập 2
- Giải sbt Toán 9
- Lý thuyết Toán 9
- Các dạng bài tập Toán lớp 9
- Giáo án Toán lớp 9 mới nhất
- Bài tập Toán lớp 9 mới nhất
- Chuyên đề Toán lớp 9 mới nhất
- Giải sgk Tiếng Anh 9 (thí điểm)
- Giải sgk Tiếng Anh 9 (sách mới) | Để học tốt Tiếng Anh 9
- Giải sbt Tiếng Anh 9
- Giải sbt Tiếng Anh 9 (thí điểm)
- Giải sgk Sinh học 9 (sách mới) | Giải bài tập Sinh học 9
- Giải vở bài tập Sinh học 9
- Lý thuyết Sinh học 9
- Giải sbt Sinh học 9
- Giải sgk Vật Lí 9 (sách mới) | Giải bài tập Vật lí 9
- Giải sbt Vật Lí 9
- Lý thuyết Vật Lí 9
- Các dạng bài tập Vật lí lớp 9
- Giải vở bài tập Vật lí 9
- Giải sgk Địa Lí 9 (sách mới) | Giải bài tập Địa lí 9
- Lý thuyết Địa Lí 9
- Giải Tập bản đồ Địa Lí 9
- Giải sgk Tin học 9 (sách mới) | Giải bài tập Tin học 9
- Lý thuyết Tin học 9
- Lý thuyết Giáo dục công dân 9
- Giải vở bài tập Lịch sử 9
- Giải Tập bản đồ Lịch sử 9
- Lý thuyết Lịch sử 9
- Lý thuyết Công nghệ 9
