Trắc nghiệm Dãy hoạt động hóa học của kim loại (có đáp án)
Trắc nghiệm Hóa học 9 Bài 17: Dãy hoạt động hóa học của kim loại
-
402 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
22/07/2024Dãy kim loại được sắp xếp theo chiều hoạt động hóa học giảm dần là
 Xem đáp án
Xem đáp án
Đáp án A
Dãy hoạt động hóa học của một số kim loại:
K, Na, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au.
→ Dãy kim loại được sắp xếp theo chiều hoạt động hóa học giảm dần là:
Na, Mg, Zn.
Câu 2:
23/07/2024Dãy kim loại tác dụng được với dung dịch Cu(NO3)2 tạo thành Cu kim loại là
 Xem đáp án
Xem đáp án
Đáp án A
Các kim loại tác dụng được với Cu(NO3)2 tạo thành Cu kim loại phải đứng trước Cu trong dãy hoạt động hóa học của kim loại và các kim loại đó phải không tác dụng với nước.
Phương trình hóa học minh họa:
2Al + 3Cu(NO3)2 → 2Al(NO3)3 + 3Cu
Zn + Cu(NO3)2 → Zn(NO3)2 + Cu
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Câu 3:
23/07/2024Dãy hoạt động hóa học của kim loại không cho biết
 Xem đáp án
Xem đáp án
Đáp án B
Dãy hoạt động hóa học của kim loại cho biết
- Mức độ hoạt động hóa học của các kim loại giảm dần từ trái qua phải.
- Kim loại đứng trước Mg phản ứng với nước ở điều kiện thường tạo thành kiềm và giải phóng khí H2.
- Kim loại đứng trước H phản ứng với một số dung dịch axit (HCl, H2SO4 loãng, …) giải phóng khí H2.
- Kim loại đứng trước (trừ Na, K,…) đẩy kim loại đứng sau ra khỏi dung dịch muối.
Câu 4:
07/07/2024Từ Cu và hoá chất nào dưới đây để thu được CuSO4 ?
 Xem đáp án
Xem đáp án
Đáp án D
Cu không phản ứng với MgSO4; Al2(SO4)3, H2SO4 loãng.
Cu + 2H2SO4 đặc t°→CuSO4 + SO2 + 2H2O
Câu 5:
23/07/2024Có một mẫu dung dịch MgSO4 bị lẫn tạp chất là ZnSO4, có thể làm sạch mẫu dung dịch này bằng kim loại
 Xem đáp án
Xem đáp án
Đáp án B
Cho một lượng dư Mg phản ứng với mẫu dung dịch. Đến khi phản ứng xảy ra hoàn toàn, lọc bỏ kim loại ta được dung dịch MgSO4 tinh khiết.
Phương trình hóa học:
Mg + ZnSO4 t°→MgSO4 + Zn
Câu 6:
23/07/2024Nếu hoà tan hết cùng một khối lượng Al và Zn bởi dung dịch HCl thì
 Xem đáp án
Xem đáp án
Đáp án A
Giả sử mAl = mZn = m gam
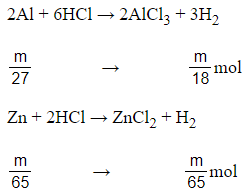
Có m18 > m65. Vậy nếu hoà tan hết cùng một khối lượng Al và Zn bởi dung dịch HCl thì Al giải phóng hiđro nhiều hơn Zn .
Câu 7:
22/07/2024Ngâm một lá kẽm (Zn) trong 20 gam dung dịch muối CuSO4 10% cho đến khi kẽm không tan được nữa thì dừng phản ứng. Khối lượng lá kẽm đã tham gia phản ứng là
 Xem đáp án
Xem đáp án
Đáp án B
nCuSO4=20160.10100=0,0125 mol
Phương trình hóa học:
Zn + CuSO4 → ZnSO4 + Cu
0,0125 ← 0,0125 (mol)
mZn pư = 0,0125.65= 0,8125 gam
Câu 8:
23/07/2024Ngâm lá sắt (Fe) có khối lượng 56 gam vào dung dịch AgNO3, sau một thời gian lấy lá sắt ra rửa nhẹ cân được 57,6 gam . Vậy khối lượng bạc (Ag) sinh ra là
 Xem đáp án
Xem đáp án
Đáp án D
Đặt số mol Fe phản ứng là a
Phương trình hóa học:
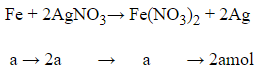
Bảo toàn khối lượng:
mFe + m Ag sinh ra – mFe(phản ứng) = 57,6
→56 + 108.2a − 56a = 57,6
→a = 0,01 mol
→ nAg = 2.a = 0,02 mol
→ mAg sinh ra = 0,02.108 = 2,16 gam
Câu 9:
18/07/2024Cho 4,8 gam kim loại M có hóa trị II vào dung dịch HCl dư, thấy thoát ra 4,48 lít khí hiđro (ở đktc). Vậy kim loại M là
 Xem đáp án
Xem đáp án
Đáp án B
nH2=4,4822,4=0,2mol
Phương trình hóa học:
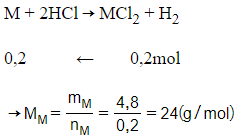
→M là Magie (Mg)
Câu 10:
21/07/2024Cho 1 viên natri (Na) vào dung dịch CuSO4, hiện tượng xảy ra là
 Xem đáp án
Xem đáp án
Đáp án C
Natri tan dần, có khí không màu thoát ra, xuất hiện kết tủa màu xanh.
Phương trình hóa học:
2Na + 2H2O →2NaOH + H2
![]()
Câu 11:
22/07/2024Phản ứng hóa học không chính xác là
 Xem đáp án
Xem đáp án
Đáp án C
Phản ứng C sai vì Cu là kim loại đứng sau Mg trong dãy hoạt động hóa học của kim loại, nên Cu không thể đẩy được Mg ra khỏi muối MgSO4.
Câu 12:
21/07/2024Kim loại được dùng để phân biệt 3 dung dịch: NaCl, CuCl2, Na2SO4 là
 Xem đáp án
Xem đáp án
Đáp án B
- Trích mẫu thử, cho vào mỗi mẫu thử một ít Ba.
- Hiện tượng:
+ Ba tan dần, có khí thoát ra → dung dịch là NaCl
Ba + 2H2O → Ba(OH)2 + H2↑
+ Có khí thoát ra, đồng thời xuất hiện kết tủa xanh → dung dịch là CuCl2.
Ba + 2H2O → Ba(OH)2 + H2↑
![]()
+ Có khí thoát ra, đồng thời xuất hiện kết tủa trắng → dung dịch là Na2SO4.
Ba + 2H2O → Ba(OH)2 + H2↑
![]()
Ngoài ra, có thể quan sát màu dung dịch để nhận ra CuCl2 (dd màu xanh); hai dung dịch còn lại không màu. Sau đó tiếp tục dùng kim loại Ba để nhận ra 2 dung dịch không màu này.
Câu 13:
23/07/2024Cho 27,6 gam hỗn hợp 2 kim loại Mg và Ag tác dụng với dung dịch HCl vừa đủ, sau phản ứng thấy thoát ra 5,6 lít khí (ở đktc). Thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu lần lượt là
 Xem đáp án
Xem đáp án
Đáp án A
Cho Mg và Ag tác dụng với HCl chỉ có Mg phản ứng.
nH2=5,622,4=0,25mol
Mg + 2HCl→MgCl2 + H2
0,25 ← 0,25 mol
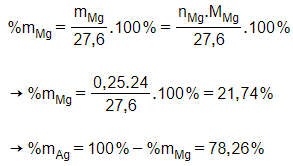
Câu 14:
19/07/2024Hiện tượng gì xảy ra khi cho 1 thanh đồng vào dung dịch H2SO4 loãng?
 Xem đáp án
Xem đáp án
Đáp án C
Do đồng đứng sau H trong dãy hoạt động hóa học của kim loại nên không tác dụng được với dung dịch H2SO4 loãng.
Câu 15:
12/07/2024Cho 10,5 gam hỗn hợp 2 kim loại Cu, Zn vào dung dịch H2SO4 loãng, dư người ta thu được 2,24 lít khí (ở đktc). Khối lượng chất rắn còn lại sau khi phản ứng kết thúc là
 Xem đáp án
Xem đáp án
Đáp án B
Hỗn hợp Zn và Cu tác dụng với dung dịch H2SO4, chỉ có Zn phản ứng.
Phương trình hóa học:
Zn + H2SO4(loãng)→ZnSO4 + H2
Theo phương trình:
⇒nZn=nH2=0,1mol
Khối lượng kẽm (Zn) phản ứng là:
mZn = nZn . MZn = 0,1.65 = 6,5gam
Khối lượng chất rắn (Cu) còn lại là:
mCu = m(Hỗn hợp) – mZn(phản ứng)
mCu = 10,5 – 6,5 = 4 gam
