Giải SGK KHTN 8 CTST Bài 4: Định luật bảo toàn khối lượng và phương trình hoá học
Giải SGK KHTN 8 CTST Bài 4: Định luật bảo toàn khối lượng và phương trình hoá học
-
62 lượt thi
-
14 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
15/07/2024Khi hai chất phản ứng với nhau sẽ tạo thành chất mới do có sự hình thành liên kết mới giữa các nguyên tử trong phân tử. Sự biến đổi hoá học có làm khối lượng các chất bảo toàn không? Làm thế nào để biểu diễn phản ứng hoá học ngắn gọn và thuận tiện?
 Xem đáp án
Xem đáp án
- Khi một phản ứng hoá học xảy ra, tổng khối lượng các chất trước và sau phản ứng không thay đổi.
- Để thuận tiện cho việc trình bày ngắn gọn một phản ứng hoá học, người ta sử dụng các công thức hoá học biểu diễn cho các chất, gọi là phương trình hoá học.
Câu 2:
23/07/2024Nhận xét màu sắc của dung dịch BaCl2 và dung dịch Na2SO4 ban đầu trong 2 cốc thuỷ tinh.
 Xem đáp án
Xem đáp án
Ban đầu cả dung dịch đều trong suốt, không có màu.
Câu 3:
22/07/2024Nêu hiện tượng sau khi rót cốc (1) vào cốc (2) và chỉ ra dấu hiệu có phản ứng hoá học xảy ra.
 Xem đáp án
Xem đáp án
Sau khi rót cốc (1) vào cốc (2):
+ Hiện tượng: có kết tủa trắng xuất hiện.
+ Dấu hiệu có phản ứng hoá học xảy ra: có kết tủa trắng xuất hiện.
Câu 4:
13/07/2024Em có nhận xét gì về tổng khối lượng của 2 cốc trước và sau phản ứng.
 Xem đáp án
Xem đáp án
Câu 5:
16/07/2024Giải thích vì sao trong một phản ứng hoá học, tổng khối lượng các chất được bảo toàn.
 Xem đáp án
Xem đáp án
Trong phản ứng hoá học diễn ra sự thay đổi liên kết giữa các nguyên tử còn số nguyên tử mỗi nguyên tố vẫn giữ nguyên và khối lượng của các nguyên tử không đổi, vì vậy tổng khối lượng các chất được bảo toàn.
Câu 6:
13/07/2024Phương trình hoá học biểu diễn gì? Gồm công thức hoá học của những chất nào?
 Xem đáp án
Xem đáp án
Phương trình hoá học biểu diễn phản ứng hoá học bằng công thức hoá học của chất tham gia và chất sản phẩm.
Câu 7:
14/07/2024Viết sơ đồ phản ứng của phản ứng giữa khí hydrogen và khí oxygen tạo ra nước.
 Xem đáp án
Xem đáp án
Sơ đồ phản ứng dạng chữ:
Khí hydrogen + khí oxygen → nước.
Câu 8:
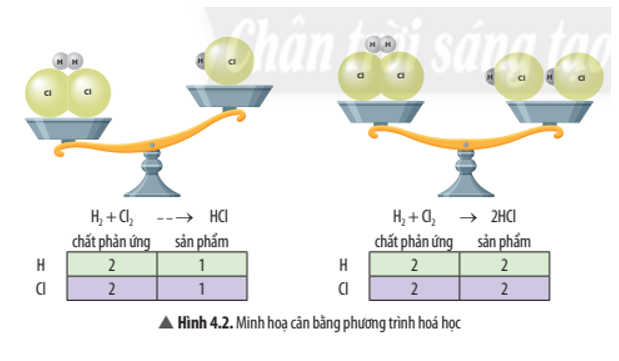
13/07/2024Quan sát Hình 4.2, hãy cho biết phương trình nào đã được cân bằng. Vì sao?
 Xem đáp án
Xem đáp án
Phương trình được cân bằng là: H2 + Cl2 → 2HCl
Do số nguyên tử của mỗi nguyên tố ở hai vế của phương trình là bằng nhau.
Câu 9:
13/07/2024Quan sát sơ đồ phản ứng (*), hãy nhận xét số nguyên tử của nguyên tố P và O ở vế trái và vế phải. Số nguyên tử của nguyên tố nào lớn hơn?
 Xem đáp án
Xem đáp án
Sơ đồ phản ứng (*): P + O2 P2O5.
- Ở vế trái: P + O2
+ Có 1 nguyên tử P và 2 nguyên tử O.
+ Số nguyên tử O lớn hơn.
- Ở vế phải: P2O5
+ Có 2 nguyên tử P và 5 nguyên tử O.
+ Số nguyên tử O lớn hơn.
Câu 10:
13/07/2024Để cân bằng, bắt đầu cân bằng từ nguyên tố nào trước?
 Xem đáp án
Xem đáp án
Để cân bằng, bắt đầu cân bằng từ nguyên tố O trước.
Câu 11:
13/07/2024Làm thế nào để cho số nguyên tử của nguyên tố O ở 2 vế bằng nhau?
 Xem đáp án
Xem đáp án
Ta làm chẵn số nguyên tử O vế phải bằng cách đặt hệ số 2 trước P2O5:
P + O2 2P2O5.
Để số nguyên tử O vế trái bằng với vế phải, ta thêm hệ số 5:
P + 5O2 2P2O5.
Câu 12:
13/07/2024Phương trình hoá học cho biết những thông tin gì?
 Xem đáp án
Xem đáp án
Phương trình hoá học cho biết tỉ lệ về số nguyên tử hoặc số phân tử giữa các chất trong phản ứng.
Câu 13:
20/07/2024Lập phương trình hoá học và cho biết tỉ lệ số nguyên tử và số phân tử của các chất trong mỗi sơ đồ phản ứng sau:
a) Na + O2 Na2O
b) Na2CO3 + Ba(OH)2 NaOH + BaCO3
c) Fe + O2 Fe3O4
 Xem đáp án
Xem đáp án
a) Bước 1: Viết sơ đồ phản ứng:
Na + O2 Na2O
Bước 2: Làm chẵn số nguyên tử O vế phải bằng cách đặt hệ số 2 trước Na2O.
Na + O2 2Na2O
Số nguyên tử Na vế trái và phải chưa bằng nhau, ta đặt hệ số 4 trước Na.
4Na + O2 2Na2O
Bước 3: Viết phương trình hoá học hoàn chỉnh:
4Na + O2 → 2Na2O
Tỉ lệ: 4 nguyên tử Na : 1 phân tử O2 : 2 phân tử Na2O.
Hay cứ 4 nguyên tử Na tác dụng với 1 phân tử O2 tạo ra 2 phân tử Na2O.
b) Bước 1: Viết sơ đồ phản ứng
Na2CO3 + Ba(OH)2 NaOH + BaCO3
Bước 2: Số nhóm (OH) ở vế phải và vế trái chưa bằng nhau, ta đặt hệ số 2 trước NaOH.
Na2CO3 + Ba(OH)2 2NaOH + BaCO3
Bước 3: Viết phương trình hoá học hoàn chỉnh:
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
Tỉ lệ: 1 phân tử Na2CO3 : 1 phân tử Ba(OH)2 : 2 phân tử NaOH : 1 phân tử BaCO3.
Hay cứ 1 phân tử Na2CO3 tác dụng với 1 phân tử Ba(OH)2 tạo ra 2 phân tử NaOH và 1 phân tử BaCO3.
c) Bước 1: Viết sơ đồ phản ứng:
Fe + O2 Fe3O4
Bước 2: Số nguyên tử O ở vế phải và vế trái chưa bằng nhau, ta thêm hệ số 2 vào O2:
Fe + 2O2 Fe3O4
Số nguyên tử Fe ở vế trái và vế phải chưa bằng nhau, ta thêm hệ số 3 vào Fe:
3Fe + 2O2 Fe3O4
Bước 3: Viết phương trình hoá học hoàn chỉnh:
3Fe + 2O2 → Fe3O4
Tỉ lệ: 3 nguyên tử Fe : 2 phân tử O2 : 1 phân tử Fe3O4.
Hay cứ 3 nguyên tử Fe tác dụng với 2 phân tử O2 được 1 phân tử Fe3O4.
Câu 14:
13/07/2024Kim loại nhôm (Al) với ưu điểm là nhẹ, dẻo, dẫn nhiệt tốt và dễ dàng phản ứng với oxygen (O2) tạo lớp màng oxide mỏng (Al2O3) bao phủ bên ngoài giúp cho kim loại nhôm được bảo vệ vững chắc trong không khí. Em hãy lập phương trình hoá học biểu diễn phản ứng hoá học giữa kim loại nhôm với khí oxygen và giải thích tại sao người ta thường dùng nhôm để chế tạo đồ dùng và dụng cụ nhà bếp.
 Xem đáp án
Xem đáp án
Bước 1: Viết sơ đồ phản ứng:
Al + O2 Al2O3
Bước 2: Ta làm chẵn số nguyên tử O vế phải bằng cách thêm 2 vào Al2O3:
Al + O2 2Al2O3
Để số nguyên tử O vế trái bằng vế phải, ta thêm hệ số 3 vào O2:
Al + 3O2 2Al2O3
Số nguyên tử Al vế trái chưa bằng vế phải, ta thêm hệ số 4 vào Al:
4Al + 3O2 2Al2O3
Bước 3: Viết phương trình hoá học hoàn chỉnh:
4Al + 3O2 → 2Al2O3
Người ta thường dùng nhôm để chế tạo đồ dùng và dụng cụ nhà bếp do nhôm bền, nhẹ, dẫn nhiệt tốt.
