Giải SGK Khoa học tự nhiên 8 Cánh diều Bài 3: Định luật bảo toàn khối lượng. Phương trình hoá học có đáp án
Giải SGK Khoa học tự nhiên 8 Cánh diều Bài 3: Định luật bảo toàn khối lượng. Phương trình hoá học có đáp án
-
58 lượt thi
-
15 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
19/07/2024Quan sát hình 3.1:
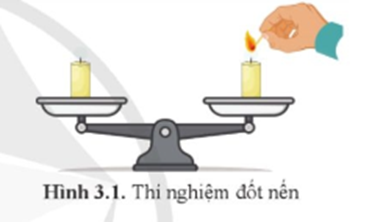
Đặt hai cây nến trên đĩa cân, cân ở vị trí thăng bằng. Nếu đốt một cây nến, sau một thời gian, cân có còn thăng bằng không? Giải thích.
 Xem đáp án
Xem đáp án
Đặt hai cây nến trên đĩa cân, cân ở vị trí thăng bằng. Nếu đốt một cây nến, sau một thời gian, cân không còn thăng bằng. Do cây nến bị đốt đã ngắn lại và không còn nặng như ban đầu.
Câu 2:
20/07/2024Chuẩn bị:
● Dụng cụ: Cân điện tử, bình tam giác (loại 100 ml), ống hút nhỏ giọt, ống đong.
● Hoá chất: Dung dịch sodium sulfate (Na2SO4), dung dịch barium chloride (BaCl2).
Tiến hành:
Bước 1: Đặt bình tam giác trong đó có chứa 10 ml dung dịch BaCl2 trên đĩa cân điện tử và lấy đầy dung dịch Na2SO4 vào ống hút nhỏ giọt có bóp cao su đậy lên miệng bình (hình 3.2a). Ghi chỉ số khối lượng hiện trên mặt cân (kí hiệu là mA).
Bước 2: Bóp nút cao su cho dung dịch Na2SO4 chảy xuống bình (hình 3.2b). Quan sát dấu hiệu của phản ứng xảy ra. Ghi chỉ số khối lượng hiện trên mặt cân (kí hiệu là mB).
● Mô tả hiện tượng thí nghiệm, cho biết khối lượng mA và mB.
● So sánh mA và mB, từ đó rút ra nhận xét về tổng khối lượng của các chất trước và tổng khối lượng của các chất sau phản ứng.

 Xem đáp án
Xem đáp án
- Học sinh tiến hành thí nghiệm, ghi giá trị mA và mB. Hiện tượng thí nghiệm: Xuất hiện kết tủa trắng.
- Ta có mA = mB.
Nhận xét: tổng khối lượng của các chất trước phản ứng bằng tổng khối lượng của các chất sau phản ứng.
Câu 3:
19/07/2024Chuẩn bị:
● Dụng cụ: Cân điện tử, bình tam giác (loại 100 ml), ống đong.
● Hoá chất: Bột sodium hydrogencarbonate (NaHCO3), dung dịch giấm ăn (CH3COOH).
Tiến hành:
Bước 1: Đặt bình tam giác có chứa 10 ml giấm ăn và một mẩu giấy có chứa một thì cafe bột NaHCO3 trên đĩa cân điện tử. Ghi chỉ số khối lượng hiện trên mặt cân (kí hiệu là mA).
Bước 2: Đổ bột NaHCO3 vào bình tam giác, đặt lại mẩu giấy lên đĩa cân, ghi chỉ số khối lượng hiện trên mặt cân (kí hiệu là mB).
● Mô tả hiện tượng thí nghiệm, cho biết khối lượng mA và mB.
● So sánh mA và mB. Giải thích.
 Xem đáp án
Xem đáp án
- Hiện tượng thí nghiệm: có khí thoát ra. Học sinh làm thí nghiệm và ghi lại giá trị mA, mB.
- So sánh: mA > mB. Giải thích:
Phản ứng hoá học xảy ra ở thí nghiệm 2 có thể được biểu diễn bằng sơ đồ ở dạng chữ như sau:
Acetic acid + Sodium hydrogencarbonate → Sodium acetate + Carbon dioxide + Nước
Vậy mA > mB do sau phản ứng có khí carbon dioxide thoát ra khỏi bình.
Câu 4:
22/07/2024Tính khối lượng FeS tạo thành trong phản ứng của Fe và S, biết khối lượng của Fe và S đã tham gia phản ứng lần lượt là 7 gam và 4 gam.
 Xem đáp án
Xem đáp án
Áp dụng định luật bảo toàn khối lượng: Trong một phản ứng hoá học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng cùa các chất tham gia phản ứng.
Vậy khối lượng FeS tạo thành = khối lượng Fe phản ứng + khối lượng S phản ứng = 7 + 4 = 11 gam.
Câu 5:
17/07/2024Trở lại thí nghiệm trong hoạt động mở đầu: Cân có còn giữ ở vị trí thăng bằng không? Giải thích.
 Xem đáp án
Xem đáp án
Cân không còn giữ ở trạng thái cân bằng. Do nến cháy sinh ra khí carbon dioxide và hơi nước làm cây nến ngắn dần so với ban đầu.
Câu 6:
17/07/2024Giải quyết tình huống:
a) Khi đốt cháy hoàn toàn một mẩu gỗ, ta thu được tro có khối lượng nhẹ hơn mẩu gỗ ban đầu. Theo em, sự thay đổi khối lượng này có mâu thuẫn với định luật bảo toàn khối lượng không?
 Xem đáp án
Xem đáp án
a) Sự thay đổi khối lượng này không có mâu thuẫn với định luật bảo toàn khối lượng.
Do sản phẩm thu được khi đốt cháy mẩu gỗ ngoài tro còn có carbon dioxide, hơi nước.
Câu 7:
13/07/2024b) Đề xuất các bước tiến hành thí nghiệm để kiểm chứng định luật bảo toàn khối lượng trong tình huống trên.
 Xem đáp án
Xem đáp án
b) Đề xuất các bước tiến hành thí nghiệm để kiểm chứng:
Chuẩn bị:
- Dụng cụ: Cân điện tử, bật lửa.
- Hoá chất: Bình chứa khí oxygen, 1 que đóm có độ dài ngắn hơn chiều cao của bình chứa khí oxygen.
Tiến hành:
- Bước 1: Đặt bình tam giác có chứa khí oxygen và que đóm trên đĩa cân điện tử. Ghi chỉ số khối lượng hiện lên mặt cân (kí hiệu là mA).
- Bước 2: Đốt một đầu que đóm và cho nhanh vào bình chứa khí oxygen, sau đó đậy nút lại. Sau khi que đóm cháy hết hoặc dừng cháy, ghi chỉ số khối lượng hiện trên mặt cân (kí hiệu là mB).
- Bước 3: So sánh mA và mB, rút ra kết luận.
Câu 8:
23/07/2024 Xem đáp án
Xem đáp án
M.V. Lô – mô – nô − xốp sinh năm 1711 trong một gia đình sống bằng nghề chài lưới. Mãi tới năm 19 tuổi nhân một chuyến theo đoàn tàu buôn đến Mát – xcơ – va, Lô – mô – nô − xốp mới xin được vào học một trường giòng gọi là Viện Hàn lâm Xla − vơ Hy Lạp. Năm 1735 ông tốt nghiệp và được Viện gửi đến Pê – téc – bua tiếp tục học tập. Ngay năm sau 1736 ông lại được cử sang Đức nghiên cứu nghề luyện kim và khai mỏ. Năm 1741 ông trở về nước Nga với tư cách là một nhà tự nhiên học, nghiên cứu những vấn đề quan trọng nhất của vật lý và hoá học. Một số thành tựu tiêu biểu của Lô – mô – nô – xốp như xây dựng thành công thuyết hạt về cấu tạo các chất, phương pháp điều chế chất màu vô cơ và thuỷ tinh màu từ các nguyên liệu trong nước. Ngoài ra, ông còn sáng tạo ra “ngôn ngữ hoá học” Nga qua nghiên cứu phân tích các thành phần của các muối và các chất khoáng….
La – voa – đi – ê là nhà bác học Pháp, ông sinh ra ở Paris vào năm 1743 trong một gia đình trung lưu. Từ năm 1754 đến 1761, La – voa – đi – ê đã nghiên cứu về nhân văn và khoa học tại Đại học Ma – za – rin. Kết quả là sau này, ông được nhận vào Hội luật sư. Tuy nhiên, ông lại nghiêng về nghiên cứu khoa học, với những thành tựu đạt được ông đã được nhận vào Học viện Khoa học Paris vào năm 1768, ở tuổi 25 năm. Trong suốt quá trình nghiên cứu của mình La – voa – đi – ê đã có những phát kiến để đời như phát hiện vai trò của oxygen trong quá trình cháy và hô hấp, đồng thời xác định rằng nước là một hợp chất của hydrogen và oxygen. Ngoài ra ông còn là người đặt nền móng giúp chuyển đổi hóa học từ một ngành khoa học định tính thành một ngành khoa học định lượng…
Đặc biệt, hai nhà bác học Lô – mô – nô – xốp và La – voa – đi – ê đã tiến hành độc lập với nhau những thí nghiệm được cân đo chính xác, từ đó phát hiện ra định luật bảo toàn khối lượng.
Câu 9:
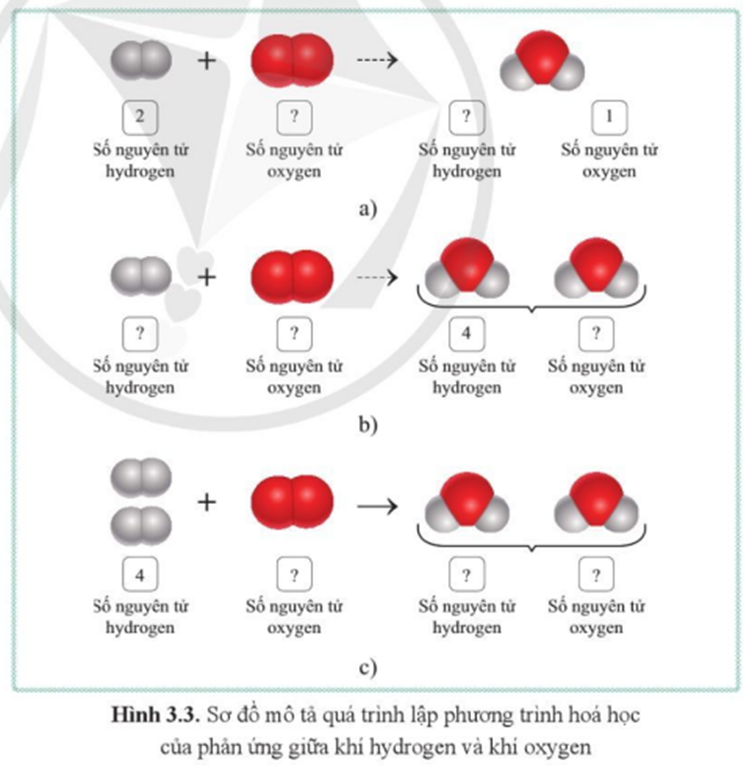
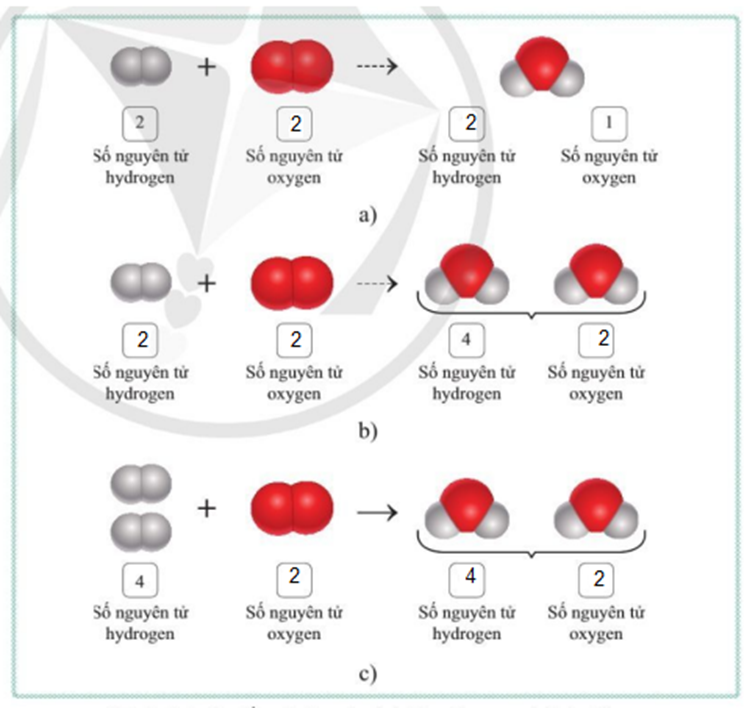
17/07/2024Dựa vào kiến thức đã học, cho biết tổng số nguyên tử của mỗi nguyên tố tham gia và tạo thành sản phẩm trong ví dụ bên cần phải tuân theo nguyên tắc như thế nào?
 Xem đáp án
Xem đáp án
Trong phản ứng hoá học, tổng số nguyên tử của mỗi nguyên tố trong các chất tham gia phản ứng luôn bằng tổng số nguyên tử của nguyên tố đó trong các chất sản phẩm.
Câu 11:
21/07/2024Lập phương trình hoá học của phản ứng magnesium (Mg) tác dụng với oxygen (O2) tạo thành magnesium oxide (MgO).
 Xem đáp án
Xem đáp án
Bước 1: Viết sơ đồ của phản ứng: Mg + O2 − − − → MgO.
Bước 2: So sánh số nguyên tử của mỗi nguyên tố có trong phân tử các chất tham gia phản ứng và các chất sản phẩm:
Mg + O2 − − − → MgO
Số nguyên tử: 1 2 1 1
Bước 3 + 4: Cân bằng số nguyên tử của mỗi nguyên tố, viết phương trình hoá học:
2Mg + O2 → 2MgO.
Câu 12:
23/07/2024Lập phương trình hoá học của phản ứng khi cho dung dịch sodium carbonate (Na2CO3) tác dụng với dung dịch calcium hydroxide (Ca(OH)2) tạo thành calcium carbonate (CaCO3) không tan (kết tủa) và sodium hydroxide (NaOH).
 Xem đáp án
Xem đáp án
Bước 1: Viết sơ đồ phản ứng:
Na2CO3 + Ca(OH)2 − − − → CaCO3↓ + NaOH
Bước 2: So sánh số nguyên tử/ nhóm nguyên tử của mỗi nguyên tố/ chất trước và sau phản ứng.
Na2CO3 + Ca(OH)2 − − − → CaCO3↓ + NaOH
Số nguyên tử/ nhóm nguyên tử: 2 1 1 2 1 1 1 1
Bước 3: Cân bằng số nguyên tử/ nhóm nguyên tử:
Na2CO3 + Ca(OH)2 − − − → CaCO3↓ + 2NaOH
Số nguyên tử/ nhóm nguyên tử: 2 1 1 2 1 1 2 2
Bước 4: Kiểm tra và viết phương trình hoá học:
Na2CO3 + Ca(OH)2 → CaCO3↓ + 2NaOH
Câu 13:
22/07/2024Xét phương trình hoá học của phản ứng sau: 4Al + 3O2 → 2Al2O3
a) Cho biết số nguyên tử, số phân tử của các chất tham gia phản ứng và các chất sản phẩm.
 Xem đáp án
Xem đáp án
a) Số nguyên tử Al : Số phân tử O2 : Số phân tử Al2O3 = 4 : 3 : 2.
Câu 14:
13/07/2024b) Cho biết tỉ lệ hệ số của các chất trong phương trình hoá học.
 Xem đáp án
Xem đáp án
b) Tỉ lệ hệ số của các chất trong phương trình hoá học = 4 : 3 : 2.
Câu 15:
17/07/2024Trong dạ dày người có một lượng hydrochloric acid (HCl) tương đối ổn định, có tác dụng trong tiêu hoá thức ăn. Nếu lượng acid này tăng lên quá mức cần thiết có thể gây ra đau dạ dày. Thuốc muối có thành phần chính là sodium hydrogencarbonate (NaHCO3) giúp giảm bớt lượng acid dư thừa trong dạ dày theo phương trình hoá học:
NaHCO3 + HCl → NaCl + H2O + CO2↑ *
Tìm hiểu và cho biết các thực phẩm có thể gây tăng lượng acid có trong dạ dày.
 Xem đáp án
Xem đáp án
Một số thực phẩm có thể gây tăng lượng acid có trong dạ dày:
- Đồ ăn chua: Quả chua như chanh, quất … và đồ ăn lên men như dưa muối, cà muối … là những thực phẩm có lượng acid cao, khi xuống đến dạ dày có thể làm tăng lượng acid có trong dạ dày.
- Nước uống có gas: Các loại nước uống có gas phổ biến như Pepsi và Coca – cola có giá trị pH khoảng 2,5 – 3,5, do đó chúng cũng làm tăng lượng acid có trong dạ dày.
- Đồ ăn giàu chất béo: Chất béo tồn tại lâu hơn trong dạ dày và khiến tăng tiết acid dạ dày liên tục trong suốt quá trình co bóp để tiêu hóa.
- Đồ ăn cay nóng: Đồ ăn cay nóng cũng được liệt vào danh sách những thực phẩm người bị đau dạ dày không nên ăn. Gia vị cay nóng có thể khiến cho dạ dày bị tổn thương, làm tình trạng dư thừa acid dạ dày càng trở nên trầm trọng.
Ngoài ra, bia, rượu và các đồ uống có cồn cũng góp phần làm tăng lượng acid có trong dạ dày.