Giải SBT Hóa học 11 CD Bài 6: Sulfur và sulfur dioxide
Giải SBT Hóa học 11 CD Bài 6: Sulfur và sulfur dioxide
-
116 lượt thi
-
16 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
22/07/2024Những phát biểu nào sau đây là đúng?
(a) Trong tự nhiên, sulfur tồn tại chủ yếu ở dạng muối sulfide và muối sulfate của một số kim loại.
(b) Là một phi kim khá hoạt động nên trong tự nhiên không tìm thấy sulfur đơn chất.
(c) Trứng gà ung có mùi thối đặc trưng một phần là do các hợp chất của sulfur có trong trứng phân huỷ gây ra.
(d) Nguyên tố sulfur có mặt trong một số loại thực vật, đặc biệt là các loại rau quả có mùi mạnh như hành tây, sầu riêng,…
(e) Thành phần chính của quặng pyrite là hợp chất của sulfur và chì (lead, Pb).
 Xem đáp án
Xem đáp án
Đáp án đúng là: (a), (c), (d).
Phát biểu (b) sai vì trong tự nhiên sulfur tồn tại cả dạng đơn chất và hợp chất.
Phát biểu (e) sai vì thành phần chính của quặng pyrite là FeS2.
Câu 2:
23/07/2024Phân tử sulfur, S8, có cấu tạo như Hình 6.
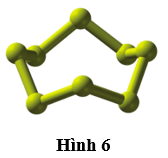
a) Giải thích vì sao phân tử này không phân cực.
 Xem đáp án
Xem đáp án
a) Các liên kết S−S trong S8 đều là liên kết cộng hóa trị không cực nên hợp chất S8 cũng là hợp chất không phân cực.
Câu 3:
08/07/2024b) Những phát biểu nào dưới đây là phù hợp với tính không phân cực của sulfur?
 Xem đáp án
Xem đáp án
Câu 4:
23/07/2024Thành phần chính của khí thiên nhiên là các hydrocarbon như methane (khoảng 80 − 85%), ethane, propane, butane cùng lượng nhỏ các khí carbon dioxide, hydrogen sulfide, nitrogen. Thành phần chính của than là carbon, ngoài ra còn có một số hợp chất của các nguyên tố H, S, O, N,…
Khi sử dụng khí thiên nhiên hoặc than làm nhiên liệu đều thải vào không khí các chất khí gây ô nhiễm. Giải thích.
Câu 5:
20/07/2024Những ý kiến nào sau đây về sulfur dioxide (SO2) là đúng?
(a) Có độc tính đối với con người.
(b) Phản ứng được với đá vôi.
(c) Khí này được tạo thành từ hoạt động của núi lửa trong tự nhiên, từ quá trình đốt cháy nhiên liệu hoá thạch của con người,…
(d) Là oxide lưỡng tính.
Câu 6:
22/07/2024Nối những đặc điểm của chất ở cột B với tên chất ở cột A cho phù hợp.
|
Cột A |
Cột B |
|
a) Sulfur
|
1. Là chất khí ở điều kiện thường. |
|
2. Ở điều kiện thường, phân tử có 8 nguyên tử. |
|
|
3. Dễ tan trong nước. |
|
|
b) Sulfur dioxide
|
4. Hòa tan trong dung môi phù hợp để làm thuốc trị bệnh ngoài da. |
|
5. Dùng để tẩy trắng vải, sợi. |
|
|
6. Có tính khử và tính oxi hóa. |
 Xem đáp án
Xem đáp án
Đáp án đúng là:
a ghép với 2, 4, 6;
b ghép với 1, 3, 5, 6.
Câu 7:
23/07/2024Trong phản ứng, SO2 có thể đóng vai trò là một oxide acid (acidic oxide). Hoàn thành các phương trình hoá học dưới đây để minh hoạ vai trò oxide acid của SO2.
a) Tan trong nước tạo thành acid yếu H2SO3.
 Xem đáp án
Xem đáp án
Các phương trình hoá học minh hoạ:
a) SO2 + H2O ⇌ H2SO3
Câu 8:
22/07/2024b) Phản ứng với dung dịch base tạo muối và nước.
 Xem đáp án
Xem đáp án
b) SO2 + 2NaOH ⟶ Na2SO3 + H2O
Câu 9:
19/07/2024c) Phản ứng với oxide base (basic oxide) tạo muối.
 Xem đáp án
Xem đáp án
c) SO2 + CaO ⟶ CaSO3
Câu 10:
19/07/2024Cho giá trị enthalpy tạo thành chuẩn của khí SO2 và khí SO3 lần lượt là −296,8 kJ mol−1 và −395,7 kJ mol−1.
Tính giá trị biến thiên enthalpy chuẩn của phản ứng sau:
SO2(g) + O2(g) → SO3(g)
Từ đó, hãy cho biết phản ứng trên có thuận lợi về mặt năng lượng không.
 Xem đáp án
Xem đáp án
Giá trị biến thiên enthalpy chuẩn của phản ứng là:
= (−395,7) − (−296,8) = −98,9 (kJ)
Giá trị biến thiên enthalpy chuẩn của phản ứng có giá trị âm, tức phản ứng toả nhiệt nên thuận lợi về mặt năng lượng.
Câu 11:
16/07/2024Một số quá trình tự nhiên và hoạt động của con người thải hydrogen sulfide vào không khí. Chất này có thể bị oxi hoá bởi oxygen có trong không khí theo hai phản ứng sau:
H2S(g) + O2(g) → SO2(g) + H2O(g) (1)
H2S(g) + O2(g) → S(s) + H2O(g) (2)
Cho biết giá trị enthalpy tạo thành chuẩn của H2S(g), SO2(g) và H2O(g) lần lượt là: −20,7 kJ mol−1; −296,8 kJ mol−1 và −241,8 kJ mol−1.
a) Tính giá trị biến thiên enthalpy chuẩn của mỗi phản ứng trên. Ở 298 K, mỗi phản ứng có thuận lợi về mặt năng lượng không?
 Xem đáp án
Xem đáp án
a) Cả hai phản ứng đều thuận lợi về mặt năng lượng vì giá trị biến thiên enthalpy chuẩn của hai phản ứng đều âm (−517,9 kJ và −221,1 kJ).
Câu 12:
21/07/2024b) Trong môi trường không khí mà nồng độ oxygen bị suy giảm, hãy dự đoán hydrogen sulfide sẽ dễ chuyển hoá thành sulfur dioxide hay sulfur. Giải thích.
 Xem đáp án
Xem đáp án
b) Hydrogen sulfide sẽ dễ chuyển thành sulfur theo phản ứng (2), vì phản ứng (2) cần ít oxygen hơn so với phản ứng (1).
Câu 13:
22/07/2024Bột đá vôi có thể được sử dụng để xử lí khí thải chứa sulfur dioxide từ các nhà máy điện đốt than và dầu mỏ. Phương trình hoá học của phản ứng là:
CaCO3(s) + SO2(g) ⟶ CaSO3(s) + CO2(g)
a) Vì sao phản ứng trên được gọi là phản ứng khử sulfur trong khí thải?
 Xem đáp án
Xem đáp án
a) Phản ứng trên được gọi là phản ứng khử sulfur trong khí thải vì S trong khí thải (SO2) được thay thế bằng C (trong CO2).
Câu 14:
10/07/2024b) Tính giá trị biến thiên enthalpy chuẩn của phản ứng trên theo số liệu giá trị enthalpy tạo thành chuẩn của các hợp chất trong bảng sau đây. Cho biết phản ứng có thuận lợi về mặt năng lượng không.
|
Hợp chất |
CaSO3(s) |
CaCO3(s) |
SO2(g) |
CO2(g) |
|
(kJ mol−1) |
−1 634,9 |
−1 207,6 |
−296,8 |
−393,5 |
 Xem đáp án
Xem đáp án
b) = [−1634,9 + (−393,5)] – [−1207,6 + (−296,8)] = −524,0 kJ.
Phản ứng toả nhiệt nên thuận lợi về năng lượng.
Câu 15:
18/07/2024c) Trong phản ứng trên, vì sao đá vôi phải được dùng ở dạng bột?
 Xem đáp án
Xem đáp án
c) Sử dụng đá vôi ở dạng bột để tăng diện tích tiếp xúc giữa calcium carbonate với khí nhằm tăng tốc độ phản ứng.
Câu 16:
08/07/2024d) Calcium sulfite (CaSO3) thường được chuyển hoá thành thạch cao có công thức CaSO4.2H2O. Phản ứng hoá học chuyển CaSO3 thành CaSO4.2H2O có thuộc loại phản ứng oxi hoá − khử không? Giải thích.
 Xem đáp án
Xem đáp án
d) Phản ứng hoá học chuyển CaSO3 thành CaSO4.2H2O là phản ứng oxi hoá − khử vì làm tăng số oxi hoá của sulfur từ +4 (trong CaSO3) lên +6 (trong CaSO4).
