Giải SBT Hóa học 10 Bài 12. Liên kết cộng hóa trị có đáp án
Giải SBT Hóa học 10 Bài 12. Liên kết cộng hóa trị có đáp án
-
49 lượt thi
-
16 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 1:
13/07/2024Liên kết cộng hóa trị là liên kết hóa học được hình thành giữa hai nguyên tử bằng
 Xem đáp án
Xem đáp án
Liên kết cộng hóa trị là liên kết hóa học được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung
Ví dụ: Liên kết cộng hóa trị trong phân tử HCl
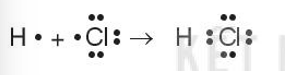
Câu 2:
17/07/2024Hợp chất nào sau đây có liên kết cộng hóa trị không phân cực?
 Xem đáp án
Xem đáp án
Hiệu độ âm điện trong phân tử N2 bằng 0.
Câu 3:
19/07/2024Hợp chất nào sau đây có liên kết cộng hóa trị phân cực?
 Xem đáp án
Xem đáp án
- H2 và N2 có hiệu độ âm điện bằng 0 ⇒ Có liên kết cộng hóa trị không phân cực.
- Hợp chất CHCl3 gồm 1 liên kết C-H và 3 liên kết C-Cl
Hợp chất CH4 gồm 4 liên kết C-H
(C-H) = |2,55 – 2,2| = 0,35 ⇒ Liên kết cộng hóa trị không phân cực
(C-Cl) = |2,55 – 3,16| = 0,61 ⇒ Liên kết cộng hóa trị phân cực.
Vậy hợp chất CHCl3 có liên kết cộng hóa trị không phân cực.Câu 4:
17/07/2024 Xem đáp án
Xem đáp án
Liên kết σ là liên kết hình thành do sự xen phủ trục của hai orbital.
Ví dụ:
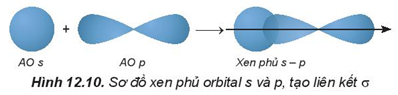
Câu 5:
13/07/2024 Xem đáp án
Xem đáp án
Liên kết π là liên kết hình thành do sự xen phủ bên của hai orbital
Câu 6:
13/07/2024Liên kết trong phân tử nào sau đây được hình thành nhờ sự xen phủ orbital p – p?
 Xem đáp án
Xem đáp án
H (Z = 1): 1s1
Cl (Z = 17): 1s22s22p63s23p5
N (Z = 7): 1s22s22p3
A. Liên kết trong phân tử H2 được hình thành nhờ sự xem phủ orbital s – s.
B. Liên kết trong phân tử Cl2 được hình thành bởi sự xen phủ orbital p – p.
C. Liên kết trong phân tử NH3 được hình thành bởi sự xen phủ orbital s – p.
D. Liên kết trong phân tử HCl được hình thành bởi sự xen phủ orbital s – p.
Câu 7:
21/07/2024Liên kết trong phân tử nào sau đây được hình thành nhờ sự xen phủ orbital s – s?
 Xem đáp án
Xem đáp án
H (Z = 1): 1s1
Cl (Z = 17): 1s22s22p63s23p5
N (Z = 7): 1s22s22p3
A. Liên kết trong phân tử H2 được hình thành nhờ sự xem phủ orbital s – s.
B. Liên kết trong phân tử Cl2 được hình thành bởi sự xen phủ orbital p – p.
C. Liên kết trong phân tử NH3 được hình thành bởi sự xen phủ orbital s – p.
D. Liên kết trong phân tử HCl được hình thành bởi sự xen phủ orbital s – p.
Câu 8:
23/07/2024Liên kết trong phân tử nào sau đây được hình thành nhờ sự xen phủ orbital s – p?
 Xem đáp án
Xem đáp án
H (Z = 1): 1s1
Cl (Z = 17): 1s22s22p63s23p5
N (Z = 7): 1s22s22p3
O (Z = 8): 1s22s22p4
A. Liên kết trong phân tử H2 được hình thành nhờ sự xem phủ orbital s – s.
B. Liên kết trong phân tử Cl2 được hình thành bởi sự xen phủ orbital p – p.
C. Liên kết trong phân tử NH3 được hình thành bởi sự xen phủ orbital s – p.
D. Liên kết trong phân tử O2 được hình thành bởi sự xen phủ orbital p – p.
Câu 9:
23/07/2024Các liên kết trong phân tử oxygen gồm
 Xem đáp án
Xem đáp án
Trong phân tử oxygen (O2) hai nguyên tử O liên kết với nhau bằng 1 liên kết đôi (O=O).
1 liên kết đôi gồm 1 liên kết σ, 1 liên kết π
Câu 10:
23/07/2024Số liên kết σ và π có trong phân tử C2H2 lần lượt là
 Xem đáp án
Xem đáp án
Công thức cấu tạo của C2H2 là: H-C≡C-H
Liên kết 3 gồm 1 liên kết σ và 2 liên kết π.
⇒ Tổng số liên kết σ và π có trong phân tử C2H2 lần lượt là: 3 và 2
Câu 11:
16/07/2024Dãy nào sau đây gồm các chất chỉ có liên kết cộng hóa trị?
 Xem đáp án
Xem đáp án
A. BaCl2 và NaCl chứa liên kết ion.
B. Na2O2 chứa liên kết ion
D. CaCl2 chứa liên kết ion.
Câu 12:
23/07/2024Cho hai nguyên tố X (Z = 20) và Y (Z = 17). Công thức hợp chất tạo thành từ nguyên tố X, Y và liên kết trong phân tử là
 Xem đáp án
Xem đáp án
X (Z = 20): 1s22s22p63s23p64s2
Y (Z = 17): 1s22s22p63s23p5
Nguyên tử X là kim loại mạnh, có xu hướng nhường đi 2 electron lớp ngoài cùng tạo thành cation X2+.
Nguyên tử Y là phi kim điển hình, có xu hướng nhận thêm 1 electron và lớp ngoài cùng tạo thành anion Y-.
Ion X2+ và Y- trái dấu hút nhau tạo thành phân tử XY2. Liên kết được tạo thành là liên kết ion.
X2+ + 2Y- → XY2
Câu 13:
13/07/2024Độ âm điện của nitrogen gần bằng độ âm điện của chlorine nhưng ở điều kiện thường N2 hoạt động kém hơn Cl2. Giải thích.
 Xem đáp án
Xem đáp án
Tuy có độ âm điện của chlorine và nitrogen gần bằng nhau nhưng do trong phân tử Cl2 có liên kết đơn σ (Cl-Cl) còn trong phân tử N2 có liên kết ba (N≡N) gồm 1 liên kết σ và 2 liên kết π rất bền vững. Năng lượng cần để phá vỡ liên kết ba trong phân tử N2 lớn hơn nhiều so với năng lượng cần để phá vỡ một liên kết đơn trong phân tử Cl2. Do đó, ở điều kiện thường, N2 hoạt động kém Cl2.
Câu 14:
23/07/2024Cho các phân tử sau: F2, N2, H2O, CO2.
a) Hãy viết công thức Lewis của các phân tử đó.
b) Hãy cho biết phân tử nào chứa liên kết cộng hóa trị phân cực và phân tử nào chứa liên kết cộng hóa trị không phân cực; phân tử nào phân cực và phân tử nào không phân cực?
 Xem đáp án
Xem đáp án
a) Công thức Lewis của các phân tử:
F2 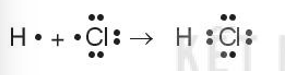
N2 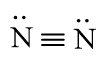
H2OD 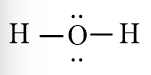
CO2 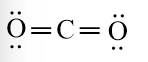
b) Phân tử chứa liên kết cộng hóa trị không phân cực: N2, F2.
Phân tử chứa liên kết cộng hóa trị phân cực: H2O, CO2.
Phân tử phân cực: H2O.
Phân tử không phân cực: N2, F2, CO2.
Câu 15:
20/07/2024Cho các phân tử sau: Br2, H2S, CH4, NH3, C2H4, C2H2
a) Phân tử nào có liên kết cộng hóa trị không phân cực? Phân tử nào có liên kết cộng hóa trị phân cực?
b) Phân tử nào chỉ có liên kết đơn? Phân tử nào có liên kết đôi? Phân tử nào có liên kết ba?
 Xem đáp án
Xem đáp án
a) Phân tử có liên kết cộng hóa trị không phân cực: Br2.
Phân tử có liên kết cộng hóa trị phân cực: H2S, CH4, NH3, C2H4 và C2H2.
b) Phân tử chỉ có liên kết đơn: H2S, CH4, NH3 và Br2.
Phân tử có liên kết đôi: CH2=CH2.
Phân tử có liên kết ba: CH≡CH.
Câu 16:
13/07/2024Ghép nhiệt độ nóng chảy với chất tương ứng và giải thích
|
Chất |
Nhiệt độ nóng chảy (oC) |
|
a) Nước |
1) -138 |
|
b) Muối ăn |
2) 80 |
|
c) Băng phiến |
3) 0 |
|
d) Butane |
4) 801 |
 Xem đáp án
Xem đáp án
a) - 3);
b) – 4);
c) – 2);
d) – 1).
Nước, băng phiến, butane là các hợp chất cộng hóa trị, phân tử có độ phân cực không cao nên dễ tách ra khỏi nhau khi đun nóng. Ngược lại, NaCl là tinh thể ion có lực hút mạnh giữa các ion nên khó tách ra khỏi nhau và có nhiệt độ nóng chảy cao.
