Giải SBT Hóa 10 Bài 10: Liên kết ion có đáp án
Giải SBT Hóa 10 Bài 10: Liên kết ion có đáp án
-
92 lượt thi
-
13 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 1:
14/07/2024Phân loại các hợp chất ion dưới đây vào các nhóm sau: hợp chất tạo nên bởi các ion đơn nguyên tử, hợp chất tạo nên bởi ion đơn nguyên tử và đa nguyên tử, hợp chất tạo nên bởi các ion đa nguyên tử.
KCl, Na2CO3, (NH4)2SO4, BaCO3, AgCl, BaSO4, KMnO4.
 Xem đáp án
Xem đáp án
Chú ý:
- Ion đơn nguyên tử là ion được tạo nên từ một nguyên tử, ví dụ: Cl-; Na+ …
- Ion đa nguyên tử là ion được tạo nên từ nhiều nguyên tử liên kết với nhau để thành một nhóm nguyên tử mang điện tích dương hoặc âm, ví dụ: NH4+; SO42- …
Vậy:
+ Hợp chất tạo nên bởi các ion đơn nguyên tử: KCl; AgCl.
+ Hợp chất tạo nên bởi ion đơn nguyên tử và đa nguyên tử: Na2CO3, BaCO3, BaSO4, KMnO4.
+ Hợp chất tạo nên bởi các ion đa nguyên tử: (NH4)2SO4.
Câu 2:
13/07/2024Cho các ion: Na+, Ca2+, F-, CO32-. Số lượng các hợp chất chứa hai loại ion có thể tạo thành từ các ion này là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các hợp chất chứa hai loại ion có thể tạo thành từ các ion này là: NaF; Na2CO3; CaF2; CaCO3.
Câu 3:
18/07/2024Cặp nguyên tố nào sau đây có khả năng tạo thành liên kết ion trong hợp chất của chúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Liên kết ion được tạo thành giữa kim loại điển hình và phi kim điển hình.
Vậy liên kết giữa calcium và oxygen là liên kết ion.
Câu 4:
22/07/2024Những đặc điểm nào sau đây là đúng khi nói về hợp chất tạo thành giữa Na+ và O2-?
A. Là hợp chất ion.
B. Có công thức hoá học là NaO.
C. Trong điều kiện thường, tồn tại ở thể khí.
D. Trong điều kiện thường, tồn tại ở thể rắn.
E. Có nhiệt độ nóng chảy và nhiệt độ sôi cao.
G. Có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
H. Lực tương tác giữa Na+ và O2- là lực tĩnh điện.
 Xem đáp án
Xem đáp án
Đáp án đúng là: A, D, E, H
B sai vì công thức hóa học là Na2O.
C sai vì hợp chất này ở thể rắn trong điều kiện thường.
G sai vì hợp chất này có nhiệt độ nóng chảy và nhiệt độ sôi cao.
Câu 5:
21/07/2024ZnO là một hợp chất ion được sử dụng nhiều trong kem chống nắng. Bán kính của nguyên tử O như thế nào so với bán kính của anion O2- trong tinh thể ZnO?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Bán kính của O nhỏ hơn bán kính của O2- do khi nhận thêm electron thì lực đẩy giữa các electron tăng lên, làm giảm lực hút giữa hạt nhân với các electron dẫn đến electron ở xa hạt nhân hơn.
Câu 6:
22/07/2024Bán kính của nguyên tử Al như thế nào so với bán kính của cation Al3+ trong tinh thể AlCl3?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Bán kính của Al lớn hơn bán kính của Al3+ do khi hình thành cation, nguyên tử sẽ mất bớt electron, lực hút của hạt nhân với các electron tăng lên, electron sẽ ở gần hạt nhân hơn.
Câu 7:
13/07/2024Ghép mỗi nguyên tử ở cột A với các giá trị điện tích của ion mà nguyên tử có thể tạo thành ở cột B.
|
Cột A |
Cột B |
|
a) S b) Al c) F d) Mg |
1. điện tích 2+ 2. điện tích 3+ 3. điện tích 2 – 4. điện tích 1 – |
 Xem đáp án
Xem đáp án
- a ghép với 3, giải thích:
S có 6 electron ở lớp ngoài cùng, có xu hướng nhận thêm 2 electron để tạo thành ion S2-. Vậy điện tích của ion là 2 –.
- b ghép với 2, giải thích:
Al có 3 electron ở lớp ngoài cùng, có xu hướng nhường đi 3 electron để tạo thành ion Al3+. Vậy điện tích của ion là 3+.
- c ghép với 4, giải thích:
F có 7 electron ở lớp ngoài cùng, có xu hướng nhận thêm 1 electron để tạo thành ion F-. Vậy điện tích của ion là 1 –.
- d ghép với 1, giải thích:
Mg có 2 electron ở lớp ngoài cùng, có xu hướng nhường đi 2 electron để tạo thành ion Mg2+. Vậy điện tích của ion là 2+.
Câu 8:
20/07/2024Chọn phương án đúng để hoàn thành câu sau:
Khi hình thành các hợp chất ion, ...(1)... mất các electron hoá trị của chúng để tạo thành ...(2)... mang điện tích dương và ...(3)... nhận các electron hoá trị để tạo thành ...(4)... mang điện tích âm.
A. (1) kim loại, (2) anion, (3) phi kim, (4) cation.
B. (1) phi kim, (2) cation, (3) kim loại, (4) anion.
C. (1) kim loại, (2) ion đa nguyên tử, (3) phi kim, (4) anion.
D. (1) phi kim, (2) anion, (3) kim loại, (4) cation.
E. (1) kim loại, (2) cation, (3) phi kim, (4) anion.
 Xem đáp án
Xem đáp án
Đáp án đúng là: E
Khi hình thành các hợp chất ion, (1) kim loại mất các electron hoá trị của chúng để tạo thành (2) cation mang điện tích dương và (3) phi kim nhận các electron hoá trị để tạo thành (4) anion mang điện tích âm.
Câu 9:
23/07/2024Điền từ thích hợp vào chỗ trống:
Barium thuộc nhóm IIA, iodine thuộc nhóm VIIA, hợp chất của hai nguyên tố này là hợp chất ...(1)... Ở điều kiện thường, hợp chất này tồn tại ở thể ...(2)... với cấu trúc tinh thể tạo nên bởi ...(3)... và ...(4)...
 Xem đáp án
Xem đáp án
Câu 10:
16/07/2024Viết hai giai đoạn của sự hình thành CaF2, từ các nguyên tử tương ứng (kèm theo cấu hình electron).
 Xem đáp án
Xem đáp án
Giai đoạn 1: Hình thành ion trái dấu theo quy tắc octet từ các quá trình kim loại (Ca) nhường electron và phi kim (F) nhận electron.
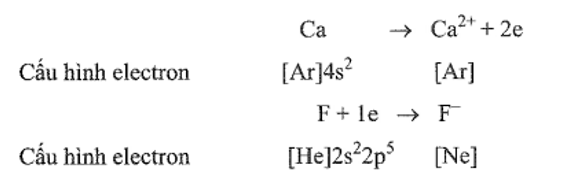
Giai đoạn 2: Các ion trái dấu hút nhau bằng lực hút tĩnh điện tạo nên hợp chất ion:
Ca2+ + 2F- → CaF2.
Câu 11:
23/07/2024Cho biết sự tạo thành NaCl (s) từ Na (s) và Cl2 (g) giải phóng nhiều năng lượng. Hãy cho biết năng lượng giải phóng có nguồn gốc từ đâu.
Gợi ý: Nếu các tiểu phân hút nhau sẽ giải phóng năng lượng, đẩy nhau sẽ hấp thu năng lượng.
 Xem đáp án
Xem đáp án
Câu 12:
17/07/2024Biết rằng năng lượng toả ra khi hình thành các hợp chất ion từ các cation và anion tỉ lệ thuận với điện tích của mỗi ion và tỉ lệ nghịch với bán kính của chúng. Dựa trên cơ sở này, hãy cho biết khi hình thành hợp chất nào trong mỗi cặp chất sau đây từ các ion tương ứng thì năng lượng tỏa ra là nhiều hơn.
a) LiCl và NaCl
 Xem đáp án
Xem đáp án
a) Khi hình thành hợp chất LiCl thì năng lượng tỏa ra là nhiều hơn. Giải thích:
Do khi tạo thành hợp chất LiCl hay NaCl thì đều đi từ các cation có điện tích 1+ và anion có điện tích 1-, nhưng bán kính của Li+ nhỏ hơn của Na+ nên lực hút tĩnh điện giữa Li+ với Cl- sẽ mạnh hơn và tỏa nhiều năng lượng hơn so với Na+.
Câu 13:
13/07/2024b) Na2O và MgO.
 Xem đáp án
Xem đáp án
b) Khi hình thành hợp chất MgO thì năng lượng tỏa ra là nhiều hơn. Giải thích:
Do khi tạo thành Na2O thì cation mang điện tích 1+ (Na+) còn khi tạo thành MgO thì cation mang điện tích 2+ (Mg2+) nên lực hút giữa Mg2+ với O2- sẽ mạnh hơn nhiều so với Na+ và O2-, do đó năng lượng tỏa ra khi tạo thành MgO cũng nhiều hơn.
