Câu hỏi:
17/07/2024 134
Viết ô orbital của lớp electron ngoài cùng cho nguyên tử H và Cl. Từ đó chỉ ra những AO nào có thể xen phủ tạo liên kết đơn trong các phân tử H2, Cl2 và HCl.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
- Cấu hình electron nguyên tử H (Z = 1): 1s1.
Ô orbital của lớp electron ngoài cùng:

- Cấu hình electron nguyên tử Cl (Z = 17): 1s22s22p63s23p5.
Ô orbital của lớp electron ngoài cùng:
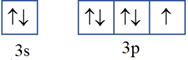
Nhận xét:
- 1 AO s xen phủ với 1 AO s tạo thành phân tử H2.
- 1 AO p xen phủ với 1 AO p tạo thành phân tử Cl2.
- 1 AO s (H) xen phủ với 1 AO p (Cl) tạo thành phân tử HCl.
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Nguyên tử Z có 7 neutron và 6 proton. Kí hiệu nguyên tử của Z là
Nguyên tử Z có 7 neutron và 6 proton. Kí hiệu nguyên tử của Z là
Câu 3:
Giải thích vì sao tetrachloromethane (CCl4) tuy là phân tử không cực nhưng có nhiệt độ sôi cao hơn trichloromethane (CHCl3) là phân tử có cực.
Giải thích vì sao tetrachloromethane (CCl4) tuy là phân tử không cực nhưng có nhiệt độ sôi cao hơn trichloromethane (CHCl3) là phân tử có cực.
Câu 5:
Nếu đường kính của nguyên tử khoảng 102 pm thì đường kính của hạt nhân khoảng
Câu 6:
Công thức electron nào sau đây không đủ electron theo quy tắc octet?
Câu 7:
Trong các nguyên tố nhóm A, đại lượng nào sau đây không biến đổi tuần hoàn?
Câu 8:
Anion X– có cấu hình electron nguyên tử ở phân lớp ngoài cùng là 3p6.
a) Viết cấu hình electron của nguyên tử X. Cho biết X là nguyên tố kim loại hay phi kim?
Anion X– có cấu hình electron nguyên tử ở phân lớp ngoài cùng là 3p6.
a) Viết cấu hình electron của nguyên tử X. Cho biết X là nguyên tố kim loại hay phi kim?
Câu 9:
Mặc dù chlorine có độ âm điện là 3,16 xấp xỉ với nitrogen là 3,04 nhưng giữa các phân tử HCl không tạo được liên kết hydrogen với nhau, trong khi giữa các phân tử NH3 tạo được liên kết hydrogen với nhau, nguyên nhân là do
Mặc dù chlorine có độ âm điện là 3,16 xấp xỉ với nitrogen là 3,04 nhưng giữa các phân tử HCl không tạo được liên kết hydrogen với nhau, trong khi giữa các phân tử NH3 tạo được liên kết hydrogen với nhau, nguyên nhân là do
Câu 12:
Khi hình thành liên kết hóa học, nguyên tử có số hiệu nào sau đây có xu hướng nhường 2 electron để đạt tới cấu hình electron bền vững theo quy tắc octet?
Câu 13:
Trong cùng một nhóm A, theo chiều tăng của điện tích hạt nhân, những yếu tố sẽ tăng dần là
Trong cùng một nhóm A, theo chiều tăng của điện tích hạt nhân, những yếu tố sẽ tăng dần là
Câu 15:
Nguyên tố R có cấu hình electron: 1s22s22p4. Công thức hợp chất oxide ứng với hóa trị cao nhất của R là
Nguyên tố R có cấu hình electron: 1s22s22p4. Công thức hợp chất oxide ứng với hóa trị cao nhất của R là


