Câu hỏi:
04/12/2024 120
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân
A. Bán kính giảm dần, tính kim loại giảm;
B. Bán kính tăng dần, tính kim loại tăng;
C. Bán kính tăng dần, tính phi kim tăng;
D. Bán kính giảm dần, tính phi kim giảm.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: A
- Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính giảm dần, tính kim loại giảm và tính phi kim tăng dần.
- Dựa vào quy luật sự biến đổi tuần hoàn tính kim loại, tính phi kim trong một chu kì.
+ Trong một chu kì, tuy nguyên tử các nguyên tố có cùng số lớp electron, nhưng khi điện tích hạt nhân tăng, lực hút giữa hạt nhân với các electron lớp ngoài cùng cũng tăng theo, do đó bán kính nguyên tử nói chung giảm dần.
+ Trong một chu kì, theo chiều tăng của điện tích hạt nhân thì năng lượng ion hóa, độ âm điện tăng dần đồng thời bán kính nguyên tử giảm dần làm cho khả năng nhận electron tăng nên tính phi kim tăng. Và đồng thời khả năng nhường electron giảm nên tính kim loại giảm.
Vậy trong một chu kì, theo chiều tăng của điện tích hạt nhân: tính kim loại giảm, tính phi kim tăng.
→ A đúng.B,C,D sai.
* Bán kính nguyên tử.
Bán kính nguyên tử phụ thuộc vào lực hút giữa hạt nhân với các electron lớp ngoài cùng. Bán kính giảm là do lực hút tăng và ngược lại, bán kính tăng là do lực hút giảm.
Xu hướng biến đổi bán kính nguyên tử:
- Trong một chu kì, bán kính nguyên tử giảm theo chiều tăng dần của điện tích hạt nhân.
- Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.
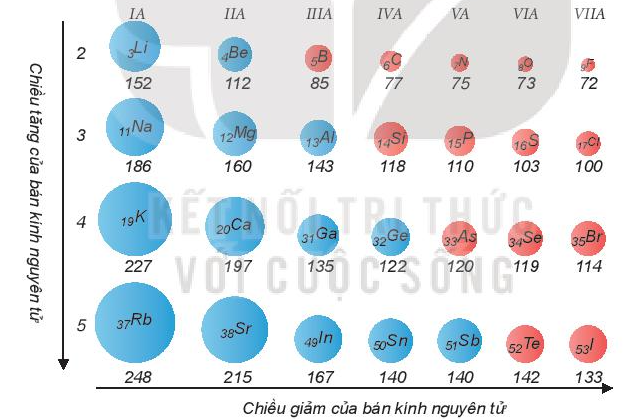
Ví dụ: So sánh bán kính nguyên tử của lithium (Z = 3) và potassium (Z = 19).
Hướng dẫn giải:
Cấu hình electron của nguyên tử:
Lithium (Z = 3): 1s22s1 Lithium thuộc chu kì 2, nhóm IA.
Potassium (Z = 19): 1s22s22p63s23p64s1 Potassium thuộc chu kì 4, nhóm IA.
Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.
Bán kính của nguyên tử lithium nhỏ hơn bán kính nguyên tử potassium.
Xem thêm các bài viết liên quan,chi tiết khác:
Đáp án đúng là: A
- Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính giảm dần, tính kim loại giảm và tính phi kim tăng dần.
- Dựa vào quy luật sự biến đổi tuần hoàn tính kim loại, tính phi kim trong một chu kì.
+ Trong một chu kì, tuy nguyên tử các nguyên tố có cùng số lớp electron, nhưng khi điện tích hạt nhân tăng, lực hút giữa hạt nhân với các electron lớp ngoài cùng cũng tăng theo, do đó bán kính nguyên tử nói chung giảm dần.
+ Trong một chu kì, theo chiều tăng của điện tích hạt nhân thì năng lượng ion hóa, độ âm điện tăng dần đồng thời bán kính nguyên tử giảm dần làm cho khả năng nhận electron tăng nên tính phi kim tăng. Và đồng thời khả năng nhường electron giảm nên tính kim loại giảm.
Vậy trong một chu kì, theo chiều tăng của điện tích hạt nhân: tính kim loại giảm, tính phi kim tăng.
→ A đúng.B,C,D sai.
* Bán kính nguyên tử.
Bán kính nguyên tử phụ thuộc vào lực hút giữa hạt nhân với các electron lớp ngoài cùng. Bán kính giảm là do lực hút tăng và ngược lại, bán kính tăng là do lực hút giảm.
Xu hướng biến đổi bán kính nguyên tử:
- Trong một chu kì, bán kính nguyên tử giảm theo chiều tăng dần của điện tích hạt nhân.
- Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.

Ví dụ: So sánh bán kính nguyên tử của lithium (Z = 3) và potassium (Z = 19).
Hướng dẫn giải:
Cấu hình electron của nguyên tử:
Lithium (Z = 3): 1s22s1 Lithium thuộc chu kì 2, nhóm IA.
Potassium (Z = 19): 1s22s22p63s23p64s1 Potassium thuộc chu kì 4, nhóm IA.
Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.
Bán kính của nguyên tử lithium nhỏ hơn bán kính nguyên tử potassium.
Xem thêm các bài viết liên quan,chi tiết khác:
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 2:
Khi xếp theo chiều tăng dần của điện tích hạt nhân, đại lượng nào sau đây không biến đổi tuần hoàn?
Khi xếp theo chiều tăng dần của điện tích hạt nhân, đại lượng nào sau đây không biến đổi tuần hoàn?
Câu 4:
Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần độ âm điện?
Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần độ âm điện?
Câu 5:
Đại lượng nào đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố hóa học khi tạo thành liên kết hóa học?
Đại lượng nào đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố hóa học khi tạo thành liên kết hóa học?
Câu 6:
Cho các phát biểu sau:
(1) F là phi kim mạnh nhất;
(2) Li có độ âm điện nhỏ nhất;
(3) H có bán kính nguyên tử nhỏ nhất;
(4) P là phi kim hoạt động mạnh nhất.
Số phát biểu đúng là?
Cho các phát biểu sau:
(1) F là phi kim mạnh nhất;
(2) Li có độ âm điện nhỏ nhất;
(3) H có bán kính nguyên tử nhỏ nhất;
(4) P là phi kim hoạt động mạnh nhất.
Số phát biểu đúng là?
Câu 7:
Yếu tố nào ảnh hưởng nhiều nhất đến tính chất hóa học của nguyên tố nhóm A?
Yếu tố nào ảnh hưởng nhiều nhất đến tính chất hóa học của nguyên tố nhóm A?
Câu 9:
Dãy nguyên tố nào sau đây sắp xếp theo chiều giảm dần của bán kính nguyên tử?
Dãy nguyên tố nào sau đây sắp xếp theo chiều giảm dần của bán kính nguyên tử?
Câu 10:
Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần của bán kính nguyên tử?
Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần của bán kính nguyên tử?
Câu 12:
Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần tính kim loại?
Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần tính kim loại?


