Câu hỏi:
16/07/2024 152
Sắp xếp các nguyên tố sau theo chiều tăng dần tính phi kim: O, S, F. Giải thích.
Sắp xếp các nguyên tố sau theo chiều tăng dần tính phi kim: O, S, F. Giải thích.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
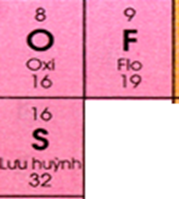
O (Z = 8) và F (Z = 9) thuộc cùng một chu kì. Theo chiều điện tích hạt nhân tăng dần ta được tính phi kim F > O (1).
O và S thuộc cùng một nhóm A. Theo chiều điện tích hạt nhân tăng dần ta được tính phi kim O > S (2)
Từ (1) và (2) ⇒ Tính phi kim F > O > S.
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Dựa vào hình 7.5, hãy nhận xét quy luật chung về sự biến đổi độ âm điện của các nguyên tử nguyên tố nhóm A trong một chu kì, trong một nhóm.
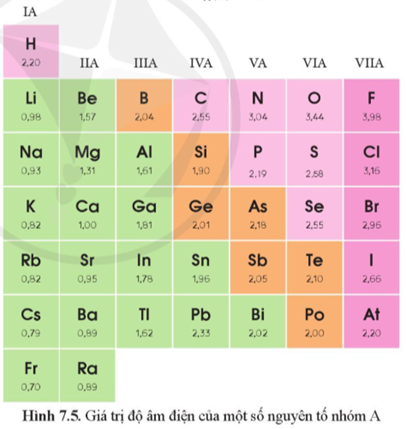
Dựa vào hình 7.5, hãy nhận xét quy luật chung về sự biến đổi độ âm điện của các nguyên tử nguyên tố nhóm A trong một chu kì, trong một nhóm.

Câu 2:
Cặp electron liên kết bị lệch nhiều hơn trong phân tử NH3 hay trong phân tử H2O? Vì sao?
Cặp electron liên kết bị lệch nhiều hơn trong phân tử NH3 hay trong phân tử H2O? Vì sao?
Câu 3:
Cấu hình electron lớp ngoài cùng của các nguyên tố chu kì 2 và 3 như sau:
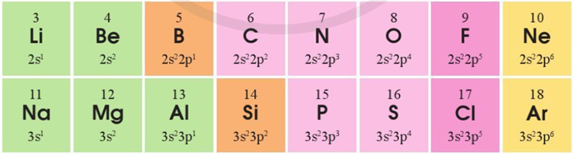
a) Sự lặp lại tuần hoàn về cấu hình electron lớp ngoài cùng của các nguyên tố chu kì 2 và 3 thể hiện như thế nào?
b*) Giải thích vì sao sự biến đổi tuần hoàn về cấu hình electron lớp ngoài cùng là nguyên nhân quyết định đến sự biến đổi tính tuần hoàn về tính chất hóa học của các đơn chất và hợp chất các nguyên tố chu kì 2 và 3. Lấy một số ví dụ để minh họa sự biến đổi đó.
Cấu hình electron lớp ngoài cùng của các nguyên tố chu kì 2 và 3 như sau:

a) Sự lặp lại tuần hoàn về cấu hình electron lớp ngoài cùng của các nguyên tố chu kì 2 và 3 thể hiện như thế nào?
b*) Giải thích vì sao sự biến đổi tuần hoàn về cấu hình electron lớp ngoài cùng là nguyên nhân quyết định đến sự biến đổi tính tuần hoàn về tính chất hóa học của các đơn chất và hợp chất các nguyên tố chu kì 2 và 3. Lấy một số ví dụ để minh họa sự biến đổi đó.
Câu 4:
Cặp electron liên kết của phân tử H2 có bị lệch về nguyên tử nào không? Vì sao?
Cặp electron liên kết của phân tử H2 có bị lệch về nguyên tử nào không? Vì sao?
Câu 5:
Các nguyên tố chu kì 2 có bao nhiêu lớp electron? Vẽ mô hình nguyên tử theo Rutherford – Bohr của Li và F để giải thích về sự khác biệt bán kính nguyên tử.
Các nguyên tố chu kì 2 có bao nhiêu lớp electron? Vẽ mô hình nguyên tử theo Rutherford – Bohr của Li và F để giải thích về sự khác biệt bán kính nguyên tử.
Câu 6:
Al(OH)3 thể hiện tính acid, tính base trong phản ứng nào trong ví dụ trên?
Al(OH)3 thể hiện tính acid, tính base trong phản ứng nào trong ví dụ trên?
Câu 7:
Một hạt nhân có điện tích +Z sẽ hút electron bằng một lực với độ lớp F = a, trong đó: r là khoảng cách từ hạt nhân tới electron, a là một hằng số. Hãy cho biết:
a) Điện tích hạt nhân càng lớn thì lực hút electron càng mạnh hay càng yếu?
b) Khoảng cách giữa electron và hạt nhân càng lớn thì electron bị hạt nhân hút càng mạnh hay càng yếu?
Một hạt nhân có điện tích +Z sẽ hút electron bằng một lực với độ lớp F = a, trong đó: r là khoảng cách từ hạt nhân tới electron, a là một hằng số. Hãy cho biết:
a) Điện tích hạt nhân càng lớn thì lực hút electron càng mạnh hay càng yếu?
b) Khoảng cách giữa electron và hạt nhân càng lớn thì electron bị hạt nhân hút càng mạnh hay càng yếu?
Câu 9:
Hãy giải thích vì sao nguyên tử He là nguyên tử nguyên tố có kích thước nhỏ nhất trong bảng tuần mà không phải là nguyên tử H.
Hãy giải thích vì sao nguyên tử He là nguyên tử nguyên tố có kích thước nhỏ nhất trong bảng tuần mà không phải là nguyên tử H.
Câu 10:
Xác định nguyên tố có tính kim loại mạnh nhất, nguyên tố có tính phi kim mạnh nhất. Giải thích.
Câu 11:
Không dùng bảng độ âm điện hãy so sánh độ âm điện của các nguyên tố X có Z = 14 và nguyên tố Y có Z = 16. Giải thích.
Không dùng bảng độ âm điện hãy so sánh độ âm điện của các nguyên tố X có Z = 14 và nguyên tố Y có Z = 16. Giải thích.
Câu 12:
Viết công thức oxide cao nhất của các nguyên tố chu kì 2, từ Li đến N.
Viết công thức oxide cao nhất của các nguyên tố chu kì 2, từ Li đến N.
Câu 13:
Những đặc trưng nào sau đây thuộc về kim loại nhóm A, những đặc trưng nào thuộc về phi kim?
(1) Dễ nhường electron
(2) Dễ nhận electron
(3) Oxide cao nhất có tính base
(4) Oxide cao nhất có tính acid
Những đặc trưng nào sau đây thuộc về kim loại nhóm A, những đặc trưng nào thuộc về phi kim?
(1) Dễ nhường electron
(2) Dễ nhận electron
(3) Oxide cao nhất có tính base
(4) Oxide cao nhất có tính acid
Câu 14:
Quan sát hình 7.2, cho biết quy luật biến đổi bán kính nguyên tử của các nguyên tố ở chu kì 3, 4, 5 theo chiều tăng dần điện tích hạt nhân.

Quan sát hình 7.2, cho biết quy luật biến đổi bán kính nguyên tử của các nguyên tố ở chu kì 3, 4, 5 theo chiều tăng dần điện tích hạt nhân.

Câu 15:
Giải thích nguyên nhân của quy luật biến đổi tính phi kim trong một chu kì, trong một nhóm.
Giải thích nguyên nhân của quy luật biến đổi tính phi kim trong một chu kì, trong một nhóm.


