Câu hỏi:
23/07/2024 7,130
Cho phản ứng sau:
2CO(g) + O2(g) → 2CO2(g)
Biết (kJ mol-1) của CO(g) và CO2(g) lần lượt là –110,53 và –393,51. Lượng nhiệt giải phóng khi chuyển 56 gam khí CO thành khí CO2 là
Cho phản ứng sau:
2CO(g) + O2(g) → 2CO2(g)
Biết (kJ mol-1) của CO(g) và CO2(g) lần lượt là –110,53 và –393,51. Lượng nhiệt giải phóng khi chuyển 56 gam khí CO thành khí CO2 là
A. 565,96 kJ.
A. 565,96 kJ.
B. 424,47 kJ.
C. 282,98 kJ.
C. 282,98 kJ.
D. 106,11 kJ.
D. 106,11 kJ.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
nCO = 2 mol.
Vậy lượng nhiệt giải phóng khi tạo 2 mol CO chính bằng :
= |2. (–393,51) – 2. (–110,53)| = 565,96 kJ.
nCO = 2 mol.
Vậy lượng nhiệt giải phóng khi tạo 2 mol CO chính bằng :
= |2. (–393,51) – 2. (–110,53)| = 565,96 kJ.
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Quá trình đốt cháy ethanol diễn ra theo phản ứng:
C2H5OH (l) + 3O2 (g) → 2CO2 (g) + 3H2O (l)
Tính của phản ứng trên từ các giá trị năng lượng liên kết sau:
EC–C = 347 kJ mol-1; EO=O = 496 kJ mol-1; EC–O = 336 kJ mol-1; EC–H = 410 kJ mol-1; EC=O = 805 kJ mol-1; EO–H = 465 kJ mol-1.
Quá trình đốt cháy ethanol diễn ra theo phản ứng:
C2H5OH (l) + 3O2 (g) → 2CO2 (g) + 3H2O (l)
Tính của phản ứng trên từ các giá trị năng lượng liên kết sau:
EC–C = 347 kJ mol-1; EO=O = 496 kJ mol-1; EC–O = 336 kJ mol-1; EC–H = 410 kJ mol-1; EC=O = 805 kJ mol-1; EO–H = 465 kJ mol-1.
Câu 2:
Cho phản ứng tổng hợp ammonia (NH3) như sau:
N2(g) + 3H2(g) → 2NH3(g)
Biết năng lượng liên kết (kJ/mol) của N≡N và H–H lần lượt là 946 và 436. Năng lượng liên kết của N–H trong ammonia là
Cho phản ứng tổng hợp ammonia (NH3) như sau:
N2(g) + 3H2(g) → 2NH3(g)
Biết năng lượng liên kết (kJ/mol) của N≡N và H–H lần lượt là 946 và 436. Năng lượng liên kết của N–H trong ammonia là
Câu 3:
Cho phản ứng: C3H8(g) ⟶ CH4(g) + C2H4(g).
Giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn được cho ở bảng sau:
Liên kết
C – H
C – C
C = C
Eb (kJ/mol)
418
346
612
Nhận xét nào sau đây là sai?
Cho phản ứng: C3H8(g) ⟶ CH4(g) + C2H4(g).
Giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn được cho ở bảng sau:
|
Liên kết |
C – H |
C – C |
C = C |
|
Eb (kJ/mol) |
418 |
346 |
612 |
Nhận xét nào sau đây là sai?
Câu 4:
Tính lượng nhiệt tỏa ra ở điều kiện chuẩn khi đốt cháy 2 gam butane (C4H10) chứa trong một chiếc bật lửa gas. Biết sản phẩm của sự đốt cháy là khí carbon dioxide và hơi nước.
Cho của C4H10 (g), CO2 (g) và H2O (l) lần lượt là –126,15 kJ mol-1, –393,51 kJ mol-1 và –285,83 kJ mol-1.
Tính lượng nhiệt tỏa ra ở điều kiện chuẩn khi đốt cháy 2 gam butane (C4H10) chứa trong một chiếc bật lửa gas. Biết sản phẩm của sự đốt cháy là khí carbon dioxide và hơi nước.
Cho của C4H10 (g), CO2 (g) và H2O (l) lần lượt là –126,15 kJ mol-1, –393,51 kJ mol-1 và –285,83 kJ mol-1.
Câu 5:
Cho phản ứng sau:
2NaCl(s) → 2Na(s) + Cl2(g)
Biết (kJ mol-1) của NaCl là –411,2. Trong quá trình nấu ăn, dù bị đun nóng nhưng muối ăn không bị phân hủy thành khí Cl2 độc, vì
Cho phản ứng sau:
2NaCl(s) → 2Na(s) + Cl2(g)
Biết (kJ mol-1) của NaCl là –411,2. Trong quá trình nấu ăn, dù bị đun nóng nhưng muối ăn không bị phân hủy thành khí Cl2 độc, vì
Câu 6:
Ở nhiệt độ 25oC và áp suất 1 bar, trong số các đơn chất halogen sau, đơn chất có enthalpy tạo thành chuẩn khác 0 là
Ở nhiệt độ 25oC và áp suất 1 bar, trong số các đơn chất halogen sau, đơn chất có enthalpy tạo thành chuẩn khác 0 là
Câu 7:
Cho phản ứng sau:
CH4(g) + Cl2(g) → CH3Cl(g) + HCl(g)
Biến thiên enthalpy chuẩn của phản ứng trên tính theo năng lượng liên kết là
Cho phản ứng sau:
CH4(g) + Cl2(g) → CH3Cl(g) + HCl(g)
Biến thiên enthalpy chuẩn của phản ứng trên tính theo năng lượng liên kết là
Câu 8:
Dưới tác dụng của các chất xúc tác, glucose lên men tạo thành ethanol:
C6H12O6 2C2H5OH + 2CO2 (1)
Ethanol sinh ra lên men thành acetic acid:
C2H5OH + O2 CH3COOH + H2O (2)
Giả sử hiệu suất cả quá trình là 60%. Lượng glucose cần dùng để thu được 1 lít acetic acid 1M là
Dưới tác dụng của các chất xúc tác, glucose lên men tạo thành ethanol:
C6H12O6 2C2H5OH + 2CO2 (1)
Ethanol sinh ra lên men thành acetic acid:
C2H5OH + O2 CH3COOH + H2O (2)
Giả sử hiệu suất cả quá trình là 60%. Lượng glucose cần dùng để thu được 1 lít acetic acid 1M là
Câu 9:
Cho 2,34 gam kim loại M (có hóa trị không đổi là n) tác dụng với dung dịch H2SO4 (đặc nóng, dư) thu được 3,2227 L SO2 (điều kiện chuẩn). Kim loại M là
Cho 2,34 gam kim loại M (có hóa trị không đổi là n) tác dụng với dung dịch H2SO4 (đặc nóng, dư) thu được 3,2227 L SO2 (điều kiện chuẩn). Kim loại M là
Câu 11:
Trong giai đoạn đầu sản xuất nitric acid từ ammonia. Ammonia bị oxi hóa bởi oxygen ở nhiệt độ cao khi có chất xúc tác.
Tổng hệ số cân bằng (là các số nguyên, tối giản) của phản ứng là
Trong giai đoạn đầu sản xuất nitric acid từ ammonia. Ammonia bị oxi hóa bởi oxygen ở nhiệt độ cao khi có chất xúc tác.
Tổng hệ số cân bằng (là các số nguyên, tối giản) của phản ứng là
Câu 12:
Cho giản đồ năng lượng của các phản ứng 1 – 5 như sau:
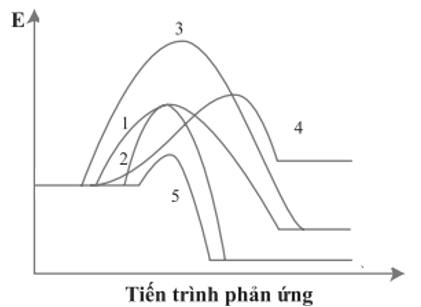
Số phản ứng toả nhiệt là
Cho giản đồ năng lượng của các phản ứng 1 – 5 như sau:

Số phản ứng toả nhiệt là
Câu 13:
Dẫn khí CO đi qua ống sứ đựng bột CuO nung nóng để thực hiện phản ứng hóa học sau: CuO + CO Cu + CO2. Trong phản ứng trên, chất đóng vai trò chất khử là
Dẫn khí CO đi qua ống sứ đựng bột CuO nung nóng để thực hiện phản ứng hóa học sau: CuO + CO Cu + CO2. Trong phản ứng trên, chất đóng vai trò chất khử là
Câu 14:
Cho phản ứng: N2(g) + O2(g) → 2NO(g). Biết năng lượng liên kết trong các phân tử O2, N2 và NO lần lượt là 494 kJ/mol, 945 kJ/mol và 607 kJ/mol. Phát biểu đúng là
Cho phản ứng: N2(g) + O2(g) → 2NO(g). Biết năng lượng liên kết trong các phân tử O2, N2 và NO lần lượt là 494 kJ/mol, 945 kJ/mol và 607 kJ/mol. Phát biểu đúng là


