Câu hỏi:
06/07/2024 123Cấu hình e của nguyên tử có số hiệu Z = 17 là:
A. 1s22s22p63s23p44s1
B. 1s22s22p63s23d5
C. 1s22s22p63s23p5
D. 1s22s22p63s23p34s2
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Chọn đáp án C
Cấu hình e của nguyên tử có số hiệu Z = 17 là: 1s22s22p63s23p5
Lưu ý: Cách viết cấu hình electron:
Bước 1: Xác định số electron của nguyên tử.
Bước 2: Điền các electron của nguyên tử vào các phân lớp theo sơ đồ năng lượng (đầy phân lớp trong mới điền ra phân lớp ngoài).
Bước 3: Khi bắt đầu có phân lớp 3d xuất hiện thì ta phải sắp xếp lại (không điền lại) các phân lớp thành từng lớp theo thứ tự tăng dần. Ta được cấu hình electron.
Sơ đồ mức năng lượng: 1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p….
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Nguyên tử X có 19 electron. Ở trạng thái cơ bản X có số obitan chứa e là :
Câu 5:
Nguyên tử nguyên tố Y có tổng số hạt cơ bản là 52, trong đó số hạt không mang điện lớn gấp 1,059 lần số hạt mang điện tích dương. Kết luận nào dưới đây là không đúng với Y ?
Câu 6:
Nguyên tử của nguyên tố X có tổng số electron ở các phân lớp p là 11. Nguyên tố X thuộc loại nguyên tố
Câu 7:
Tổng số hạt cơ bản (p, n, e) của nguyên tử X là 40, cấu hình electron của nguyên tử X là
Câu 8:
Nguyên tử X có tổng số hạt p,n,e là 52 và số khối là 35. Cấu hình electron của X là
Câu 9:
Nguyên tử của nguyên tố X có tổng số electron ở phân lớp d là 6. Nguyên tố X thuộc loại nguyên tố
Câu 10:
Nguyên tử của nguyên tố A và B đều có phân lớp ngoài cùng là 2p. Tổng số e ở hai phân lớp ngoài cùng hai nguyên tử này là 3. Vậy số hiệu nguyên tử của A và B lần lượt là:
Câu 12:
Nguyên tử R mất đi 1 electron tạo ra cation R+ có cấu hình electron ở phân lớp ngoài cùng là 2p6. Cấu hình electron và số hiệu nguyên tử của R lần lượt là
Câu 13:
Cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố X được phân bố như sau :
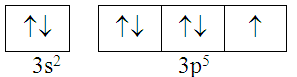
Số hiệu nguyên tử và kí hiệu của nguyên tố X là
Câu 14:
Cấu hình electron của nguyên tố X là 1s22s22p63s1. Biết rằng X có số khối là 24 thì trong hạt nhân của X có:
Câu 15:
Đối với năng lượng của các phân lớp theo nguyên lý vững bền, trường hợp nào sau đây không đúng ?


