Câu hỏi:
21/07/2024 6,461Tính 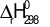 của phản ứng đốt cháy 21 gam CO (g) biết các sản phẩm thu được đều ở thể khí.
của phản ứng đốt cháy 21 gam CO (g) biết các sản phẩm thu được đều ở thể khí.
Cho enthalpy tạo thành chuẩn của các chất tương ứng là
|
Chất |
CO (g) |
CO2 (g) |
O2 (g) |
|
|
- 110,5 |
− 393,5 |
0 |
A. – 59,43 kJ;
B. – 283 kJ;
C. − 212,25 kJ;
D. – 3962 kJ.
Trả lời:
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: C
CO (g) +  O2 (g) ⟶ CO2 (g)
O2 (g) ⟶ CO2 (g)
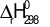 của phản ứng đốt cháy 1 mol CO (g) là
của phản ứng đốt cháy 1 mol CO (g) là
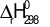 =
= 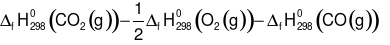
= 
= − 283 (kJ)
21 gam CO có số mol là: nCO =  = 0,75 (mol)
= 0,75 (mol)
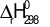 của phản ứng đốt cháy 21 gam CO (g) là:
của phản ứng đốt cháy 21 gam CO (g) là: 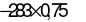 = − 212,25 (kJ)
= − 212,25 (kJ)
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1:
Tính biến thiên enthalpy chuẩn của phản ứng nhiệt nhôm và cho biết đây là phản ứng tỏa nhiệt hay thu nhiệt.
2Al (s) + Fe2O3 (s)  2Fe (s) + Al2O3 (s)
2Fe (s) + Al2O3 (s)
Biết  của Fe2O3 (s) và Al2O3 (s) lần lượt là -825,5 kJ/mol; -1676 kJ/mol
của Fe2O3 (s) và Al2O3 (s) lần lượt là -825,5 kJ/mol; -1676 kJ/mol
Câu 3:
Cho phản ứng có dạng: aA + bB ⟶ mM + nN
Công thức tính biến thiên enthalpy phản ứng theo enthalpy tạo thành là
Câu 4:
Cho phương trình nhiệt hóa học sau:
SO2 (g) +  O2 (g)
O2 (g) 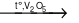 SO3 (g)
SO3 (g) 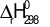 = − 98,5 kJ
= − 98,5 kJ
Lượng nhiệt giải phóng ra khi chuyển 76,8 gam SO2 (g) thành SO3 (g) là
Câu 5:
Cho phản ứng: NH3 (g) + HCl (g) ⟶ NH4Cl (s)
Biết 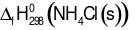 = − 314,4 kJ/mol;
= − 314,4 kJ/mol; 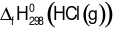 = − 92,31 kJ/mol;
= − 92,31 kJ/mol; 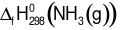 = − 45,9 kJ/mol.
= − 45,9 kJ/mol.
Biến thiên enthalpy chuẩn của phản ứng tính là
Câu 6:
Tính 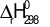 của phản ứng đốt cháy 1 mol C2H2 (g) biết các sản phẩm thu được đều ở thể khí.
của phản ứng đốt cháy 1 mol C2H2 (g) biết các sản phẩm thu được đều ở thể khí.
Cho enthalpy tạo thành chuẩn của các chất tương ứng là
|
Chất |
C2H2 (g) |
CO2 (g) |
H2O (g) |
|
|
+ 227 |
− 393,5 |
− 241,82 |
Câu 7:
Cho phản ứng có dạng: aA (g) + bB (g) ⟶ mM (g) + nN (g)
Công thức tính biến thiên enthalpy phản ứng theo năng lượng liên kết Eb là
Câu 8:
Tính lượng nhiệt sinh ra khi đốt cháy hoàn toàn 7,8 gam C6H6 (l)
Cho enthalpy tạo thành chuẩn của các chất tương ứng là
|
Chất |
C6H6 (l) |
CO2 (g) |
H2O (g) |
|
|
+49 |
− 393,5 |
-241,82 |
Câu 9:
Cho phương trình nhiệt hóa học sau:
2H2 (g) + O2 (g) ⟶ 2H2O (g) 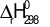 = − 483,64 kJ
= − 483,64 kJ
So sánh đúng là
Câu 10:
Cho phản ứng sau ở điều kiện chuẩn:
2H2 (g) + O2 (g)  2H2O (g)
2H2O (g)
Biến thiên enthalpy chuẩn của phản ứng trên tính theo năng lượng liên kết là
Câu 11:
Cho phản ứng:
4HCl (g) + O2 (g)  2Cl2 (g) + 2 H2O (g)
2Cl2 (g) + 2 H2O (g)
Biến thiên enthalpy chuẩn của phản ứng trên tính theo năng lượng liên kết là bao nhiêu? Phản ứng tỏa nhiệt hay thu nhiệt?
Câu 12:
Sự phá vỡ liên kết cần ….. năng lượng, sự hình thành liên kết …... năng lượng.
Cụm từ tích hợp điền vào chỗ chấm trên lần lượt là
Câu 13:
Cho phản ứng:
3O2 (g)⟶2O3 (g) (1)
2O3 (g) ⟶ 3O2 (g) (2)
Biết phân tử O3 gồm 1 liên kết đôi O = O và 1 liên kết đơn O – O.
So sánh 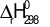 của hai phản ứng là
của hai phản ứng là
Câu 14:
Để tính biến thiên enthalpy phản ứng theo năng lượng liên kết, phải viết được


